
PAMEZONE
ESOMEPRAZOL
Cápsulas con microgránulos
28 Cápsulas , 20 Miligramos
28 Cápsulas , 40 Miligramos
Cápsulas con microgránulos , 20 Miligramos
Cápsulas con microgránulos , 40 Miligramos
COMPOSICIÓN:
PAMEZONE 20:
Cada CÁPSULA CON MICROGRÁNULOS GASTRORRESISTENTES contiene:
Esomeprazol magnésico trihidrato
(equivalente a 20 mg esomeprazol) 22,2 mg
Excipientes c.s.p.
PAMEZONE 40:
Cada CÁPSULA CON MICROGRÁNULOS GASTRORRESISTENTES contiene:
Esomeprazol magnésico trihidrato
(equivalente a 40 mg esomeprazol) 44,4 mg
Excipientes c.s.p.
FÓRMULA:
PAMEZONE 20:
Cada CÁPSULA CON MICROGRÁNULOS GASTRORRESISTENTES contiene: Esomeprazol magnésico trihidrato 22,2 mg (equivalente a 20 mg de esomeprazol). Excipientes c.s.
PAMEZONE 40:
Cada CÁPSULA CON MICROGRÁNULOS GASTRORRESISTENTES contiene: Esomeprazol magnésico trihidrato 44,4 mg (equivalente a 40 mg de esomeprazol). Excipientes c.s.
LISTA DE EXCIPIENTES:
PAMEZONE 20: Sacarosa, manitol, hidroxipropilmetilcelulosa ftalato, fosfato sódico dibásico, alcohol cetílico, lauril sulfato de sodio.
PAMEZONE 40: Sacarosa, manitol, hidroxipropilmetilcelulosa ftalato, fosfato sódico dibásico, alcohol cetílico, lauril sulfato de sodio.
Para reportar reacciones adversas probables, por favor contacte a Laboratorios Roemmers S.A. Tlf: 462-1616 Anexo 252 o escríbanos a farmacovigilancia@pe.roemmers.com
Fabricado por Laboratorios Rowe S.R.L.
Santo Domingo, República Dominicana
Importado por:
LABORATORIOS ROEMMERS S.A.
Jr. Faustino Sánchez Carrión 425,
Magdalena del Mar. Telf.: 462-1616
Lima 17-Perú
CONSERVACIÓN DEL PRODUCTO:
Manténgase fuera del alcance de los niños.
Conservar a temperatura inferior a 30 ºC.
Mantener en su envase original hasta su utilización
No utilice si observa signos de deterioro del envase o del contenido del mismo.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que no necesita. De esta forma ayudará a proteger el medio ambiente.
INDICACIONES:
• PAMEZONE está indicado para el tratamiento de acidez estomacal y otros síntomas asociados con la enfermedad por reflujo gastroesofágico (ERGE).
• PAMEZONE está indicado para el tratamiento a corto plazo de esofagitis erosiva confirmada mediante diagnóstico (asociada con ERGE).
• PAMEZONE está indicado además para el tratamiento de mantenimiento de la resolución de los síntomas y cicatrización de esofagitis erosiva.
• PAMEZONE está indicado para reducir la ocurrencia de úlceras gástricas asociadas con la terapia continua con AINEs en pacientes con riesgo de desarrollarlas (pacientes de 60 años o más y / o antecedentes documentados de úlceras gástricas).
INDICACIONES TERAPÉUTICAS:
Tratamiento de la enfermedad de reflujo gastroesofágico (ERGE): Curación de la esofagitis erosiva: PAMEZONE está indicado en el tratamiento a corto plazo (4 a 8 semanas) para la curación y resolución sintomática de la esofagitis erosiva con diagnóstico confirmado. Para aquellos pacientes que no se han curado después de 4 a 8 semanas de tratamiento, un curso adicional de 4 a 8 semanas de PAMEZONE puede ser considerado.
Mantenimiento de la curación de la esofagitis erosiva: PAMEZONE está indicado para mantener la resolución de los síntomas y la curación de la esofagitis erosiva. Estudios controlados no se extienden más de 6 meses.
Enfermedad por Reflujo Gastroesofágico sintomático: PAMEZONE está indicado para el tratamiento a corto plazo (4 a 8 semanas) de la acidez y otros síntomas asociados con la ERGE en adultos y niños de 1 año o más.
Reducción del Riesgo de úlcera gástrica asociada a AINEs: PAMEZONE está indicado para la reducción de la aparición de úlceras gástricas asociadas a terapia continua con AINEs en pacientes con riesgo de desarrollar úlceras gástricas. Los pacientes se consideran en riesgo de acuerdo a su edad (≥60) y/o historia documentada de úlcera gástrica.
Los estudios controlados no se extienden más de 6 meses
Erradicación de H. pylori para reducir el riesgo de recurrencia de úlcera duodenal: Terapia triple (PAMEZONE más amoxicilina y claritromicina): PAMEZONE, en combinación con amoxicilina y claritromicina, está indicado para el tratamiento de pacientes con infección de H. pylori y úlcera duodenal (activa o con historia en los 5 años previos) para erradicar H. pylori. La erradicación de H. pylori ha demostrado que reduce el riesgo de recurrencia de úlcera duodenal [ver Posología y forma de administración].
En los pacientes que no responden al tratamiento, se deben realizar pruebas de sensibilidad. Si la resistencia a claritromicina es demostrada o la prueba de sensibilidad no es posible, se debe empezar terapia antimicrobiana alternativa [véase la información de prescripción para la claritromicina].
Condiciones de hipersecreción patológica incluyendo el síndrome de Zollinger-Ellison: PAMEZONE está indicado para el tratamiento a largo plazo de las condiciones de hipersecreción patológicas, incluyendo el síndrome de Zollinger-Ellison.
ACCIÓN FARMACOLÓGICA: Esomeprazol es un inhibidor de la bomba de protones que actúa suprimiendo la secreción de ácido gástrico mediante la inhibición específica de la hidrógeno-potasio ATPasa en la célula gástrica parietal. En el compartimento acídico de la célula parietal, los isómeros R y S son protonados y convertidos en el inhibidor activo, la sulfenamida aquiral. Al actuar específicamente sobre la bomba de protones, esomeprazol bloquea el paso final en la producción de ácido, reduciendo de esta forma la actividad gástrica. Este efecto está relacionado con una dosis diaria de hasta 20 a 40 mg y conlleva a la inhibición de secreción de ácido gástrico.
PROPIEDADES FARMACOLÓGICAS:
Propiedades farmacodinámicas:
Grupo farmacoterapéutico: Antiulcerosos. Inhibidores de la bomba de protones.
ATC: A02BC
Descripción: El ingrediente activo en el inhibidor de la bomba de protones PAMEZONE (magnesio esomeprazol) cápsulas con microgránulos gastrorresistentes para la administración oral es bis (5-metoxi-2 - [(S) - [(4-metoxi-3,5-dimetil-2-piridinil) metil] sulfinil] -1 H -benzoimidazol-1-il) magnesio trihidratado. El esomeprazol es el isómero S de omeprazol, que es una mezcla de los isómeros S y R-. (Aprobación inicial del magnesio esomeprazol en los EE.UU.: 2001). Su fórmula molecular es (C17H18N3O3S)2 Mg x 3H2O con peso molecular de 767.2 como trihidrato y 713.1 como una base anhidra. La fórmula estructural es:
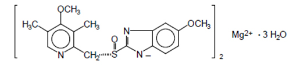
La sal de magnesio es un polvo cristalino blanco o ligeramente coloreado. Contiene 3 moles de agua de solvatación y es ligeramente soluble en agua. La estabilidad de magnesio esomeprazol tiene que ver con el pH; se degrada rápidamente en medios ácidos, pero tiene una estabilidad aceptable en condiciones alcalinas. A un pH 6,8 (tampón), la vida media de la sal de magnesio es de alrededor de 19 horas a 25 °C y aproximadamente 8 horas a 37 °C.
Mecanismo de acción: Esomeprazol es un inhibidor de la bomba de protones que suprime la secreción de ácido gástrico con la inhibición especifica de H+/K+-ATPasa en las células gástricas parietales. Los isómeros S- y R- del omeprazol son protonados y convertidos en el compartimiento ácido de las células parietales formando en inhibidor activo, la sulfenamida aquiral. Actuando específicamente sobre la bomba de protones, el esomeprazol bloquea el paso final en la producción del ácido, reduciendo la acidez gástrica. Este efecto es dependiente de la dosis, dosis diarias de hasta 20 a 40 mg inhibe la secreción de ácidos.
Actividad antisecretoria: El efecto de esomeprazol en el pH del intragástrico fue determinado en pacientes con enfermedad de reflujo gastroesofágico en dos estudios separados. En el primer estudio de 36 pacientes, esomeprazol cápsulas de 40 mg y 20 mg fueron administradas por cinco días. Los resultados se muestran en la tabla 1:
Tabla 1: Efecto sobre el pH intragástrico en el día 5 (N = 36)
|
Parámetro |
PAMEZONE 40 mg |
PAMEZONE 20 mg |
|
% tiempo gástrico |
70%* |
53% |
|
pH > 4† (horas) |
(16.8 h) |
(12.7 h) |
|
Coeficiente de variación |
26% |
37% |
|
Mediana del pH de 24 horas |
4.9* |
4.1 |
|
Coeficiente de variación |
16% |
27% |
|
† pH gástrico se midió durante un periodo de 24 horas * p< 0.01 PAMEZONE 40 mg vs PAMEZONE 20 mg |
||
En un segundo estudio, el efecto del pH intragástrico de esomeprazol 40 mg administrado uno diariamente por un periodo de cinco días similar al primer estudio, (% de tiempo con PH> 4 fue del 68% o 16.3 horas)
Efectos en la gastrina sérica: El efecto de esomeprazol sobre las concentraciones de gastrina en suero se evaluó en aproximadamente 2.700 pacientes en ensayos clínicos de hasta 8 semanas y en más de 1.300 pacientes para de 6-12 meses. El nivel medio de gastrina en ayunas aumento dependiendo de la dosis. Este incremento alcanzo una meseta en dos o tres meses de tratamiento y volvió a los niveles basales en cuatro semanas después de la interrupción del tratamiento.
El aumento de gastrina causa hiperplasia de células similares a Enterocromafines y el aumento de los niveles de Cromogranina A (CgA) en suero. El aumento de los niveles de CgA puede causar falsos positivos en los resultados en investigaciones del diagnóstico de tumores neuroendocrinos. Los proveedores de salud podrían interrumpir el tratamiento con esomeprazol por lo menos 14 días antes de evaluar los niveles de CgA y considerar repetir la prueba si los resultados iniciales son altos.
Efectos en células similares a Enterocromafines (ECL): En estudios de carcinogenicidad de 24 meses de omeprazol en ratas, a dosis significativas relacionadas con la ocurrencia de tumores gástricos carcinoides por células ECL la hiperplasia de células ECL fue observada tanto en machos como hembras [ver Datos de seguridad pre clínica]. Los tumores carcinoides también se han observado en ratas sometidas a fundectomia o tratamiento a largo plazo con otros inhibidores de protones o dosis altas de receptores antagonistas del H2.
Muestras de biopsias gástricas humanas se han obtenido a partir de más de 3.000 pacientes (tanto niños como adultos) tratados con omeprazol en los ensayos clínicos a largo plazo. La incidencia de hiperplasia de células ECL en estos estudios aumentó con el tiempo; sin embargo, no se encontró ningún caso de células carcinoides ECL, displasia o neoplasia en estos pacientes.
En más de 1000 pacientes tratados con esomeprazol (10, 20 o 40 mg/día) de 6 a 12 meses, la prevalencia de hiperplasia de células ECL se incrementó de acuerdo al tiempo y a las dosis. Ningún paciente desarrolló células carcinoides ECL, displasia o neoplasia en la mucosa gástrica.
Efectos endocrinos: Esomeprazol no tuvo ningún efecto en la función tiroidea cuando se administró vía oral a dosis de 20 o 40 mg por cuatro semanas. Otros efectos de esomeprazol en el sistema endocrino se evaluó utilizando estudios de omeprazol. El omeprazol que se administró vía oral en dosis de 30 o 40 mg durante 2 a 4 semanas no tuvo efecto sobre el metabolismo de los carbohidratos, los niveles circulantes de la hormona paratiroidea, cortisol, estradiol, testosterona, prolactina, colecistoquinina o secretina.
Propiedades farmacocinéticas:
Absorción: Esomeprazol cápsulas con microgránulos gastrorresistentes contienen una fórmula de gránulos con recubrimiento entérico bioequivalente al esomeprazol magnesio. La bioequivalencia se basa en un estudio de dosis única (40 mg) en 94 personas voluntarias entre hombres y mujeres sanos bajo condiciones de ayuno. Después de la administración oral el pico de niveles plasmáticos (Cmax) ocurre en aproximadamente 1.5 horas (Tmax). El Cmax se incrementa proporcionalmente cuando se aumenta la dosis y hay un aumento de tres veces el área bajo la curva de concentración de plasma-tiempo (AUC) de 20 a 40 mg. Al repetir la dosis diariamente una vez al día con 40 mg. La biodisponibilidad sistémica es aproximadamente 90% comparada con un 64% después de una sola dosis de 40 mg. La exposición media (AUC) al esomeprazol se incrementa de 4.32 µmol*hr/L en el día 1 a 11.2 µmol*hr/L en el día 5 después de una dosificación diaria de 40 mg.
El AUC después de la administración de la dosis única de 40 mg de esomeprazol se reduce de un 53% a un 43% después de ingerir comidas comparadas con las condiciones de ayuno. Esomeprazol debe administrarse al menos una hora antes de las comidas.
El perfil farmacocinético de esomeprazol estuvo determinado en 36 pacientes con la enfermedad de reflujo gastroesofágico sintomático, por un periodo de cinco días se les administró una vez al día capsulas de esomeprazol de 20 y 40 mg. Los resultados se muestran en la Tabla 2:
Tabla 2: Parámetros farmacocinéticos de esomeprazol en el día 5, después de la dosificación oral durante 5 días
|
Parámetro* (CV) |
PAMEZONE 40 mg |
PAMEZONE 20 mg |
|
AUC (µmol.h/L) |
12.6 (42%) |
4.2 (59%) |
|
Cmax (µmol/L) |
4.7 (37%) |
2.1 (45%) |
|
Tmax (h) |
1.6 |
1.6 |
|
t1/2 (h) |
1.5 |
1.2 |
|
*Los valores representan la media geométrica, excepto la Tmax, que es la media aritmética; CV = coeficiente de variación |
||
Distribución: Esomeprazol se liga al 97% de las proteínas plasmáticas. Las proteínas plasmáticas ligadas son constantes sobre la rango de 2 a 20 µmol/L. el volumen de distribución aparente en estado estacionario en los voluntarios sanos es aproximadamente 16 L.
Metabolismo: El esomeprazol es principalmente metabolizado en el hígado por la enzima del citocromo P450 (CYP). Los metabolitos de esomeprazol carecen de actividad antisecretora. La mayor parte del metabolismo del esomeprazol depende de la isoenzima CYP2C19, la cual forma los metabolitos hidroxi y dimetil. La cantidad restante depende de la CYP3A4 el cual forma el metabolito sulfona. La isoenzima CYP2C19 exhibe un polimorfismo en el metabolismo de esomeprazol, desde un 3% en los caucásicos y el 15- 20% de asiáticos carecen de CYP2C19 y son denominados metabolizadores pobres. En estado estacionario, el radio de AUC en los metabolizadores pobres al AUC en el resto de la población (metabolizadores) es aproximadamente 2.
Siguiendo la administración de dosis equimolares, los isómeros S- y R- son metabolizados en diferentes formas por el hígado, resultando en un incremento de los S- isómeros más que los R- isómeros.
Excreción: La semivida plasmática del esomeprazol es aproximadamente 1 a 1.5 horas. Menos del 1% del fármaco original se excreta en la orina. Aproximadamente el 80% de una dosis oral de esomeprazol se excreta en forma de metabolitos inactivos en la orina, y el resto se encuentra como metabolitos inactivos en las heces.
Farmacocinética: Terapia combinatoria con antimicrobianos.
Esomeprazol magnesio 40 mg una vez al día se administró en combinación con claritromicina 500 mg dos veces al día y amoxicilina 1000 mg dos veces al día durante 7 días a 17 hombres y mujeres sanos. El estado estacionario AUC y Cmax de esomeprazol aumentado en un 70% y 18%, respectivamente, durante la terapia de combinación triple en comparación con el tratamiento con esomeprazol solo. El aumento observado en la exposición esomeprazol durante la coadministración con claritromicina y amoxicilina no produce preocupaciones significantes de seguridad.
Los parámetros farmacocinéticos para claritromicina y amoxicilina fueron similares durante la triple terapia de combinación y la administración de cada uno de estos fármacos de forma individual. Sin embargo, la media de AUC y Cmax para la14-hidroxiclaritromicina se incrementa en un 19% y 22%, respectivamente, durante la triple terapia de combinación en comparación con el tratamiento de claritromicina sola. . Este aumento de la exposición a 14-hidroxiclaritromicina no se considera clínicamente significativa.
Uso concomitante de clopidogrel: Resultados de un estudio cruzado en sujetos sanos mostró una interacción farmacocinética entre clopidogrel (dosis de 300 mg/75 mg mantenida diariamente) y esomeprazol (40 mg por vía oral una vez al día) cuando se administra conjuntamente durante 30 días. La exposición al metabolito activo de clopidogrel se redujo en un 35% a 40% durante este período de tiempo. Los parámetros farmacodinámicos también miden y demuestran un cambio en la inhibición de la agregación plaquetaria, relacionada con el metabolito activo del clopidogrel.
Uso concomitante de micofenolato mofetil: La administración con el omeprazol de 20 mg dos veces al día por 4 días y una sola dosis de MMF aproximadamente una hora después de la última dosis de omeprazol en doce sujetos sanos en un estudio cruzado resultando en una reducción del 52% en el Cmax y una reducción del 23% en el AUC de MPA
Poblaciones especiales:
Geriátricos: Los valores del AUC y Cmax en estado de equilibrio fueron ligeramente altos (25% y 18%, respectivamente) en ancianos comparados con sujetos jóvenes sanos. El ajuste de dosis basado en la edad no es necesario
Pediátricos - 1 a 11 años de edad: La farmacocinética de esomeprazol se ha estudiado en pacientes pediátricos con ERGE con edades comprendidas entre 1 a 11 años. Siguiendo la dosis de una vez al día durante 5 días, la exposición total (AUC) para la dosis de 10 mg en pacientes de 6 a 11 años fue similar a la observada con la dosis de 20 mg en adultos y adolescentes de 12 a 17 años. La exposición total a la dosis de 10 mg en pacientes de 1 a 5 años fue de aproximadamente 30% mayor que la dosis de 10 mg en pacientes de edades comprendidas entre 6 y 11 años. La exposición total para la dosis de 20 mg en pacientes de entre 6 y 11 años fue mayor a la observada con la dosis de 20 mg en pacientes de 12 a 17 años de edad y adultos, pero menor que la observada con la dosis de 40 mg en pacientes de 12 a 17 años de edad y adultos. Ver Tabla 3.
Tabla 3: Resumen de los parámetros farmacocinéticos en pacientes de 1 a 11 años de edad con ERGE, después de un tratamiento de 5 días con esomeprazol oral una vez al día.
|
Parámetro |
1 a 5 años |
6 a 11 años |
|
|
10 mg (N=8) |
10 mg (N=7) |
20 mg (N=6) |
|
|
AUC (µmol.h/L)* |
4.83 |
3.70 |
6.28 |
|
Cmax (µmol/L)* |
2.98 |
1.77 |
3.73 |
|
tmax (h)† |
1.44 |
1.79 |
1.75 |
|
t 1/2lz (h)* |
0.74 |
0.88 |
0.73 |
|
Cl/F (L/h)* |
5.99 |
7.84 |
9.22 |
|
*media geométrica, †media aritmética |
|||
Pediátrico - De 12 a 17 años de edad: La farmacocinética de esomeprazol fue estudiada en 28 pacientes adolescentes con ERGE de 12 a 17 años, de un mismo centro de estudios. Los pacientes fueron aleatorizados para recibir esomeprazol de 20 mg o 40 mg una vez al día durante 8 días. Los valores medios de Cmax y los valores del AUC del omeprazol no se vieron afectados por el peso corporal o la edad; y se observó un incremento medio en los valores de Cmax y AUC de acuerdo a la proporción de las dosis entre los dos grupos de estudio. En general la farmacocinética de esomeprazol en pacientes adolescentes de 12 a 17 años es similar a la observada en pacientes adultos con ERGE. Ver tabla 4.
Tabla 4: Comparación de los parámetros farmacocinéticos en pacientes de 12 a 17 años de edad con ERGE y adultos con ERGE sintomática, tras administración de dosis repetidas diarias de esomeprazol* vía oral.
|
12 a 17 años (N=28) |
Adultos (N=36) |
|||
|
20 mg |
40 mg |
20 mg |
40 mg |
|
|
AUC (µmol*h/L) |
3.65 |
13.86 |
4.2 |
12.6 |
|
Cmax (µmol/L) |
1.45 |
5.13 |
2.1 |
4.7 |
|
tmax (h) |
2.00 |
1.75 |
1.6 |
1.6 |
|
t 1/2?z (h) |
0.82 |
1.22 |
1.2 |
1.5 |
|
Los datos presentados son medias geométricas para el AUC, Cmax y t1/2?z y mediana para el valor de tmax. *La duración del tratamiento en los pacientes de 12 a 17 años de edad y adultos, fueron de 8 días y 5 días, respectivamente. Los datos se obtuvieron a partir de dos estudios independientes. |
||||
Género: Los valores de AUC y Cmax fueron ligeramente más altos (13%) en mujeres que en varones en el estado estable. No es necesario el ajuste de dosis de acuerdo al sexo.
Insuficiencia hepática: La farmacocinética en equilibrio del esomeprazol fue obtenida después de la administración de 40 mg, una vez al día a 4 pacientes con leve (Child-Pugh A), moderada (Child-Pugh B) y severa (Child-Pugh C) insuficiencia hepática se compararon con los obtenidos en 36 varones y mujeres con ERGE con función hepática normal. En pacientes con leve a moderada insuficiencia hepática, las AUCs estuvieron dentro del rango esperado en pacientes con función hepática normal. En pacientes con insuficiencia hepática severa los AUCs fueron 2 a 3 veces mayor que en los pacientes con función hepática normal. No se recomienda un ajuste de dosis para pacientes con insuficiencia hepática leve a moderada (Child-Pugh A y B). Sin embargo, en pacientes con insuficiencia hepática severa (Child-Pugh C) no se debe exceder una dosis de 20 mg al día [ver Posología y Forma de administración].
Insuficiencia renal: No se espera que la farmacocinética de PAMEZONE se vea alterada en pacientes con daño renal respecto a voluntarios sanos, menos del 1% de esomeprazol es excretada sin cambios en la orina.
Otras observaciones farmacocinéticas: La coadministración con anticonceptivos, diazepam, fenitoína o quinidina no parecen alterar el perfil farmacocinético del omeprazol.
Estudios evalúan el uso concomitante de esomeprazol con naproxeno (AINE no selectivo) o rofecoxib (AINE COX-2 selectivo) no se identificó ningún cambio relevante en el perfil farmacocinético del esomeprazol con estos AINES.
CONTRAINDICACIONES:
PAMEZONE está contraindicado en pacientes con hipersensibilidad conocida a sustitutos benzoimidazólicos o a algún componente de la fórmula. Las reacciones de hipersensibilidad pueden incluir anafilaxis, shock anafiláctico, angioedema, broncoespasmo, nefritis aguda intersticial, y urticaria [véase Reacciones adversas].
Para obtener información acerca de contraindicaciones de los agentes antibacterianos (claritromicina y amoxicilina) indicados en combinación con PAMEZONE, ver la sección de Contraindicaciones en cada uno de sus insertos.
REACCIONES ADVERSAS:
Experiencia en ensayos clínicos: Dado que los ensayos clínicos se realizaron en condiciones muy variables, la tasa de reacciones adversas que se han observado en los ensayos clínicos de un fármaco no pueden compararse directamente con la tasa encontrada en los ensayos clínicos de otro fármaco y puede no reflejar la tasa observadas en la práctica.
Adultos: La seguridad de esomeprazol se evaluó en más de 15.000 pacientes (de 18 a 84 años) en ensayos clínicos en todo el mundo, incluyendo más de 8.500 pacientes en los Estados Unidos y más de 6.500 pacientes en Europa y Canadá. Más de 2.900 pacientes fueron tratados en estudios a largo plazo de 6-12 meses. En general, esomeprazol fue bien tolerado tanto a corto como a largo plazo en los ensayos clínicos.
La seguridad en el tratamiento de la esofagitis erosiva se evaluó en cuatro ensayos clínicos comparativos aleatorizados, los cuales incluyeron 1.240 pacientes tratados diariamente con esomeprazol 20 mg, 2.434 pacientes con esomeprazol 40 mg, y 3.008 pacientes en omeprazol 20 mg al día. La reacción adversa más frecuente (≥1%) en los tres grupos fueron dolor de cabeza (5.5, 5 y 3.8, respectivamente) y diarrea (no hay diferencia entre los tres grupos). Náuseas, flatulencia, dolor abdominal, estreñimiento, y sequedad de boca ocurrieron con una frecuencia similar entre los pacientes que toman esomeprazol u omeprazol.
Adicionalmente se reportaron reacciones adversas posible o probablemente relacionadas con esomeprazol con una incidencia <1% listadas como sigue por sistema:
• El cuerpo como un todo: distensión abdominal, reacciones alérgicas, astenia, dolor de espalda, dolor en el pecho, dolor subesternal en el pecho, edema facial, edema periférico, bochornos, fatiga, fiebre similar a la gripe, edema generalizado, edema de las piernas, malestar general, dolor, rigidez;
• Cardiovascular: sofocos, hipertensión, taquicardia;
• Endocrino: bocio;
• Gastrointestinales: irregularidad intestinal, estreñimiento agravado, dispepsia, disfagia, displasia GI, dolor epigástrico, eructos, trastornos del esófago, deposiciones frecuentes, gastroenteritis, hemorragia GI, los síntomas gastrointestinales no se especifique de otro modo, hipo, melena, trastorno de la boca, la faringe, trastorno rectal, gastrina sérica aumentada, trastornos de la lengua, edema de lengua, Estomatitis ulcerativa, vómitos;
• Audición: dolor de oído, zumbido de oídos;
• Hematológicas: anemia, anemia hipocrómica, adenopatías cervicales, epistaxis, leucocitosis, leucopenia, trombocitopenia;
• Hepática: bilirrubinemia, función hepática anormal, TGO aumentado, TGP aumentado;
• Metabólicos/nutricionales: glucosuria, hiperuricemia, hiponatremia, incremento de la fosfatasa alcalina, sed, la deficiencia de vitamina B12, aumento de peso, disminución del peso;
• Músculo esquelético: artralgia, artritis agravada, artropatía, calambres, fibromialgia, hernia, polimialgia reumática;
• Sistema nervioso/psiquiátrico: anorexia, apatía, aumento del apetito, confusión, depresión agravada, mareos, hipertonía, nerviosismo, hipoestesia, impotencia, insomnio, migraña, migraña agravada, parestesia, trastorno del sueño, somnolencia, temblores, vértigo, defecto en el campo visual
• Reproductiva: dismenorrea, trastornos menstruales, vaginitis;
• Respiratorio: asma agravada, tos, disnea, edema de laringe, faringitis, rinitis, sinusitis;
• Piel y apéndices: acné, angioedema, dermatitis, prurito, prurito anal, erupción cutánea, erupción eritematosa, erupción maculopapular, inflamación de la piel, aumento de la sudoración, urticaria;
• Órganos de los sentidos: otitis media, parosmia, pérdida del gusto, alteración del gusto;
• Urogenital: anormal de la orina, la albuminuria, cistitis, disuria, infección fúngica, hematuria, la frecuencia de la micción, moniliasis, candidiasis genital, poliuria;
• Visual: conjuntivitis, trastornos de la visión.
Los siguientes cambios potenciales clínicamente significativos hallados en ensayos clínicos independientemente de la relación con esomeprazol, fueron reportados en ≤ 1% de los pacientes y son: incremento de la creatinina, ácido úrico, bilirrubina total, fosfatasa alcalina, TGA, AST, hemoglobina, recuento de glóbulos blancos de la sangre, plaquetas, gastrina sérica, potasio, sodio, tiroxina y tiroides, hormona estimulante [ver Propiedades farmacológicas]. Se observaron disminuciones en la hemoglobina, en el recuento de glóbulos blancos, en las plaquetas, en el potasio, en el sodio, y en la tiroxina.
Los hallazgos endoscópicos que fueron reportados como reacciones adversas incluyen: duodenitis, esofagitis, estenosis esofágica, úlcera esofágica, varices esofágicas, úlcera gástrica, gastritis, hernia, pólipos benignos o nódulos, esófago de Barrett, y la decoloración de la mucosa.
La incidencia de reacciones adversas relacionadas con el tratamiento durante 6 meses fue similar a placebo. No hubo diferencias en el tipo de reacciones adversas relacionadas con el mantenimiento del tratamiento hasta 12 meses en comparación con el tratamiento a corto plazo.
Se realizaron dos estudios controlados con placebo en 710 pacientes para el tratamiento de la enfermedad por reflujo gastroesofágico sintomática. Las reacciones adversas más frecuentes que eran reportadas como posible o probablemente relacionadas con esomeprazol fueron diarrea (4,3%), cefalea (3,8%), y dolor abdominal (3,8%).
Pediatría: La seguridad de PAMEZONE se evaluó en 316 pacientes pediátricos y adolescentes de edades comprendidas del 1 a 17 años en cuatro ensayos clínicos para el tratamiento de la ERGE sintomática. En 109 pacientes pediátricos de 1 a 11 años, la reacción más frecuentemente notificada (al menos 1%) en relación al tratamiento fueron la diarrea (2,8%), cefalea (1,9%) y somnolencia (1,9%). En 149 pacientes pediátricos de 12 a 17 años, la mayor frecuencia de reacciones adversas (al menos 2%) relacionadas con el tratamiento en estos pacientes fueron dolor de cabeza (8,1%), dolor abdominal (2,7%), diarrea (2%), y náuseas (2%).
La seguridad de esomeprazol se evaluó en 167 pacientes pediátricos desde el nacimiento hasta <1 año de edad en tres ensayos clínicos. En un estudio que incluyó a 26 pacientes pediátricos de 1 mes de nacimiento no hubo reacciones adversas relacionadas con el tratamiento. En un estudio que incluyó 43 pacientes pediátricos de edad 1 a 11 meses, las reacciones adversas más frecuentes (por lo menos el 5%), independientemente de las causas, fueron irritabilidad y vómitos. En un estudio que incluyó 98 pacientes pediátricos, 1 a 11 meses de edad ,expuestos a esomeprazol hasta por 6 semanas (incluyendo 39 pacientes asignados al azar a la fase de abstinencia), habían 4 reacciones adversas relacionadas con el tratamiento: dolor abdominal (1%), regurgitación (1%), taquipnea (1%), y aumento de TGA (1%).
No han sido identificados nuevos problemas de seguridad en pacientes pediátricos
Tratamiento combinado con amoxicilina y claritromicina: En ensayos clínicos usando la terapia que combina PAMEZONE con amoxicilina y claritromicina, no se observaron reacciones adversas adicionales a la combinación específica de estos fármacos. Las reacciones adversas que ocurrieron fueron limitadas cuando se usando PAMEZONE, amoxicilina y claritromicina de forma individual.
La reacción adversa más reportada con relación a la combinación de los tres fármacos en pacientes por diez días fueron diarrea (9.2%), alteración del gusto (6,6%), y dolor abdominal (3,7%). No se observaron tasas más altas de reacciones adversas derivadas del tratamiento de la triple terapia que de las que se observaron con PAMEZONE solo.
Para obtener más información sobre las reacciones adversas de amoxicilina o claritromicina, consulte los prospectos individuales de cada fármaco, en la sección de reacciones adversas
En ensayos clínicos utilizando la terapia que combina PAMEZONE con amoxicilina y claritromicina, no se encontraron anomalías de laboratorio particulares adicionales con la combinación
Para obtener más información sobre los cambios de laboratorio con amoxicilina o claritromicina, consulte a sus prospectos, en la sección de Reacciones adversas.
Experiencia post comercialización: Las siguientes reacciones adversas han sido identificadas durante el uso después de la aprobación de PAMEZONE
Debido a que estas reacciones se informaron voluntariamente por una población de tamaño incierto, no es posible estimar de forma fiable la frecuencia o establecer una relación causal de la exposición al fármaco. Estos informes se enumeran por sistema corporal:
• Sanguínea y linfática: agranulocitosis, pancitopenia;
• Ojo: visión borrosa;
• Gastrointestinales: pancreatitis; estomatitis; colitis microscópica
• Hepatobiliar: insuficiencia hepática, hepatitis con o sin ictericia;
• Sistema inmunológico: reacción anafiláctica/shock;
• Infecciones e infestaciones: candidiasis gastrointestinal; diarrea asociada a Clostridium difficile;
• Trastornos del metabolismo y nutricionales: hipomagnesemia, con o sin hipocalcemia y/o hipopotasemia
• Trastornos musculo esqueléticos y del tejido conjuntivo: debilidad muscular, mialgia, fractura ósea;
• Sistema nervioso: encefalopatía hepática, alteración del gusto;
• Psiquiatría: agresión, agitación, depresión, alucinaciones;
• Urinario y renal: nefritis intersticial;
• Sistema reproductor y de mama: ginecomastia;
• Respiratorios, torácicos y mediastínicos: broncoespasmo;
• Piel y del tejido subcutáneo: alopecia, eritema multiforme, hiperhidrosis, fotosensibilidad, síndrome de Stevens-Johnson, necrólisis tóxica epidérmica (algunos mortales).
Comunicar a su médico o farmacéutico cualquier reacción adversa que no estuviese descrita en el inserto
INCOMPATIBILIDADES: No se han reportado.
INTERACCIONES CON OTROS MEDICAMENTOS:
Por inhibir la secreción de ácido gástrico, PAMEZONE tiene el potencial de afectar la biodisponibilidad de cualquier medicamento cuya absorción sea dependiente del pH.
Estudios in vitro e in vivo han mostrado que no es probable que esomeprazol inhiba las CYPs 1A2, 2A6, 2C9, 2D6, 2E1 y 3A4. No se espera que se presenten interacciones clínicamente relevantes con medicamentos metabolizados por estas enzimas.
Estudios de interacción entre medicamentos han mostrado que esomeprazol no presenta interacciones clínicamente significativas con fenitoína, warfarina, quinidina, claritromicina, o amoxicilina.
Esomeprazol puede interferir potencialmente con su enzima metabolizante principal, la CYP2C19.
La coadministración de 30 mg de esomeprazol y diazepam, un sustrato de la CYP2C19, resultó en una disminución del 45% en el aclaramiento de diazepam. Los niveles plasmáticos incrementados de diazepam se observaron a partir de las 12 horas de ser administrado. Debido a que los niveles plasmáticos de diazepam en ese momento fueron menores al intervalo terapéutico, es poco probable que esta interacción se considere clínicamente significativa.
Amoxicilina o claritromicina: El uso concomitante con esomeprazol puede resultar en niveles plasmáticos incrementados de esomeprazol y 14-hidroxiclaritromicina.
Ketoconazol, sales de hierro o digoxina: Esomeprazol puede interferir con la absorción de estos agentes ya que incrementa el pH gastrointestinal.
Warfarina: Informes poscomercialización han indicado cambios en los valores de protrombina con la terapia concomitante. Se debe monitorizar los incrementos en los valores del INR y el tiempo de protrombina con el uso concomitante ya que estos incrementos pueden conducir a sangrado anormal e incluso producir la muerte.
INTERACCIONES MEDICAMENTOSAS:
Interferencia con la terapia antirretroviral: El uso concomitante de atazanavir y nelfinavir con inhibidores de la bomba de protones no se recomienda. La coadministración de atazanavir con el inhibidor de la bomba de protones derivará en la disminución de atazanavir en las concentraciones plasmáticas y eso puede resultar en una pérdida del efecto terapéutico y el desarrollo de resistencia al fármaco. La coadministración de saquinavir con el inhibidor de la bomba de protones se espera derive en un incremento de las concentraciones de saquinavir, lo cual puede incrementar la toxicidad y requerir la disminución de la dosis.
El omeprazol, del cual el esomeprazol es un enantiómero, ha sido reportado debido a la interacción con algunos medicamentes antirretrovirales. La importancia clínica y los mecanismos detrás de estas interacciones no siempre se conocen. El aumento de pH gástrico durante el tratamiento omeprazol puede cambiar la absorción del fármaco antirretroviral. Otros posibles mecanismos de interacción son a través de la vía CYP2C19.
Reducción de las concentraciones de atazanavir y nelfinavir: Para algunos medicamentos antirretrovirales, como atazanavir y nelfinavir, los niveles séricos disminuidos han sido reportados cuando se administra de forma conjunta con el omeprazol. Después de varias dosis de nelfinavir (1250 mg, dos veces al día) y omeprazol (40 mg diarios), el AUC se redujo en un 36% y un 92% Cmax por 37% y 89% y Cmin por 39% y 75% respectivamente para nelfinavir y M8. Después de múltiples dosis de atazanavir (400 mg, al día) y omeprazol (40 mg, al día, 2 horas. antes de atazanavir), el AUC se redujo en un 94%, Cmax en un 96%, y Cmin por 95%.
La administración concomitante con omeprazol y medicamentos tales como atazanavir y nelfinavir; por lo tanto, no se recomienda.
Aumento de las concentraciones de saquinavir: Para otros fármacos antirretrovirales, tales como saquinavir, se ha informado de niveles séricos elevados, con un aumento del AUC en un 82%, en Cmax por 75%, y en Cmin en un 106%, a raíz de múltiples dosis de saquinavir/ritonavir (1000/100 mg) dos veces al día durante 15 días con omeprazol 40 mg coadministrados diariamente por 11 a 15 días. Por lo tanto, la monitorización, clínica y de laboratorio para toxicidad de saquinavir se recomienda durante el uso concurrente con PAMEZONE. La reducción de la dosis de saquinavir se debe considerar por la seguridad de los pacientes.
También hay algunos medicamentos antirretrovirales en los cuales no han sido reportados cambios en los niveles séricos cuando se administran con omeprazol
Medicamentos a los cuales el pH gástrico puede afectar la biodisponibilidad: Debido a los efectos en la secreción de ácido gástrico, esomeprazol puede reducir la absorción de algunos fármacos para los cuales el pH gástrico determina su biodisponibilidad. Así como otros fármacos que disminuyen la acidez intragástrica, la absorción de fármacos como ketoconazol, atazanavir, sales de hierro, erlotinib, y micofenolato mofetil (MMF) puede disminuir, mientras que la absorción de fármacos como digoxina puede aumentar durante el tratamiento con esomeprazol.
Esomeprazol es un enantiómero del omeprazol. El tratamiento concomitante con omeprazol (20 mg diariamente) y digoxina en sujetos sanos aumentó la biodisponibilidad de la digoxina en un 10% (30% en dos sujetos).En la coadministración de digoxina con PAMEZONE se espera un aumento de la exposición sistémica de la digoxina. Por lo tanto, los pacientes pueden necesitar ser monitorizados cuando se usa digoxina en forma concomitante con PAMEZONE
La coadministración de omeprazol en sujetos sanos y en pacientes trasplantados que están recibiendo MMF ha sido reportada para reducir la exposición al metabolito activo, el ácido micofenólico (AMF), posiblemente debido a una disminución en la solubilidad del MMF ante el incremento del PH gástrico. La relevancia clínica de reducir la exposición de AMF en el rechazo de órganos no ha sido establecida en pacientes trasplantados que reciben PAMEZONE y MMF. Usar PAMEZONE con cuidado en pacientes trasplantados que reciben MMF [ver Propiedades farmacológicas - Farmacocinética].
Efectos sobre el metabolismo hepático/vías del citocromo P-450: Esomeprazol es mayormente metabolizado en el hígado por CYP2C19 and CYP3A4. Estudios In vivo e In vitro han mostrado que el esomeprazol no es como un inhibidor de CYPs 1A2, 2A6, 2C9, 2D6, 2E1, y 3A4. No existen interacciones relevantes con los fármacos metabolizados por estos CYPs. Estudios de interacciones farmacológicas muestran que el omeprazol no tiene ninguna interacción clínica significante con fenitoína, warfarina, quinidina, claritromicina o amoxicilina
Sin embargo, se han recibido reportes post comercialización de cambios en las medidas de protrombina en pacientes que usan en forma concomitante warfarina y esomeprazol. Los aumentos en INR y tiempo de protrombina pueden llevar a un sangrado anormal e incluso la muerte. Los pacientes tratados con un inhibidor de la bomba de protones y warfarina en forma concomitante pueden necesitar un control para los incrementos de INR y tiempo de protrombina.
Esomeprazol puede interferir con el CYP2C19, la enzima con mayor metabolismo del esomeprazol. La coadministración de esomeprazol 30 mg y diazepam al sustrato CYP2C19, resulta en una disminución del 45% de la depuración del diazepam.
Clopidogrel: El Clopidogrel es metabolizado en su metabolito activo en parte por CYP2C19. El uso concomitante de esomeprazol de 40 mg resulta en una reducción del metabolito activo del clopidogrel en los niveles de plasma y una reducción en la inhibición plaquetaria. Evitar el uso concomitante de PAMEZONE con clopidogrel. Si usa PAMEZONE, considere el uso de una terapia alternativa anti plaquetaria [ver Propiedades farmacológicas - Farmacocinética].
El omeprazol actúa como un inhibidor de la CYP2C19. El omeprazol, administrado en dosis de 40 mg al día durante 1- 20 semanas a sujetos sanos en un estudio cruzado, aumentó el Cmax y AUC del cilostazol a un 18% y 26% respectivamente. Cmax y AUC de uno de los metabolitos activos, 3,4-dihidrocilostazol, el cual tiene 4-7 veces la actividad de cilostazol, se incrementó en un 29% y 69% respectivamente. En la coadministración de cilostazol con esomeprazol se espera el incremento de las concentraciones de cilostazol y su metabolito activo mencionado anteriormente. Por lo tanto una reducción de dosis de 100 mg a dos de 50 mg, dos veces al día debe ser considerada.
La administración concomitante de esomeprazol y un inhibidor combinado de CYP2C19 y CYP3A4, como voriconazol, puede resultar en una doble exposición de esomeprazol. Normalmente no es necesario ajustar la dosis de esomeprazol. Sin embargo, en pacientes con el síndrome de Zollinger-Ellison, que pueden requerir dosis más altas de hasta 240 mg/día, el ajuste de dosis puede ser considerado.
Los fármacos que se sabe que inducen CYP2C19 o CYP3A4 o ambos (como rifampicina) pueden dar lugar a disminución de los niveles séricos de esomeprazol. El omeprazol, del cual el esomeprazol es un enantiómero, se ha reportado que interactúa con la yerba de San Juan, un inductor de CYP3A4 en un estudio cruzado en 12 sujetos sanos, la yerba de San Juan (300 mg tres veces al día por 14 días) disminuye significativamente la exposición al esomeprazol en metabolizadores lentos de CYP2C19 (disminución de Cmax y AUC en 37.5% y 37.9%, respectivamente). Evitar el uso concomitante de la yerba de San Juan o rifampicina con PAMEZONE
Interacciones con investigaciones en tumores neuroendocrinos: La disminución del ácido gástrico inducida por fármacos resulta en una hiperplasia de células similares a los enterocromafines e incrementa los niveles de Cromogranina A, los cuales intervienen en las investigaciones para tumores neuroendocrinos [ver Advertencias, y Propiedades Farmacológicas - Farmacodinámica].
Tacrolimus: Administración concomitante de esomeprazol y tacrolimus puede incrementar los niveles séricos de tacrolimus.
Terapia combinada con claritromicina: La coadministración de esomeprazol, claritromicina y amoxicilina resulta en un incremento en las concentraciones plasmáticas de esomeprazol y 14- hidroxiclaritromicina.
La administración concomitante de la claritromicina con otros fármacos puede ocasionar reacciones adversas severas debido a la interacción con fármacos [ver Advertencias en la información de prescripción para claritromicina]. Debido a estas interacciones farmacológicas, claritromicina está contraindicada para la coadministración con fármacos determinados [ver Contraindicaciones en la información de prescripción para claritromicina].
Metrotexato: Los reportes de casos publicados en estudios farmacocinéticas en la población, y análisis retrospectivos sugieren que la administración concomitante de IBPs y metotrexato (principalmente en altas dosis; ver la información de prescripción para el metotrexato) se pueden elevar y prolongar los niveles séricos de metotrexato y/o su metabolito activo hidrometotrexato. Sin embargo, no existen estudios formales de metotrexato e IBPs [ver Advertencias].
DATOS DE SEGURIDAD PRECLÍNICA:
Carcinogénesis, mutagénesis, problemas de fertilidad: El carcinogénesis potencial de PAMEZONE fue evaluado usando estudios de omeprazol, del cual el esomeprazol es un enantiómero. En estudios de carcinogenicidad oral en ratas DE 2 a 24 meses, omeprazol a dosis diarias de 1.7, 3.4, 13.8, 44 y de 149.8 mg/kg/día (alrededor de 0.4 a 34 veces las dosis humanas de 40 mg/día basados en el área de superficie corporal) produjo células gástricas carcinoides ECL relacionadas a la dosis en ambos sexos de las ratas; la incidencia de este efecto fue más marcado en las ratas hembras, las cuales presentaban un nivel elevado de esomeprazol en sangre. Los carcinomas gástricos no ocurrieron en las ratas no tratadas. Adicionalmente, la hiperplasia de las células ECL se presentó en todos los grupos tratados en ambos sexos. En uno de estos estudios, las ratas hembra se trataron con 13, 8 mg de omeprazol/kg/día (alrededor de 3 a 4 veces la dosis humana de 40 mg/día de acuerdo a la superficie corporal) por un año, después por un año adicional sin el fármaco. No se observaron carcinoides en estas ratas. Una incidencia incrementada en el tratamiento relacionado a la hiperplasia de células ECL fue observada al término del primer año (94% tratadas vs 10% control) en el segundo año la diferencia entre las ratas tratadas y las control fue menor (46% vs 26%) pero se seguía observando más hiperplasia en el grupo tratado. Adenocarcinoma gástrico fue visto en una rata (2%). No se observaron tumores similares en las ratas hembras o machos tratados por dos años. Para esta cepa de ratas ningún tumor similar ha sido observado en la historia, pero el encuentro de solo un tumor es difícil de interpretar. Un estudio de 78 semanas de carcinogenicidad en ratones no mostró una ocurrencia incrementada del tumor, pero el estudio no fue concluyente.
Esomeprazol resultó negativa en el ensayo de mutaciones Ames, en el ensayo in vivo de aberraciones cromosómicas de las células de la médula ósea de ratas y en el ensayo in vivo del de micronúcleos del ratón. Sin embargo, el esomeprazol fue positivo en el ensayo in vitro de aberraciones cromosómicas de linfocitos humanos. Omeprazol fue positivo en el ensayo in vitro de aberraciones cromosómicas en linfocitos humanos, en el ensayo in vivo de los cromosomas de las células de la médula ósea, y en el ensayo in vivo de micronúcleos en el ratón.
Se evaluaron los efectos potenciales del esomeprazol sobre la fertilidad y el rendimiento reproductivo utilizando estudios de omeprazol. Omeprazol a dosis orales de hasta 138 mg/kg/día en ratas (aproximadamente el 34 veces la dosis humana de 40 mg/día en base al área de la superficie corporal) no tuvo ningún efecto sobre el comportamiento reproductivo de los animales.
Toxicología y/o farmacología animal:
• Estudios reproductivos: Los estudios reproductivos se realizaron en ratas a dosis orales de hasta 280 mg/kg/día (alrededor de 68 veces la dosis oral humana de 40 mg en base a la superficie corporal) y en conejos en dosis orales de 86 mg/kg/día (alrededor de 42 veces la dosis oral humana de 40 mg de acuerdo al área de la superficie corporal) y no se evidenciaron alteraciones en la fertilidad o desarrollo del feto debido al esomeprazol. [Ver Embarazo – Datos en animales].
• Estudio en animales jóvenes: Un estudio de toxicidad de 28 días con una fase de recuperación de 14 días fue conducido en ratas juveniles con esomeprazol magnesio a dosis de 70 a 280 mg/kg/día (alrededor de 17 a 68 veces la dosis diaria de 40 mg en el ser humano basada en el área de superficie corporal). Un incremento en el número de muertes a la mayor dosis de 280 mg/kg/día fue observada cuando se les administró a las ratas juveniles esomeprazol magnesio desde el día 7 al 35 después de nacidos. Adicionalmente, dosis iguales o mayores de 140 mg/kg/día (alrededor de 34 veces la dosis humana de 40 mg basado en el área de superficie corporal), producía reducciones en el peso relacionadas al tratamiento (aproximadamente el 14%) y el la ganancia de peso, disminución del peso del fémur y la longitud del fémur, y afectaba en general, el crecimiento. Resultados comparables descritos anteriormente se observaron también en estudios con otra sal de esomeprazol, esomeprazol estroncio, a dosis equimolares de esomeprazol.
ADVERTENCIAS:
Concurrencia de malignidad gástrica: La respuesta sintomática a la terapia con PAMEZONE no excluye la presencia de malignidad gástrica.
Gastritis atrófica: La gastritis atrófica ha sido ocasionalmente vista en la biopsia gástrica de pacientes tratados a largo plazo con omeprazol, siendo el omeprazol un enantiómero
Nefritis aguda intersticial: La nefritis intersticial aguda se ha observado en pacientes que consumen IBPs incluido PAMEZONE. La nefritis intersticial aguda puede ocurrir en cualquier punto durante la terapia con IBP y es generalmente atribuida a una reacción de hipersensibilidad idiopática. Descontinuar el uso de PAMEZONE si se adquiere nefritis aguda intersticial. [ver Contraindicaciones].
Deficiencia de cianocobalamina (vitamina B12): El tratamiento diario con algún medicamento supresor de ácido a largo plazo (por ejemplo más de tres años) puede causar malabsorción de cianocobalamina (vitamina B12) causada por hipo o aclorhidria. Casos raros de deficiencia de cianocobalamina ocurridos por una terapia de supresión de ácido han sido reportados en la literatura. Este diagnóstico debe ser considerado si se observan síntomas clínicos compatibles con la deficiencia de cianocobalamina.
Diarrea asociada a Clostridium difficile: Los estudios observacionales publicados sugieren que la terapia con IBP como PAMEZONE se puede asociar a un mayor riesgo de diarrea asociada a Clostridium difficile, especialmente en el pacientes hospitalizados. Este diagnóstico debe ser considerado para la diarrea que no mejora [ver Reacciones adversas].
Los pacientes deben utilizar la dosis más baja y la duración más corta del tratamiento con IBP adecuado a la enfermedad que padece.
Diarrea asociada a Clostridium difficile (DACD) ha sido reportada con el uso de casi todos agentes antibacterianos. Para obtener más información específica a los agentes antibacterianos (claritromicina y amoxicilina) indicado para su uso en combinación con PAMEZONE, consulte la sección de Advertencias y Precauciones en sus insertos respectivos.
Interacción con clopidogrel: Se debe evitar el uso concomitante de PAMEZONE con clopidogrel. El clopidogrel es un profármaco. La inhibición de la agregación plaquetaria por clopidogrel se debe enteramente a un metabolito activo. El metabolismo del metabolito activo del clopidogrel puede verse afectado por el uso con medicamentos concomitantes, tales como esomeprazol, que inhiben la actividad de CYP2C19. El uso concomitante de clopidogrel con 40 mg de esomeprazol reduce la actividad farmacológica del clopidogrel. Cuando se usa PAMEZONE se debe considerar una terapia alternativa antiplaquetaria [ver Interacciones medicamentosas, y Propiedades farmacológicas - Farmacocinética].
Fractura ósea: Un gran número de estudios observacionales publicados sugieren que la terapia con el inhibidor de la bomba de protones (IBP) puede estar asociada a un mayor riesgo de osteoporosis relacionado con fracturas de cadera, muñeca o columna vertebral. El riesgo de fractura se incrementó en pacientes que recibieron una dosis elevada, definida por dosis múltiples y diarias y a largo plazo con terapia del IBP (un año a más).Los pacientes deben usar la dosis más baja y la terapia con IBP más corta apropiada a la condición de cada paciente. Pacientes con riesgo de fracturas relacionadas a la osteoporosis deben ser manejados de acuerdo al tratamiento establecido [ver Posología y forma de administración, y Reacciones adversas].
Hipomagnesemia: La hipomagnesemia, sintomática o asintomática, se ha reportado raramente en pacientes tratados con IBPs por al menos tres meses, en muchos de los casos después del año de tratamiento. Complicaciones severas incluyen tetania, arritmias y convulsiones. En la mayoría de los pacientes, el tratamiento de la hipomagnesemia requiere reemplazo de magnesio y la interrupción de IBP.
Para los pacientes que requieren un tratamiento prolongado o que toman IBPs con medicamentos como digoxina o fármacos que puedan causar hipomagnesemia (por ejemplo, diuréticos) los profesionales de la salud pueden considerar monitorizar los niveles de magnesio antes de iniciar el tratamiento con IBP así como periódicamente [ver Reacciones adversas].
Uso concomitante de PAMEZONE con la hierba de San Juan o Rifampicina: Los fármacos que inducen CYP2C19 o CYP3A4 (como rifampicina o la hierba de San Juan) pueden disminuir sustancialmente las concentraciones de esomeprazol [véase Interacciones medicamentosas]. Evitar el uso concomitante de PAMEZONE con la hierba de San Juan o rifampicina.
Interacciones con investigaciones diagnósticas de Tumores Neuroendocrinos: Los niveles séricos de cromogranina A (CgA) se incrementan secundariamente a la reducción de la acidez gástrica inducida por fármacos. El incremento de los niveles de CgA puede causar resultados falsos positivos en las investigaciones diagnósticas de tumores neuroendocrinos. Los profesionales de la salud deben suspender temporalmente el tratamiento de esomeprazol por lo menos 14 días antes de evaluar los niveles de CgA y considerar repetir la prueba si los niveles iniciales de CgA están elevados. Si se llevan a cabo pruebas en serie (para el control, por ejemplo), se deben utilizar pruebas del mismo laboratorio comercial, pues los rangos de referencia pueden variar entre las pruebas. [ver Propiedades farmacológicas - Farmacodinámica]
Uso concomitante con metrotexato: La bibliografía sugiere que el uso concomitante de IBPs con metotrexato (principalmente en dosis elevadas; ver la información de prescripción para el metotrexato) puede elevar y prolongar los niveles séricos de metotrexato y/o su metabolito, que posiblemente lleve a toxicidad del metotrexato. En la administración de dosis elevadas de metotrexato se puede considerar el retiro temporal de IBP en algunos pacientes [ver Interacciones medicamentosas].
PRECAUCIONES:
Embarazo:
Embarazo Categoría: C
Resumen de riesgos: No hay estudios adecuados y bien controlados con PAMEZONE en mujeres embarazadas. Esomeprazol es el isómero S del omeprazol. Los datos epidemiológicos disponibles no logran demostrar un aumento del riesgo de malformaciones congénitas u otros adversos del embarazo con el uso en el primer trimestre de omeprazol.
No se observó teratogenicidad en los estudios de reproducción animal con la administración por vía oral de esomeprazol magnesio en ratas y conejos con dosis aproximadamente 68 veces y 42 veces, respectivamente, una dosis humana oral de 40 mg (basado en una base de área de superficie corporal de una persona de 60 kg). Sin embargo, no se observaron cambios en la morfología ósea de las crías de ratas dosificadas a través de la mayor parte de embarazo y la lactancia en dosis iguales a o mayores que aproximadamente 34 veces la dosis humana oral de 40 mg (ver Datos para animales). Debido al efecto en el desarrollo óseo observado en ratas a altas dosis de esomeprazol magnesio, PAMEZONE debe utilizarse durante el embarazo sólo si el beneficio potencial justifica el riesgo potencial para el feto.
Datos en humanos: Esomeprazol es el isómero S del omeprazol. Cuatro estudios epidemiológicos comparan la frecuencia de anormalidades congénitas en infantes de madres que usan omeprazol durante el embarazo con la frecuencia de anormalidades de infantes de mujeres expuestas Al receptor de antagonistas de H2 u otros controles
Un estudio epidemiológico retrospectivo de cohortes basado en los registros de nacimiento del Swedish Medical, que cubren aproximadamente el 99% de los embarazos, desde 1995-99 informó sobre 955 lactantes (824 expuestos durante el primer trimestre, 39 de ellos expuestos más del primer trimestre y 131 expuestos después del primer trimestre) cuyas madres usaron omeprazol durante el embarazo. El número de infantes expuestos al omeprazol en el útero que no tenían ninguna malformación, bajo peso al nacer, índice de Apgar bajo, o la hospitalización fue similar a la observada en esta población. El número de infantes que nacen con defectos del septo ventricular y el número de los fallecidos al nacer fue ligeramente mayor en los recién nacidos expuestos a omeprazol que las cifras esperadas en esta población.
Un estudio de cohortes retrospectivo basado en la población que cubre todos los nacimientos vivos en Dinamarca desde 1996- 2009, informó sobre 1.800 nacidos vivos 837 cuyas madres usaron omeprazol durante el primer trimestre del embarazo y, 317 nacidos vivos cuyas madres no utilizaron ningún inhibidor de la bomba de protones. La tasa global de defectos de nacimiento en los bebés nacidos de madres que consumían omeprazol en el primer trimestre fue de 2,9% y 2,6% en los bebés nacidos de madres que no estaban expuestas a ninguna bomba de protones durante el primer trimestre de embarazo.
Un estudio de cohortes retrospectivo informó sobre 689 mujeres embarazadas expuestas a bloqueadores de H2 u omeprazol en el primer trimestre (134 expuestos al omeprazol) y 1.572 mujeres embarazadas no expuestas durante el primer trimestre. La tasa de malformaciones en la descendencia nacida de las madres con la exposición al primer trimestre del omeprazol, un bloqueador de H2, o no fueron expuestas fueron 3.6%, 5.5% y 4.1%, respectivamente.
Un pequeño estudio de cohorte prospectivo observacional seguido 113 mujeres expuestas al omeprazol durante el embarazo (89% exposiciones en el primer trimestre). La tasa de notificación de las principales malformaciones congénitas fue del 4% en el grupo de omeprazol, 2% en los controles no expuestos a teratógenos, y el 2,8% controles expuestos. Las tasas de abortos espontáneos y electivos, parto prematuro, edad gestacional al momento del parto, y el peso medio al nacer fueron similares entre los grupos.
Numerosos estudios no han reportado efectos adversos aparentes a corto plazo en el lactante cuando solo una dosis de omeprazol oral o intravenosa se administró a más de 200 mujeres embarazadas, como pre medicación para la cesárea bajo anestesia general.
Datos en animales: Estudios en la reproducción se han realizado con magnesio esomeprazol en ratas por vía oral dosis de hasta 280 mg/kg/día (aproximadamente 68 veces la dosis humana oral de 40 mg en base a la superficie corporal) y en conejos con dosis orales de hasta 86 mg/kg/día (aproximadamente 41 veces un ser humano por vía oral dosis de 40 mg en base al área de la superficie corporal) y no han revelado ninguna evidencia de deterioro de la fertilidad o daño fetal debido a esomeprazol magnesio.
Un estudio de toxicidad para el desarrollo prenatal y postnatal en ratas con criterios de valoración adicionales a evaluar el desarrollo óseo se realizó con magnesio esomeprazol en dosis orales de 14 a 280 mg/kg/día (aproximadamente 3,4 a 68 veces la dosis humana oral de 40 mg basado en la superficie corporal). Neonatal/prematuro (desde el nacimiento al destete) se redujo la supervivencia a dosis iguales o mayores que 138 mg/kg/día (aproximadamente 34 veces la dosis humana oral de 40 mg basados en la superficie corporal). El peso corporal y el peso corporal ganado se redujeron y el comportamiento neurológico o desarrollo general se retrasó inmediatamente después del destete fueron evidentes en dosis iguales o mayor que 69 mg/kg/día (aproximadamente 17 veces la dosis humana oral de 40 mg en un cuerpo basados en la superficie). Además, la disminución de la longitud del fémur, la anchura y el espesor del hueso cortical, disminución de espesor de la placa de crecimiento tibial y leve hipocelularidad en a la médula ósea se encontraron a dosis iguales o superiores a 14 mg/kg/día (aproximadamente 3,4 veces una dosis humana oral de 40 mg base al área de superficie corporal). Displasia ósea en el fémur fue observado en las crías de ratas tratadas con dosis orales de magnesio esomeprazol en dosis iguales o mayores de 138 mg/kg/día (aproximadamente 34 veces la dosis humana oral de 40 mg en una superficie corporal).
No se observaron efectos sobre el hueso materno en ratas embarazadas y lactantes en un estudio de toxicidad pre y postnatal cuando magnesio esomeprazol se administró a dosis orales de 14 a 280 mg/kg/día (aproximadamente 3,4 a 68 veces la dosis humana oral de 40 mg en una basados en una superficie corporal).Cuando se les administró a las ratas desde el día 7 de gestación hasta el destete en el día 21 postnatal, una disminución estadísticamente significativa en el peso fémur materno de hasta 14% (en comparación con el tratamiento con placebo) fue observado en dosis iguales o mayores que 138 mg/kg/día (aproximadamente 34 veces una dosis humana oral de 40 mg en base a la superficie corporal).
Un estudio previo y postnatal en ratas con estroncio esomeprazol (usando una dosis equimolar en comparación con el estudio de esomeprazol magnesio) produjo resultados similares en los amamantados como se describe anteriormente.
Lactancia: El esomeprazol está probablemente presente en la leche humana. Esomeprazol es el isómero S de omeprazol y datos limitados indican que las dosis maternas de omeprazol 20 mg al día producen bajos niveles de la leche humana. Se debe tener cuidado cuando se administra PAMEZONE a una mujer lactante.
Uso pediátrico: La seguridad y eficacia de esomeprazol se ha establecido en pacientes pediátricos de 1 a 17 años de edad para el tratamiento a corto plazo (hasta ocho semanas) de la ERGE. La seguridad y la eficacia de esomeprazol se han establecido en pacientes pediátricos de 1 mes a menos de 1 año para el tratamiento a corto plazo (hasta 6 semanas) de la esofagitis erosiva debido al ácido mediados ERGE. Sin embargo, la seguridad y la eficacia de esomeprazol no se han establecido en los pacientes de menos de 1 mes de edad.
De 1 a 17 años de edad: El uso de esomeprazol en pacientes pediátricos y adolescentes 1 a 17 años de edad en un tratamiento a corto plazo (hasta ocho semanas) de la ERGE es apoyado por la extrapolación de los resultados a partir de estudios adecuados y bien controlados para adultos y estudios de seguridad y farmacocinéticos realizados en pacientes pediátricos y adolescentes [ver Dosificación y administración (2), Reacciones Adversas (6.1), Farmacología Clínica (12.3), y Estudios Clínicos (14.3) ]. La seguridad y la efectividad de esomeprazol para otros usos pediátricos todavía no ha sido establecida.
Neonatos de 0 a 1 mes de edad: Después de la administración por vía oral de esomeprazol a los recién nacidos la media geométrica (rango) para el depuración aparente (CL/F) fue de 0,55 l/h/kg (0,25 a 1,6 l/h/kg).
No se ha establecido la seguridad y eficacia de esomeprazol en los recién nacidos.
Datos en animales jóvenes: En un estudio de toxicidad en ratas jóvenes, esomeprazol se administró con magnesio y sales de estroncio en dosis orales de 34 a 68 veces a la dosis humana diaria de 40 mg en basada en el área de la superficie corporal. La mortalidad se observa a dosis altas de esomeprazol, hubo una reducción y ganancia en el peso corporal, un aumento del peso y grosor del fémur y disminución del crecimiento general [ver Datos de seguridad pre clínica].
Uso geriátrico: Del número total de pacientes que recibieron esomeprazol en ensayos clínicos 1459 tenían de 65 a 74 años de edad y 354 pacientes tenían una edad ≥ 75 años.
No se observaron diferencias significativas en la seguridad y eficacia entre las personas de edad y más jóvenes, y otro reporte clínico no identifica diferencias en las respuestas entre los ancianos y los pacientes más jóvenes, pero existe mayor sensibilidad en personas mayores que no se puede descartar.
DOSIS Y VÍA DE ADMINISTRACIÓN:
Dosis usual en adultos:
• Tratamiento de enfermedad por reflujo gastroesofágico (ERGE): Vía oral, 20 a 40 mg una vez al día por 4 a 8 semanas.
En pacientes que no hayan curado en el periodo inicial de tratamiento de 4 a 8 semanas, se puede considerar una terapia adicional de igual duración.
• Mantenimiento de esofagitis erosiva curada: Vía oral, 20 mg una vez al día.
• Tratamiento de enfermedad por reflujo gastroesofágico sintomática: Vía oral, 20 mg una vez al día durante 4 semanas.
En pacientes cuyos síntomas no se hayan resuelto completamente después de un periodo de tratamiento de 4 semanas, se puede considerar una terapia adicional de igual duración.
• Reducción del riesgo de úlcera gástrica asociada con AINEs: Vía oral, 20 o 40 mg una vez al día por hasta 6 meses.
Nota: En pacientes con disfunción hepática severa (clase C en la escala de Child Pugh), la dosis no debe exceder 20 mg de esomeprazol al día.
Dosis usual pediátrica: No se han establecido la seguridad y eficacia para indicaciones diferentes a ERGE.
• Tratamiento a corto plazo de ERGE:
— Niños de 12 a 17 años de edad: Vía oral, 20 o 40 mg una vez al día por hasta 8 semanas.
— Niños menores a 12 años de edad: No se han establecido la seguridad y eficacia.
Dosis usual geriátrica: Ver Dosis usual en adultos.
POSOLOGÍA Y FORMA DE ADMINISTRACIÓN:
PAMEZONE se presenta en cápsulas con microgránulos gastrorresistentes para administración oral o en paquetes para la preparación de suspensiones orales de liberación retardada. Las dosis recomendadas se resumen en la Tabla 5. PAMEZONE debe tomarse al menos una hora antes de las comidas.
La duración de la administración del inhibidor de la bomba de protones debe estar basado en datos específicos de seguridad y eficacia para definir la indicación y frecuencia de las dosis, como se describe en la información de prescripción, y las necesidades médicas de cada paciente. El tratamiento con el inhibidor de la bomba de protones solo debe ser iniciado y continuado si los beneficios superan los riesgos del tratamiento.
Tabla 5: Esquema posológico recomendado de PAMEZONE
|
Indicación |
Dosis |
Frecuencia |
|
Enfermedad por Reflujo Gastroesofágico (ERGE) |
||
|
Curación de esofagitis erosiva |
20 mg o 40 mg |
Una vez al día durante 4 a 8 semanas* |
|
Mantenimiento de curación de esofagitis erosiva |
20 mg |
Una vez al día** |
|
Enfermedad por reflujo gastroesofágico sintomático |
20 mg |
Una vez al día durante 4 semanas*** |
|
ERGE pediátrico |
||
|
12 a 17 años de edad |
||
|
Curación de esofagitis erosiva |
20 mg o 40 mg |
Una vez al día durante 4 a 8 semanas |
|
ERGE sintomático |
20 mg |
Una vez al día durante 4 semanas |
|
1 a 11 años+ de edad |
||
|
Curación de esofagitis erosiva |
||
|
peso ≥ 20 kg |
10 mg o 20 mg |
Una vez al día durante 8 semanas |
|
Reducción del riesgo de úlcera gástrica asociada a AINES |
20 mg o 40 mg |
Una vez al día durante un máximo de 6 meses** |
|
Erradicación de H. pylori para reducir el riesgo de recurrencia de úlcera duodenal |
||
|
Terapia triple: |
||
|
PAMEZONE |
40 mg |
Una vez al día durante 10 días |
|
Amoxicilina |
1000 mg |
Dos veces al día durante 10 días |
|
Claritromicina |
500 mg |
Dos veces al día durante 10 días |
|
Condiciones de hipersecreción patológica que incluye el síndrome de Zollinger-Ellison |
40 mg† |
‡Dos veces al día |
|
*La mayoría de los pacientes se curan dentro de 4 a 8 semanas. Para los pacientes que no se curan después de 4 a 8 semanas, puede ser considerado un tratamiento de 4 a 8 semanas adicional. **Los estudios controlados no se extendieron más de seis meses. ***Si los síntomas no se resuelven completamente después de 4 semanas, puede ser considerado un tratamiento adicional de 4 semanas. + No se han estudiado dosis mayores a 1 mg/kg/día. † La dosis de PAMEZONE en pacientes con la condición de hipersecreción patológica varía de forma individual con cada paciente. Los regímenes de dosificación se deben ajustar a las necesidades individuales de cada paciente. ‡ Dosis de hasta 240 mg se han administrado diariamente [ver Interacciones medicamentosas]. |
||
Por favor revisar la información de prescripción de amoxicilina y claritromicina respecto a Contraindicaciones, Advertencias, y dosificación en pacientes adultos mayores y pacientes con insuficiencia renal.
Poblaciones especiales: Insuficiencia hepática: En pacientes con insuficiencia hepática de leve a moderada (Child-Pugh clase A y B), el ajuste de dosis no es necesario. Para los pacientes con insuficiencia hepática grave (Child-Pugh Clase C), no se debe exceder de una dosis de 20 mg de PAMEZONE [ver Propiedades farmacológicas - Farmacocinética].
Las pautas para el uso específico de los métodos y vías de administración por cada una de las dosis se presentan en la Tabla 6.
Tabla 6: Opciones de administración
|
Opciones de administración (Véase el texto adjunto a la tabla para instrucciones adicionales) |
||
|
Forma de dosificación |
Vía |
Opciones |
|
Cápsulas con microgránulos gastrorresistentes |
Oral |
La cápsula puede ser ingerida completamente. -o- La cápsula se puede abrir y mezclar con puré de manzana. |
|
Cápsulas de liberación retardada |
Sonda nasogástrica |
Abrir la cápsula y llenar en una jeringa los gránulos intactos, luego administrar a través de la sonda nasogástrica. |
PAMEZONE Cápsulas con microgránulos gastrorresistentes: PAMEZONE cápsulas con microgránulos gastrorresistentes deben ser tragadas enteras.
Alternativamente, para los pacientes que tienen dificultad para tragar las cápsulas, una cucharada de puré de manzana se puede añadir a un recipiente vacío y la cápsula de PAMEZONE de liberación retardada puede ser abierta, y los gránulos dentro de la cápsula cuidadosamente vaciados sobre el puré. Los gránulos se deben mezclar con el puré de manzana y ser ingeridos inmediatamente: No almacene para uso futuro. El puré de manzana utilizado no debe estar caliente y debe ser lo suficientemente suave para ser tragado sin masticar. Los gránulos no deben masticarse ni triturarse. Si la mezcla gránulos/puré de manzana no se utiliza en su totalidad, la mezcla restante se debe descartar inmediatamente.
Para los pacientes que tienen una sonda nasogástrica, la cápsula de liberación retardada PAMEZONE se puede abrir y vaciar los gránulos intactos en el catéter con punta de jeringa de 60 ml y mezclar con 50 ml de agua. Es importante usar únicamente el catéter con punta de jeringa cuando se administra PAMEZONE a través del tubo nasogástrico. Desplazar el émbolo y agitar la jeringa vigorosamente por 15 segundos. Mantenga la jeringa con la punta hacia arriba y comprobar si hay gránulos que quedan en la punta. Conectar la jeringa a un tubo nasogástrico y liberar el contenido de la jeringa a través de la sonda nasogástrica en el estómago. Después de la administración de los gránulos, la sonda nasogástrica debe lavarse con abundante agua. No administrar los gránulos si se han disuelto o desintegrado.
La mezcla debe ser utilizada inmediatamente después de su preparación.
SOBREDOSIS:
Una sola dosis oral de esomeprazol de 510 mg/kg (aproximadamente 124 veces la dosis humana basados en el área de superficie corporal), fue letal para ratas. Los principales signos de toxicidad aguda se redujeron a actividad motora, cambios en la frecuencia respiratoria, temblor, ataxia, convulsiones clónicas e intermitentes.
Los síntomas descritos en relación con la sobredosis deliberada de PAMEZONE (experiencias limitadas de dosis superiores a 240 mg/día) son transitorios. Las dosis únicas de 80 mg de esomeprazol fueron toleradas sin incidentes. Los informes de sobredosis con omeprazol en humanos pueden ser también relevante. Las dosis oscilaron hasta 2.400 mg (120 veces la dosis clínica habitual recomendada).Las manifestaciones fueron variables, pero incluyen confusión, somnolencia, visión borrosa, taquicardia, náuseas, sudoración, enrojecimiento, dolor de cabeza, sequedad de boca, y otras reacciones adversas similares a los observados en la experiencia clínica habitual (ver el prospecto omeprazol – Reacciones adversas). No hay un antídoto conocido y específico para esomeprazol. Dado que el esomeprazol es una proteína ligada, no se espera que pueda ser eliminada por diálisis. En el caso de sobredosis, el tratamiento debe ser sintomático y de apoyo.
Al igual que con el manejo de cualquier sobredosis, debe considerarse la posibilidad de ingestión de múltiples fármacos.
MONITOREO DEL PACIENTE: No aplica.
EXPIRACIÓN DEL PRODUCTO:
No utilizar después de la fecha de vencimiento que aparece en el envase.
La fecha de vencimiento es el último día del mes que se indica.