
KEFLEX
CEFALEXINA MONOHIDRATADA
Tabletas
FORMA FARMACÉUTICA Y FORMULACIÓN:
KEFLEX® 500 mg Tabletas recubiertas:
Cada TABLETA RECUBIERTA contiene:
Cefalexina monohidrato equivalente a 500 mg
de cefalexina base.
Excipientes*c.s.p 1 tableta
* Celulosa microcristalina, estearato de magnesio, glicolato sódico de almidón, Opadry II naranja.
KEFLEX® 250 m g/5 mL Suspensión:
Cada 5 mL de la SUSPENSIÓN contiene:
Cefalexina monohidrato 262.95 mg equivalente a 250 mg de cefalexina base.
Excipientes*c.s.p 5 mL
*Lecitina refinada, butilparabeno, estearato de aluminio, aceite de ricino hidrogenado, sacarosa granulada, cloruro de sodio, rojo D&C N°6 Laca de bario, saborizante artificial a fresa, aceite de coco fraccionado.
INDICACIONES:
La cefalexina está indicada para el tratamiento de las siguientes infecciones causadas por cepas susceptibles de los microorganismos ya designados:
Infecciones del tracto respiratorio causadas por Streptococcus pneumoniae y Streptococcus pyogenes (la penicilina es el fármaco habitual de elección en el tratamiento y la prevención de las infecciones estreptocócicas, incluyendo la profilaxis de la fiebre reumática. La cefalexina es generalmente eficaz en la erradicación de los estreptococos de la nasofaringe; Sin embargo no están disponibles en la actualidad datos sustanciales que establecen la eficacia de cefalexina en la subsiguiente prevención de la fiebre reumática).
Otitis media debido a Streptococcus pneumoniae, Haemophilus influenzae, Staphylococcus aureus, Streptococcus pyogenes, y Moraxella catarrhalis. Infecciones de la piel y estructura de la piel causada por Staphylococcus aureus y/o Streptococcus pyogenes. Infecciones óseas causadas por Staphylococcus aureus y/o Proteus mirabilis. Infecciones del tracto genitourinario, incluyendo prostatitis aguda, causada por Escherichia coli, Proteus mirabilis, y Klebsiella pneumoniae.
Nota: Se deben efectuar los cultivos y estudios de susceptibilidad adecuados antes y durante el tratamiento para determinar la susceptibilidad del microorganismo patógeno a la cefalexina. Cuando estén indicados, deben efectuarse estudios de función renal.
Para reducir el desarrollo de bacterias resistentes a los medicamentos y mantener la eficacia de las cápsulas de cefalexina, cefalexina para suspensión oral, Tabletas de cefalexina y otros fármacos antibacterianos, las cápsulas de cefalexina, cefalexina para suspensión oral y tabletas de cefalexina sólo deben usarse para tratar o prevenir las infecciones que se ha comprobado o se sospecha fuertemente que es causada por bacterias susceptibles. Cuando los cultivos y la información de susceptibilidad están disponibles, Estos deben ser considerados en la selección o modificación de la terapia antibacteriana. En la ausencia de estos datos, los patrones de la epidemiología y la susceptibilidad locales pueden contribuir a la selección empírica de la terapia.
MECANISMO DE ACCIÓN
Farmacología humana: La cefalexina es resistente a los ácidos y puede ser administrada con o entre las comidas. Es absorbida rápidamente tras la administración oral. Después de haber administrado dosis de 250 mg, 500 mg y 1 g, se obtuvieron a la hora, concentraciones séricos máximas de aproximadamente 9, 18, y 32 mcg/ml, respectivamente. Existen concentraciones séricas medibles hasta por 6 horas después de su administración. La cefalexina se excreta en la orina por filtración glomerular y secreción tubular. Los estudios demostraron que más del 90% del fármaco se excreta sin cambios en la orina dentro de las 8 horas. Durante este período las concentraciones urinarias pico después de administrar 250 mg, 500 mg y 1 g dosis fueron de aproximadamente 1000, 2200, y 5000 mcg/ml, respectivamente.
Microbiología: Los estudios “in vitro” demuestran que las cefalosporinas son bactericidas porque inhiben la síntesis de la pared celular. La cefalexina ha demostrado ser activa contra la mayoría de cepas de los siguientes microorganismos, tanto in vitro como en infecciones clínicas que se describe en la sección de indicaciones.
Aerobios, gram-positivos:
• Staphylococcus aureus (incluyendo cepas productoras de penicilinasa).
• Streptococcus pneumoniae (cepas susceptibles a la penicilina).
• Streptococcus pyogenes
Aerobios, gram-negativos:
• Escherichia coli
• Haemophilus influenzae
• Klebsiella pneumoniae
• Moraxella (Branhamella) catarrhalis
• Proteus mirabilis
Nota: La mayoría de las cepas de enterococos (Enterococcus faecalis [anteriormente Streptococcus faecalis]) y los estafilococos resistentes a meticilina son resistentes a las cefalosporinas incluyendo cefalexina. No es activa contra la mayoría de las cepas de las especies de Entrobacter, Morganella morganii (anteriormente Proteus morganii) y Proteus vulgaris. No es activa contra las especies de Pseudomonas o Acinetobacter calcoaceticus (anteriormente especies Mima y Herellea).
CONTRAINDICACIONES:
La cefalexina está contraindicada en pacientes con alergia conocida al grupo de antibióticos cefalosporínicos.
REACCIONES ADVERSAS:
Gastrointestinales: Aparición de colitis pseudomembranosa puede ocurrir durante o después del tratamiento antibacteriano. Náuseas y vómitos se han reportado raramente. La diarrea ha sido el efecto secundario más frecuente. En muy rara vez lo suficientemente grave como para justificar el cese de la terapia.
Dispepsia, gastritis, y dolor abdominal también se han producido. Al igual que con algunas penicilinas y algunas otras cefalosporinas, hepatitis transitoria e ictericia colestásica se han reportado raramente.
Hipersensibilidad: Reacciones alérgicas en forma de erupción cutánea, urticaria, angioedema, y, rara vez, eritema multiforme, síndrome de Stevens-Johnson o necrólisis epidérmica tóxica han sido observadas.
Estas reacciones por lo general desaparecieron al suspender el medicamento. En algunas de estas reacciones, puede ser necesaria la terapia de apoyo. También se ha informado de anafilaxia.
Otras reacciones han incluido prurito, moniliasis genital y anal, genital, flujo vaginal y vaginitis, mareos, fatiga, dolor de cabeza, agitación, confusión, alucinaciones, artralgias, artritis, y trastorno de las articulaciones. Nefritis intersticial reversible se ha comunicado raramente. También se han reportado eosinofilia, neutropenia, trombocitopenia, anemia hemolítica y ligeras elevaciones de AST y ALT.
Además de las reacciones adversas anteriormente mencionadas que se han observado en pacientes tratados con cefalexina, se han notificado las siguientes reacciones adversas y pruebas de laboratorio alteradas para antibióticos de la clase de cefalosporina:
Reacciones adversas: Fiebre, colitis, anemia aplásica, hemorragia, disfunción renal, y nefropatía tóxica.
Varias cefalosporinas han estado implicadas en convulsiones desencadenantes, sobre todo en pacientes con insuficiencia renal cuando la dosis no se redujo (ver Indicaciones y uso y Precauciones). Si se producen convulsiones asociadas con el tratamiento farmacológico, el fármaco debe ser descontinuado. Un tratamiento anticonvulsivo se puede dar si está clínicamente indicado.
Pruebas de laboratorio alteradas: Tiempo de protrombina prolongada, aumento de urea, aumento de creatinina, fosfatasa alcalina elevada, bilirrubina elevada, LDH elevada, pancitopenia, leucopenia y agranulocitosis.
INTERACCIONES:
Metformina: En personas sanas que recibieron dosis únicas de 500 mg de cefalexina y metformina, la Cmax media y AUC de metformina plasmática aumentaron en un promedio de 34% y 24%, respectivamente, y el aclaramiento renal medio de metformina disminuyo en un 14%. No se dispone de información acerca de la interacción de la cefalexina y metformina después de múltiples dosis de cada fármaco.
Aunque no se observó en este estudio, podrían surgir potencialmente efectos adversos de la administración conjunta de cefalexina y metformina por la inhibición de la secreción tubular a través de los sistemas de transportador de cationes orgánicos. En consecuencia, se recomienda la monitorización cuidadosa del paciente y ajustar la dosis de metformina en pacientes que toman concomitantemente cefalexina y metformina.
Probenecid: Al igual que con otros B-lactámicos, la excreción renal de cefalexina es inhibida por probenecid.
Pruebas de laboratorio de interacciones con drogas: Como resultado de la administración de cefalexina, puede ocurrir una reacción falsa positiva para glucosa en orina. Esto se ha observado con las soluciones de Benedict y Fehling y también con Clinitest®.
Carcinogénesis, mutagénesis, deterioro de la fertilidad: Estudios de Tiempo de vida en animales no han sido desarrollados para evaluar el potencial carcinogénico de cefalexina. No se han realizado pruebas para determinar el potencial mutagénico de cefalexina. En ratas macho y hembra, la fertilidad y la función reproductora no fueron afectados por dosis orales de cefalexina hasta 1,5 veces la dosis máxima recomendada en humanos sobre la base de mg/m2.
Embarazo:
Efectos teratogénicos.
Categoría B de embarazo: Estudios de reproducción se han realizado en ratones y ratas con dosis orales de cefalexina monohidrato 0,6 y 1,5 veces la dosis humana diaria máxima (66 mg / kg / día) en base a mg/m2, y no han revelado ningún daño al feto. No obstante, no hay estudios adecuados y bien controlados en mujeres embarazadas. Dado que los estudios de reproducción en animales no siempre son predictivos de la respuesta humana, este medicamento debe usarse durante el embarazo sólo si es claramente necesario.
Lactancia: La excreción de cefalexina en la leche humana aumentó hasta 4 horas después de una dosis de 500 mg, el medicamento alcanzó un nivel máximo de 4 mcg / ml, luego disminuyó gradualmente, y había desaparecido 8 horas después de la administración. Se debe tener precaución cuando se administra cefalexina a una mujer lactante.
Uso pediátrico: La seguridad y eficacia de cefalexina en pacientes pediátricos fue establecida en ensayos clínicos para las dosis descritas en la sección Dosis y administración. En estos ensayos, los pacientes pediátricos pueden haber recibido cefalexina para suspensión oral. Las tabletas de cefalexina sólo deben usarse en niños y adolescentes capaces de ingerir la tableta.
Uso geriátrico: De 701 sujetos en 3 estudios clínicos publicados de cefalexina, 433 (62%) eran de 65 años a más. No se observaron diferencias generales en la seguridad o eficacia entre estos sujetos y los sujetos más jóvenes, y otra experiencia clínica informada no identificó diferencias en las respuestas entre los ancianos y los pacientes más jóvenes, pero una mayor sensibilidad en algunos individuos mayores no se puede descartar.
Este medicamento se sabe que se excreta principalmente por el riñón, y el riesgo de reacciones tóxicas a este fármaco puede ser mayor en pacientes con insuficiencia renal. Dado que los pacientes de edad avanzada son más propensos a padecer disfunción renal, se debe tener cuidado al seleccionar la dosis y esto puede ser de utilidad para controlar la función renal (ver Precauciones).
ADVERTENCIAS:
Antes de instituir la terapia con cefalexina, debe determinarse si el paciente ha tenido reacciones previas de hipersensibilidad a la cefalexina, cefalosporinas, penicilinas u otros fármacos. Si este producto es administrado a pacientes sensibles a la penicilina, se debe tener precaución ya que ha sido claramente documentada hipersensibilidad cruzada entre antibióticos betalactámicos y pueden ocurrir hasta en el 10% de los pacientes con antecedentes de alergia a la penicilina. Si ocurre una reacción alérgica a cefalexina, debe suspenderse el uso del fármaco. Reacciones graves de hipersensibilidad aguda pueden requerir tratamiento con epinefrina y otras medidas de emergencia, incluyendo oxígeno, fluidos intravenosos, antihistamínicos intravenosos, corticosteroides, aminas presoras y administración por vía respiratoria, según esté clínicamente indicado.
Existe alguna evidencia clínica y de laboratorio de una alergenicidad cruzada parcial de las penicilinas y las cefalosporinas. Algunos pacientes han reportado haber tenido reacciones graves (incluyendo anafilaxia) a ambos medicamentos.
Cualquier paciente que haya mostrado alguna forma de alergia, particularmente a los medicamentos, debe recibir antibióticos con cautela.
No debe hacerse excepción con respecto a la cefalexina.
Clostridium difficile asociado a diarrea (CDAD) ha sido reportado con el uso de casi todos los agentes antibacterianos, incluyendo cefalexina, y puede variar en gravedad desde diarrea leve a colitis fatal. El tratamiento con agentes antibacterianos altera la flora normal del colon que lleva a sobrecrecimiento de C. difficile.
C. difficile produce toxinas A y B que contribuyen al desarrollo de CDAD.
Hipertoxina producida por cepas de C. difficile causa aumento de la morbilidad y la mortalidad, ya que estas infecciones pueden ser refractarias a la terapia antimicrobiana y pueden requerir colectomía. CDAD debe ser considerada en todos los pacientes que presenten diarrea después del uso de antibióticos. Una historia médica cuidadosa es necesaria, ya que la presencia de CDAD se ha reportado más de dos meses después de la administración de agentes antibacterianos.
Si se sospecha o confirma CDAD, el uso de antibióticos continuo no es dirigido contra C. difficile y puede necesitar ser interrumpido. Control adecuado fluidos y de electrolitos, suplementación proteica, tratamiento antibiótico de C. difficile y evaluación quirúrgica, se deben instituir según criterio clínico.
PRECAUCIONES:
General: Prescripción de KEFLEX® 250 mg/5 mL suspensión, o KEFLEX® 500 mg tabletas recubiertas en ausencia de una infección bacteriana comprobada, o fuerte sospecha de ella, o una indicación profiláctica, es poco probable que proporcione beneficio para el paciente y aumente el riesgo de desarrollo de bacterias resistentes a los fármacos.
Los pacientes deben ser cuidadosamente vigilados para que cualquier efecto secundario o manifestaciones inusuales de la idiosincrasia de los medicamentos puedan ser detectados. Si se presenta una reacción alérgica a la cefalexina, la administración del medicamento debe ser suspendida y el paciente debe ser tratado con los medicamentos habituales (Epinefrina u otras aminas vasopresoras, antihistamínicos o corticosteroides).
El uso prolongado de cefalexina puede dar lugar a la proliferación de microorganismos no susceptibles. La observación cuidadosa del paciente es esencial. Si se produce una sobreinfección durante el tratamiento, se deben tomar las medidas adecuadas.
Resultados positivos de Coombs directo se notificaron durante el tratamiento con antibióticos de cefalosporinas. En estudios hematológicos o en procedimientos de pruebas cruzadas de transfusión cuando las pruebas de antiglobulina se realizan en el lado menor se debe reconocer que una prueba de Coombs positiva puede ser debido a la drogas, o en pruebas de Coombs en recién nacidos cuyas madres han recibido antibióticos de cefalosporina antes del parto.
La cefalexina se debe administrar con precaución en presencia de insuficiencia renal severa. Bajo tales condiciones, una observación clínica cuidadosa y estudios de laboratorio deben hacerse porque la dosificación segura puede ser menor que la normalmente recomendada.
Procedimientos quirúrgicos indicados deben llevarse a cabo en combinación con la terapia antibiótica.
Los antibióticos de amplio espectro deben prescribirse con precaución en personas con antecedentes de enfermedad gastrointestinal, particularmente colitis.
Las cefalosporinas pueden estar asociadas con una caída en la actividad de la protrombina. Los pacientes que están en riesgo son aquellos con insuficiencia renal o hepática, o con estado nutricional deficiente, así como los pacientes que reciben un tratamiento prolongado de la terapia antimicrobiana y pacientes previamente estabilizados con un tratamiento anticoagulante. El tiempo de protrombina debe ser monitoreado en pacientes con riesgo y debe administrarse vitamina K exógena como se indica.
Información para el paciente: Los pacientes deben ser informados que los medicamentos antibacterianos, como KEFLEX® 250 mg/5 mL suspensión y KEFLEX® 500 mg tabletas recubiertas sólo deben usarse para tratar infecciones bacterianas. No sirven para tratar infecciones virales (por ejemplo, el resfriado común). Cuando cefalexina para suspensión oral o cefalexina tabletas se prescriben para tratar una infección bacteriana, los pacientes deben ser informados de que a pesar de que es común sentirse mejor en las primeras etapas del tratamiento, el medicamento se debe tomar exactamente como se indica. Saltarse las dosis o no completar el tratamiento completo puede (1) disminuir la eficacia del tratamiento inmediato y (2) aumentar la probabilidad de que las bacterias desarrollen resistencia y no se puedan tratar con KEFLEX® 250 mg/5 mL suspensión, KEFLEX® 500 mg tabletas recubiertas u otros medicamentos antibacterianos en el futuro.
La diarrea es un problema común causado por los antibióticos que normalmente finaliza cuando se suspende el antibiótico. A veces, después de iniciar el tratamiento con antibióticos, los pacientes pueden desarrollar heces acuosas y sanguinolentas (con o sin calambres en el estómago y fiebre), incluso de dos o más meses después de haber tomado la última dosis del antibiótico. Si esto ocurre, los pacientes deben comunicarse con su médico tan pronto como sea posible.
DOSIS Y ADMINISTRACIÓN:
Cefalexina se administra por vía oral.
Adultos: Los intervalos de dosis de adultos son de 1 a 4 g diarios en dosis divididas.
Dosis fuertes de 333 mg y 750 mg deben ser administrados de tal manera que la dosis diaria está dentro de 1 a 4 gramos por día. La dosis habitual para adultos es 250 mg cada 6 horas. Para las siguientes infecciones: faringitis estreptocócica, infecciones de la piel y sus estructuras, cistitis no complicada en pacientes mayores de 15 años de edad, una dosis de 500 mg se puede administrar cada 12 horas. Se debe continuar la terapia de cistitis por 7 a 14 días. Para infecciones más graves o aquellas causadas por microorganismos menos sensibles, pueden ser necesarias dosis mayores. Si se requieren dosis diarias de cefalexina superior a 4 g, cefalosporinas parenterales se deben considerar en dosis adecuadas.
Pacientes pediátricos: La dosis diaria habitual recomendada para los pacientes pediátricos es de 25 a 50 mg / kg en dosis divididas. Para la faringitis estreptocócica en pacientes mayores de 1 año de edad y para infecciones de la piel y sus estructuras, la dosis diaria total puede ser dividida y administrada cada 12 horas.
|
KEFLEX® Suspensión |
|
|
Peso |
250 mg/5 ml |
|
10 kg (22 lb) |
1/4 a 1/2 cucharitas cuatro veces al día |
|
20 kg(44 lb) |
1/2 a 1 cucharitas cuatro veces al día |
|
40 kg(88 lb) |
1 a 2 cucharitas cuatro veces al día |
|
Peso |
250 mg/5 ml |
|
10 kg (22 lb) |
1/2 a 1 cucharitas dos veces al día |
|
20 kg(44 lb) |
1 a 2 cucharitas dos veces al día |
|
40 kg(88 lb) |
2 a 4 cucharitas dos veces al día |
En infecciones severas, se puede doblar la dosis.
En el tratamiento de la otitis media, los estudios clínicos han demostrado que se requiere una dosis de 75 a 100 mg/kg/día en 4 dosis divididas.
En el tratamiento de las infecciones por estreptococos ß-hemolíticos, una dosis terapéutica de cefalexina debe administrarse durante al menos 10 días.
KEFLEX® 250 mg/5 mL Suspensión no necesita reconstituir. Antes de utilizar
KEFLEX® 250 mg/5 mL Suspensión agítese bien. Mantener el frasco bien tapado.
Consérvese a una temperatura no mayor de 30 °C.
Periodo de validez: No usar el producto pasada la fecha de vencimiento declarada en la etiqueta y en el estuche.
Elaborado por:
Antibióticos do Brasil Ltda. - Brasil
Importado por:
FARMAKONSUMA S.A.
SOBREDOSIS:
Signos y síntomas: Los síntomas de sobredosis oral pueden incluir náusea, vómito, malestar epigástrico, diarrea y hematuria. Si se presentan otros síntomas, probablemente sea secundario a un estado de la enfermedad subyacente, una reacción alérgica o toxicidad debida a la ingestión de un segundo medicamento.
Tratamiento: En el manejo de la sobredosificación, considere la posibilidad de sobredosis por múltiples medicamentos, interacción entre los fármacos, y la cinética de drogas inusuales en su paciente.
A menos que de 5 a 10 veces la dosis normal de cefalexina se haya ingerido, la descontaminación gastrointestinal no debería ser necesaria.
Proteja las vías respiratorias del paciente y debe haber apoyo de ventilación y perfusión. Controlar y mantener meticulosamente dentro de unos límites aceptables, los signos vitales del paciente, gases sanguíneos, electrolitos séricos, etc. La absorción de fármacos desde el tracto gastrointestinal puede disminuirse con la administración de carbón activado, que, en muchos casos, es más efectivo que el vómito o lavado; considerar carbón activado en lugar de o además del vaciado gástrico.
Dosis repetidas de carbón activado con tiempo, pueden acelerar la eliminación de algunos medicamentos que han sido absorbidos. Proteja las vías respiratorias del paciente cuando emplee el vaciamiento gástrico o el carbón.
Diuresis forzada, diálisis peritoneal, hemodiálisis o hemoperfusión con carbón activado no han establecido el beneficio para una sobredosis de cefalexina, sin embargo, sería muy poco probable que uno de estos procedimientos sean indicados.
La dosis letal media oral de cefalexina en ratas es > 5000 mg/kg.
DESCRIPCIÓN:
La cefalexina es un antibiótico cefalosporínico semisintético destinado para la administración oral. Es 7-(D-α-amino-α-fenilacetamido)-3-metil-3-cefem-4-carboxílico, monohidrato.
La cefalexina tiene la siguiente fórmula estructural.
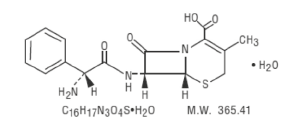
El núcleo de la cefalexina se relaciona con la de otros antibióticos de cefalosporinas.
El compuesto es un zwitterion, es decir, la molécula contiene tanto un grupo básico y un grupo ácido. El punto isoeléctrico de la cefalexina en agua es de aproximadamente 4,5 a 5.
La forma cristalina de la cefalexina que está disponible es un monohidrato.
Es un sólido cristalino blanco que tiene un sabor amargo. Su solubilidad en agua es baja a temperatura ambiente; 1 o 2 mg/ml se pueden disolver fácilmente, pero concentraciones más altas se obtienen con mayor dificultad.
Las cefalosporinas difieren de penicilinas en la estructura del sistema de anillo bicíclico. La cefalexina tiene un grupo D-fenilglicil como sustituyente en la posición 7-amino y un grupo metilo no sustituido en la posición 3.
Cada 5 ml de KEFLEX® Suspensión oral contendrá cefalexina monohidrato, equivalente a 250 mg de cefalexina base. Cada Tableta recubierta de KEFLEX® contiene cefalexina monohidrato, equivalente a 500 mg de cefalexina base.
Mecanismo de acción.
Farmacología humana: La cefalexina es resistente a los ácidos y puede ser administrada con o entre las comidas. Es absorbida rápidamente tras la administración oral.
Después de haber administrado dosis de 250 mg, 500 mg y 1 g, se obtuvieron a la hora, concentraciones séricos máximas de aproximadamente 9, 18, y 32 mcg/ml, respectivamente. Existen concentraciones séricas medibles hasta por 6 horas después de su administración. La cefalexina se excreta en la orina por filtración glomerular y secreción tubular. Los estudios demostraron que más del 90% del fármaco se excreta sin cambios en la orina dentro de las 8 horas.
Durante este período las concentraciones urinarias pico después de administrar 250 mg, 500 mg y 1 g dosis fueron de aproximadamente 1000, 2200, y 5000 mcg / ml, respectivamente.
Microbiología: Los estudios “in vitro” demuestran que las cefalosporinas son bactericidas porque inhiben la síntesis de la pared celular. La cefalexina ha demostrado ser activa contra la mayoría de cepas de los siguientes microorganismos, tanto in vitro como en infecciones clínicas que se describe en la sección de indicaciones.
Aerobios, Gram-positivos:
• Staphylococcus aureus (incluyendo cepas productoras de penicilinasa)
• Streptococcus pneumoniae (cepas susceptibles a la penicilina)
• Streptococcus pyogenes.
Aerobios, Gram-negativos:
• Escherichia coli
• Haemophilus influenzae
• Klebsiella pneumoniae
• Moraxella (Branhamella) catarrhalis
• Proteus mirabilis
Nota: La mayoría de las cepas de enterococos (Enterococcus faecalis [anteriormente Streptococcus faecalis]) y los estafilococos resistentes a meticilina son resistentes a las cefalosporinas incluyendo cefalexina. No es activa contra la mayoría de las cepas de las especies de Entrobacter, Morganella morganii (anteriormente Proteus morganii) y Proteus vulgaris.
No es activa contra las especies de Pseudomonas o Acinetobacter calcoaceticus (anteriormente especies Mima y Herellea).