INFLAMMIDE HFA
BUDESONIDA
Aerosol para inhalación
Aerosol para inhalación, 200 mcg
COMPOSICIÓN:
Principio activo: Budesonida.
Una dosis liberada contiene 200 microgramos de budesonida.
Excipientes: (ácido oleico, etanol absoluto, propelente HFA 134a) c.s.p.
INDICACIONES TERAPÉUTICAS:
Asma bronquial, en pacientes que previamente no hayan respondido a terapia con broncodilatadores y/o antialérgicos.
DATOS FARMACÉUTICOS:
Incompatibilidades: No procede
Período de validez: Período de validez del producto envasado para la venta: 2 años.
“No consumir el producto una vez alcanzada la fecha de vencimiento indicada en los rotulados”.
Precauciones especiales de conservación: Almacénese a temperatura no mayor de 30 °C.
Al igual que con otros aerosoles, el efecto terapéutico puede disminuir si el envase aerosol se enfría.
Proteger de la luz solar directa y no congelar. El envase aerosol no debe ser perforado, roto o quemado aún cuando aparentemente esté vacío.
“Consulte a su médico o farmacéutico, según proceda, para cualquier aclaración sobre la utilización del producto”.
Venta con receta médica
Manténgase fuera del alcance de los niños
PROPIEDADES FARMACOLÓGICAS:
Propiedades farmacodinámicas:
Grupo terapéutico: R03BA02.
Mecanismo de acción: La Budesonida es un corticosteroide no halogenado eficaz en el tratamiento del asma debido a su capacidad antiinflamatoria.
Efectos farmacodinámicos: En estudios farmacológicos y clínicos la Budesonida ha demostrado poseer, para una amplia gama de dosis, una favorable relación entre actividad antiinflamatoria local y efectos secundarios sistémicos de tipo corticoide. Ello se debe a que la Budesonida se inactiva rápidamente en el hígado tras su absorción sistémica. Por otra parte, la Budesonida ejerce un efecto antianafiláctico y antiinflamatorio que se manifiesta disminuyendo la broncoconstricción producida por las reacciones alérgicas, tanto inmediatas como retardadas. También se ha demostrado, que la Budesonida disminuye la reactividad respiratoria a la histamina y metacolina en pacientes hiperreactivos.
Propiedades farmacocinéticas:
Absorción: La Budesonida administrada por vía inhalatoria oral es absorbida rápidamente por la mucosa y parénquima pulmonar.
Distribución: Tras la administración por vía inhalatoria, la Budesonida se detecta rápidamente en sangre, lo que indica que el fármaco se absorbe de forma intacta a través del tracto respiratorio.
Metabolismo o Biotransformación: Esta elevada concentración plasmática inicial también indica un mínimo metabolismo del medicamento en el pulmón.
La semivida plasmática de la Budesonida intacta es de 2,0 ± 0,2 horas, valor análogo al encontrado después de la administración intravenosa del fármaco (2,8 ± 1,1 horas).
La Budesonida sufre un extenso metabolismo de primer paso en el hígado mediante una biotransformación oxidativa y reductora dando lugar a dos metabolitos biológicamente inactivos, responsables de que la acción sistémica de la Budesonida sea muy baja. La unión a proteínas plasmáticas es de un 88,0%.
Eliminación: Los estudios de eliminación realizados en humanos, administrando 3H-Budesonida por vía inhalatoria, demuestran una excreción mayoritaria de radiactividad por vía urinaria (32%) y heces (15%).
CONTRAINDICACIONES:
INFLAMMIDE® HFA está contraindicado en pacientes con historial de hipersensibilidad al principio activo o a alguno de los excipientes.
FERTILIDAD, EMBARAZO Y LACTANCIA:
Embarazo: No hay evidencia suficiente acerca de la seguridad en mujeres embarazadas. La administración de corticoides a animales preñados puede causar anormalidades en el desarrollo del feto, incluyendo paladar hendido y retraso del crecimiento intrauterino. En consecuencia existe un riesgo, aunque pequeño, de que aparezcan tales efectos en el feto humano.
El uso de Budesonida por vía inhalatoria durante el embarazo en humanos requiere que los beneficios sean sopesados frente a los posibles riesgos.
Lactancia: No se han realizado estudios específicos acerca de la transferencia a la leche en animales lactantes. El uso de Budesonida en madres durante el período de lactancia requiere sopesar los beneficios terapéuticos del fármaco frente a los posibles riesgos para la madre y el niño.
EFECTOS SOBRE LA CAPACIDAD PARA CONDUCIR Y UTILIZAR MÁQUINAS:
La influencia de INFLAMMIDE® HFA sobre la capacidad para conducir y utilizar máquinas es nula o insignificante.
REACCIONES ADVERSAS:
Ocasionalmente se han descrito casos de ligera irritación de la garganta, tos y ronquera. Asimismo, se han dado algunos casos de sobreinfección por Candida en la cavidad orofaríngea. En la mayoría de los casos responde a una terapia antifúngica tópica, sin necesidad de interrumpir el tratamiento con Budesonida. En casos excepcionales se han descrito reacciones alérgicas cutáneas (urticaria, rash, dermatitis) asociadas con la utilización de corticosteroides tópicos.
Raramente puede aparecer nerviosismo, inquietud, depresión, alteraciones del comportamiento y hematomas cutáneos. En raras ocasiones, con glucocorticoides inhalados se pueden producir signos o síntomas del efecto sistémico de los glucocorticoides, incluyendo hipofunción de la glándula suprarrenal y reducción de la velocidad de crecimiento, dependiendo probablemente de la dosis, tiempo de exposición, exposición concomitante y previa a glucocorticoides, y sensibilidad individual.
Trastornos psiquiátricos: Hiperactividad psicomotora, trastornos del sueño, ansiedad, depresión, agresividad y cambios de humor (principalmente en niños). Frecuencia desconocida.
Deberá tenerse en cuenta la posibilidad de aparición de broncoespasmo paradójico con un aumento de la sibilancia tras la administración. Si ocurriera, suspender inmediatamente la administración e instaurar una terapia alternativa.
“Por favor comunicarse con su médico o farmacéutico en caso se presente cualquier reacción adversa que no esté descrita en este inserto”.
INTERACCIÓN CON OTROS MEDICAMENTOS Y OTRAS FORMAS DE INTERACCIÓN:
La única interacción descrita hasta el momento es la posible influencia de la cimetidina sobre la farmacocinética y la farmacodinamia de la Budesonida tras la administración concomitante oral e intravenosa, si bien es de escasa importancia clínica.
Se desconoce la posible interacción con otros medicamentos.
DATOS PRECLÍNICOS SOBRE SEGURIDAD:
La Budesonida, administrada oralmente a roedores, posee una DL50 superior a 1000 mg/kg; administrada a ratones por vía subcutánea, la DL50 de la Budesonida es superior a 50 mg/kg. En administración subcutánea a ratas durante un período de 6 meses con dosis elevadas de hasta 80 mcg/kg/día, la Budesonida induce los cambios característicos del tratamiento prolongado con corticosteroides, tales como retraso del crecimiento, inmunosupresión, alteraciones hepáticas y retención urinaria.
ADVERTENCIAS Y PRECAUCIONES ESPECIALES DE EMPLEO:
Estos preparados deben administrarse con gran precaución en pacientes con tuberculosis pulmonar o con infecciones fúngicas o virales de las vías respiratorias.
El paso de un tratamiento oral con corticosteroides a un tratamiento con Budesonida, debe efectuarse con especial precaución, debido principalmente a la lenta normalización de la función hipotálamo-hipofisario- adrenal, previamente alterada por la corticoterapia oral. Esta normalización puede tardar algunos meses en alcanzarse. Durante este cambio de medicación, los pacientes pueden recuperar la sintomatología primitiva (rinitis, eccema) o experimentar cansancio, cefaleas, dolores musculares o articulares y ocasionalmente náuseas y vómitos. En estos casos deberá procederse a un tratamiento sintomático complementario.
Los corticosteroides inhalados pueden provocar efectos sistémicos, en especial a dosis altas prescritas durante períodos prolongados. No obstante, es mucho menos probable que se produzcan estos efectos que cuando se utilizan los corticosteroides orales y pueden variar dependiendo de cada paciente y entre diferentes preparaciones de corticosteroides.
Los posibles efectos sistémicos pueden incluir síndrome de Cushing, aspecto Cushingoide, supresión suprarrenal, retraso del crecimiento en niños y adolescentes, disminución de la densidad mineral ósea, cataratas, glaucoma y, más raramente, una variedad de efectos psicológicos o de comportamiento tales como hiperactividad psicomotora, trastornos del sueño, ansiedad, depresión o agresividad (especialmente en niños). Por tanto, es importante que la dosis del corticosteroide inhalado se ajuste a la dosis más baja capaz de mantener un control eficaz del proceso asmático.
Los pacientes que han sido tratados con esteroides sistémicos durante largos períodos de tiempo o altas dosis pueden tener supresión cortico-suprarrenal. Deberá vigilarse regularmente la función cortico-suprarrenal de estos pacientes y reducir cuidadosamente la dosis de esteroides sistémicos.
Estos preparados no están indicados para el tratamiento de la crisis aguda asmática. El tratamiento con Budesonida no debe suspenderse repentinamente.
Advertencia: El uso de estos preparados por los deportistas puede establecer un resultado analítico de control de dopaje como positivo.
Este medicamento contiene 0.31% de etanol (alcohol), que se corresponde con una cantidad de 0.1535 mg/dosis.
POSOLOGÍA Y FORMA DE ADMINISTRACIÓN:
La dosificación de INFLAMMIDE® HFA debe ser individualizada. Al inicio del tratamiento con glucocorticoides inhalados, durante períodos de asma grave y mientras se reduce o suspende el tratamiento con glucocorticoides orales la dosis debe ser:
Población pediátrica:
• Niños de 2-7 años: 200-400 mcg diarios, divididos en 2-4 administraciones.
• Niños a partir de 7 años: 200-800 mcg diarios, divididos en 2-4 administraciones.
• Adultos: 200-1600 mcg diarios, divididos en 2-4 administraciones.
Forma de administración:
1. Comprobar que el aerosol se encuentra bien ensamblado al adaptador bucal de plástico. Agitar el conjunto y retirar la tapa blanca.
2. Sostener el frasco en posición invertida entre los dedos pulgar e índice. Introducir la boquilla en la boca, apretando los labios alrededor de la misma.
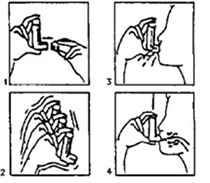
3. Realizar una espiración profunda (expulsar el aire por la nariz) y seguidamente efectuar una inspiración a fondo por la boca, presionando al mismo tiempo el frasco entre los dedos y provocando una sola descarga.
4. Retirar el aparato de la boca y retener el aire inspirado unos segundos. Espirar lentamente y guardar el frasco, colocando la tapa otra vez.
Optativamente pueden utilizarse cámaras de inhalación para conseguir un mejor aprovechamiento de la dosis y facilitar la llegada del medicamento a los pulmones.
Una vez obtenidos los efectos clínicos deseados, la dosis de mantenimiento debe ser gradualmente reducida hasta la cantidad mínima necesaria para el control de los síntomas.
• En pacientes no dependientes de corticoides orales: un tratamiento con dosis recomendadas normalmente manifiesta los resultados al cabo de 7 días. Sin embargo, en ciertos pacientes con excesiva secreción mucosa bronquial, es recomendable administrar simultáneamente, durante una o dos semanas, un corticosteroide oral cuya dosis se reducirá gradualmente hasta continuar solamente con la terapia a base de Budesonida. Las exacerbaciones asmáticas producidas por infecciones bacterianas deben controlarse con una terapia antibiótica y posiblemente incrementando la dosis de Budesonida, o si es necesario, administrando corticosteroides sistémicos.
• En pacientes dependientes de corticoides orales: el paso de un tratamiento con esteroides orales al tratamiento con Budesonida debe producirse cuando el paciente se encuentra en una fase estable.
Durante unos 10 días se administrará una dosis elevada de Budesonida en combinación con el corticoide oral utilizado hasta entonces. Posteriormente, se podrá ir reduciendo la dosis oral de corticoide (p. ej. 2.5 mg de prednisolona o equivalente, cada mes) hasta el mínimo nivel posible. En muchos casos, puede retirarse por completo el corticoide oral y dejar al paciente bajo el tratamiento exclusivo con Budesonida.
Después de cada dosificación el paciente se lavará la boca con agua.
SOBREDOSIS:
Si en alguna circunstancia aparecieran síntomas sugestivos de hipercorticismo, como edema, cara de luna llena, etc., se deberá corregir el desequilibrio electrolítico correspondiente, mediante el empleo de diuréticos que no afecten al potasio, como la espironolactona y el triamtereno. La administración por vía oral o inhalatoria de dosis elevadas de corticoides durante un período prolongado de tiempo puede conducir a la supresión del eje hipotalámico-hipofisario-corticosuprarrenal.
INFORMACIÓN PARA USUARIOS:
Inflammide® HFA
BUDESONIDA
200 mcg/dosis
Aerosol para inhalación
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
Si tiene alguna duda, consulte a su médico, farmacéutico o enfermero.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico, farmacéutico o enfermero, incluso si se trata de efectos adversos que no aparecen en este prospecto.
Contenido del prospecto:
1. Qué es INFLAMMIDE® HFA 200mcg/dosis Aerosol para inhalación y para qué se utiliza.
2. Qué necesita saber antes de empezar a usar INFLAMMIDE® HFA 200mcg/dosis Aerosol para inhalación.
3. Cómo usar INFLAMMIDE® HFA 200mcg/dosis Aerosol para inhalación.
4. Posibles efectos adversos.
5. Conservación de INFLAMMIDE® HFA 200mcg/dosis Aerosol para inhalación.
6. Contenido del envase e información adicional.
Qué es INFLAMMIDE® HFA 200 mcg/dosis Aerosol para inhalación y para qué se utiliza:
La Budesonida es un corticosteroide no halogenado eficaz en el tratamiento del asma debido a su capacidad antiinflamatoria.
Está indicado en: Tratamiento del asma bronquial, en pacientes que previamente no hayan respondido a terapia con broncodilatadores y/o antialérgicos.
Qué necesita saber antes de empezar a usar INFLAMMIDE® HFA 200 mcg/dosis Aerosol para inhalación: No use INFLAMMIDE® HFA 200 mcg/dosis Aerosol para inhalación:
Si es alérgico a la Budesonida o a cualquiera de los demás componentes de este medicamento.
Advertencias y precauciones: Consulte a su médico, farmacéutico o enfermero antes de empezar a usar INFLAMMIDE® HFA 200 mcg/dosis Aerosol para inhalación.
Tenga especial cuidado con INFLAMMIDE® HFA 200 mcg/dosis Aerosol para inhalación
- Si padece infecciones fúngicas o virales de las vías respiratorias o tuberculosis pulmonar.
- El paso de un tratamiento oral con corticosteroides a un tratamiento con Budesonida, debe efectuarse con especial precaución, debido principalmente a la lenta normalización de la función hipotálamo-pituitaria-adrenal, previamente alterada por la corticoterapia oral.
Esta normalización puede tardar algunos meses en alcanzarse. Durante este cambio de medicación, Ud. puede recuperar la sintomatología primitiva (rinitis,eccema) o experimentar cansancio, cefaleas, dolores musculares o articulares y ocasionalmente náuseas y vómitos. En estos casos deberá procederse a un tratamiento sintomático complementario.
- Esta terapia es únicamente preventiva, no está indicada para el tratamiento de la crisis aguda asmática. El tratamiento con Budesonida no debe suspenderse repentinamente.
Información importante sobre alguno de los componentes de INFLAMMIDE® HFA 200 mcg/dosis Aerosol para inhalación:
Se informa a los deportistas que este medicamento contiene un componente que puede establecer un resultado analítico de control del dopaje como positivo.
Embarazo, lactancia y fertilidad: Si está embarazada o en período de lactancia, o cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico o farmacéutico antes de utilizar este medicamento.
Los estudios en animales han demostrado que los corticosteroides pueden producir distintos tipos de malformaciones fetales, aunque tales efectos no parecen extrapolables al hombre. Por otra parte, no existen datos demostrativos de un posible paso de la Budesonida a la leche materna durante la lactancia. A pesar de estas consideraciones, por razones de seguridad, se desaconseja su empleo durante el embarazo y la lactancia.
Conducción y uso de máquinas: No se han descrito efectos sobre la capacidad de conducción y uso de máquinas.
Toma de INFLAMMIDE® HFA 200 mcg/dosis Aerosol para inhalación con otros medicamentos:
Informe a su médico o farmacéutico si está tomando o utilizando, ha tomado o utilizado recientemente o podría tener que tomar o utilizar cualquier otro medicamento.
Se desconoce la posible interacción con otros medicamentos.
INFLAMMIDE® HFA 200 mcg/dosis Aerosol para inhalación contiene: Este medicamento contiene 0.31% de etanol (alcohol), esta pequeña cantidad se corresponde con 0.1535 mg/dosis.
Cómo usar INFLAMMIDE® HFA 200 mcg/dosis Aerosol para inhalación:
Recuerde usar su medicamento.
Instrucciones para un uso adecuado: Si estima que la acción de INFLAMMIDE® HFA 200 mcg/dosis Aerosol para inhalación es demasiado fuerte o débil, comuníqueselo.
Siga exactamente las instrucciones de administración de INFLAMMIDE® HFA 200 mcg/dosis Aerosol para inhalación indicadas por su médico o farmacéutico. En caso de duda, consulte de nuevo a su médico o farmacéutico.
INFLAMMIDE® HFA 200 mcg/dosis aerosol para inhalación se administra por vía inhalatoria.
A menos que su médico le haya dado otras indicaciones distintas siga la siguiente posología: La dosificación debe ser individualizada.
Uso en niños y adolescentes:
• Niños de 2-7 años: 200-400 mcg diarios, divididos en 2-4 administraciones.
• Niños a partir de 7 años: 200-800 mcg diarios, divididos en 2-4 administraciones.
Uso en adultos:
• Adultos: 200-1600 mcg diarios, divididos en 2-4 administraciones.
Una vez obtenidos los efectos clínicos deseados, la dosis de mantenimiento debe ser gradualmente reducida hasta la cantidad mínima necesaria para el control de los síntomas.
- En pacientes no dependientes de corticoides orales: un tratamiento con dosis recomendadas normalmente manifiesta los resultados al cabo de 7 días.
Sin embargo, en ciertos pacientes con excesiva secreción mucosa bronquial, es recomendable administrar simultáneamente, durante una o dos semanas, un corticosteroide oral cuya dosis se reducirá gradualmente hasta continuar solamente con terapia a base de Budesonida. Las exacerbaciones asmáticas producidas por infecciones bacterianas deben controlarse con una terapia antibiótica y posiblemente incrementando la dosis de Budesonida, o si es necesario, administrando corticosteroides sistémicos.
- En pacientes dependientes de corticoides orales: el paso de un tratamiento con esteroides orales al tratamiento con Budesonida debe producirse cuando el paciente se encuentra en una fase estable. Durante unos 10 días se administrará una dosis elevada de Budesonida en combinación con el corticoide oral utilizado hasta entonces. Posteriormente, se podrá ir reduciendo la dosis oral de corticoide (p. ej. 2.5 mg de prednisona o equivalente, cada mes) hasta el mínimo nivel posible. En muchos casos, puede retirarse por completo el corticoide oral y dejar al paciente bajo el tratamiento exclusivo con Budesonida. Sin embargo, en caso de que el paciente experimente desasosiego y en situaciones de estrés físico tales como infecciones agudas, tratamientos o intervenciones quirúrgicas debe restaurarse el tratamiento corticoide oral adicional. Las exacerbaciones agudas acompañadas de un aumento de la viscosidad mucosa, taponamiento mucoso, requieren tratamiento complementario durante un corto período de tiempo con corticoides orales.
Después de cada dosificación el paciente se lavará la boca con agua.
Instrucciones para la correcta administración del preparado: Antes de usar el medicamento, comprobar la fecha de caducidad.

a. Quítese la tapa (fig.1). En caso de que sea un inhalador nuevo o no se haya utilizado durante varios días, agitar el aerosol (fig. 2) y efectuar una pulsación para asegurar el buen funcionamiento del inhalador. En caso de que el inhalador se utilice regularmente pase a las instrucciones siguientes:
b. Agite el inhalador (fig. 2).
c. Elimine de sus pulmones la máxima cantidad de aire posible.
d. Adapte el aerosol a su boca según la posición que se indica en el dibujo (fig. 3).
e. Haga una inspiración lo más profunda posible.
Debe oprimir, según las flechas del dibujo (fig. 4), el aparato mientras está haciendo esta inspiración.
f. Retire el aerosol de su boca y procure retener el aire en sus pulmones durante unos segundos.
g. Debe lavarse periódicamente el pulsador-adaptador oral del aerosol. Para ello, retire el pulsador del aerosol y límpielo con un trapo o bien con un pañuelo de papel.
h. Guardar con la tapa colocada y para protegerlo del polvo y de la suciedad.
El médico debe comprobar que el paciente sabe usar el inhalador y sincroniza la inspiración con la pulsación.
Si usa más INFLAMMIDE® HFA 200 mcg/dosis Aerosol para inhalación del que debiera: Es importante que tome su dosis tal y como le ha indicado su médico. No debe aumentar ni disminuir su dosis sin supervisión médica.
Aunque no cabe esperar ningún tipo de síntoma tóxico por sobredosis o ingestión accidental, si usted ha inhalado más INFLAMMIDE® HFA 200 mcg/dosis Aerosol para inhalación de la que debiera, consulte inmediatamente a su médico o farmacéutico.
Si en alguna circunstancia muy especial se observasen síntomas de edema, hinchazón del rostro o cara de luna llena, etc., deberá ponerlo en conocimiento de su médico para que se apliquen las medidas oportunas.
Si olvidó usar INFLAMMIDE® HFA 200 mcg/dosis Aerosol para inhalación: No use una dosis doble para compensar las dosis olvidadas.
Posibles efectos adversos: Al igual que todos los medicamentos, INFLAMMIDE® HFA 200 mcg/dosis Aerosol para inhalación puede producir efectos adversos, aunque no todas las personas los sufran.
Ocasionalmente se han descrito casos de ligera irritación de la garganta, tos y ronquera. Asimismo, se han dado casos de sobre infección por Candida en la cavidad bucal, faríngea y laríngea. En la mayoría de los casos responde a una terapia antifúngica tópica, sin necesidad de interrumpir el tratamiento con Budesonida. En casos excepcionales se han descrito reacciones alérgicas cutáneas (urticaria, dermatitis) asociadas con la utilización de corticosteroides tópicos.
Deberá tenerse en cuenta la posibilidad de aparición de broncoespasmo paradójico con un aumento de la sibilancia “pitidos” tras la administración. Si ocurriera, suspender inmediatamente la administración e instaurar una terapia alternativa.
Frecuencia desconocida pero también pueden aparecer: Alteraciones del sueño, depresión o sensación de preocupación, inquietud, nerviosismo, excitabilidad o irritabilidad. Estos efectos son más probables que aparezcan en niños.
Si experimenta efectos adversos, consulte a su médico o farmacéutico o enfermero, incluso si se trata de efectos adversos que no aparecen en este prospecto.
Conservación de INFLAMMIDE® HFA 200 mcg/dosis Aerosol para inhalación.
Mantener este medicamento fuera de la vista y del alcance de los niños.
Conservar por debajo de 30 ºC. Proteger de la luz solar directa y no congelar ni enfriar. El envase aerosol no debe ser perforado, roto o quemado aún cuando aparentemente esté vacío.
No utilice este medicamento después de la fecha de caducidad que aparece en la etiqueta después de FV: La fecha de vencimiento es el último día del mes que se indica.
Los medicamentos no se deben tirar por los desagües ni a la basura. En caso de duda pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que no necesita. De esta forma ayudará a proteger el medio.
Contenido del envase e información adicional:
Composición de INFLAMMIDE HFA 200mcg/dosis Aerosol para inhalación.
Principio activo: Budesonida
Una dosis liberada contiene 200 microgramos de budesonida.
Excipientes: (ácido oleico, etanol absoluto, propelente HFA 134a) c.s.p.
Venta con receta médica
Manténgase fuera del alcance de los niños
Importado por:
BOEHRINGER INGELHEIM PERÚ S.A.C
RUC: 20523163320 Tel: (01) 412-5000
Dir. Técnico Q.F. Jesús Peña