
TRADOXIL D
DICLOFENACO SÓDICO, TRAMADOL
Tabletas
1 Caja, 10 Tabletas, 25/25 mg
1 Caja, 20 Tabletas, 25/25 mg
1 Caja, 30 Tabletas, 25/25 mg
COMPOSICIÓN:
Composición cualicuantitativa
Cada TABLETA contiene:
Diclofenaco sódico 25.00 mg
Tramadol Clorhidrato 25.00 mg
Excipientes c.s.p.
Lista de excipientes:
Celulosa Microcristalina
Lactosa Monohidrato
Almidón de Maíz Pregelatinizado
Croscarmelosa Sódica
Dióxido de Silicio Coloidal
Estearato de Magnesio
Agua purificada
Forma farmacéutica: Tableta.
PRINCIPIO ACTIVO (S) / GRUPO FARMACOLÓGICO:
Estructura:
Diclofenaco sódico
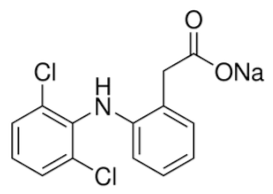
Nombre químico: Sodio; 2- [2- (2,6-dicloroanilino) fenil] acetato
Tramadol Clorhidrato
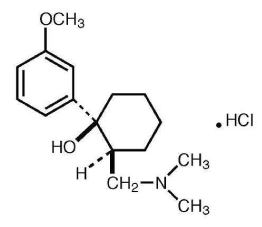
Nombre químico: 2-[(dimetilamino)metil]-1-(3-metoxifenil) ciclohexanol hidrocloruro.
Código ATC
M01AB05: M Sistema musculoesquelético.
M01 Productos antiinflamatorios y antirreumáticos. M01A Productos antiinflamatorios y antirreumáticos, no esteroideos.
M01AB Derivados de ácido acético y sustancias relacionadas.
M01AB05 Diclofenaco
N02AJ15: N Sistema nervioso.
N02 Analgésicos.
N02A Opioides.
N02AX Opioides en combinación con analgésicos no opioides.
N02AX02 Tramadol y otros analgésicos no opioides.
INDICACIONES TERAPÉUTICAS:
TRADOXIL D está indicado para el manejo del dolor inflamatorio de intensidad moderado a severo.
MECANISMO DE ACCIÓN:
Propiedades farmacológicas
Propiedades farmacodinámicas
Diclofenaco
Mecanismo de acción: Diclofenaco es un compuesto no esteroideo con marcas propiedades analgésicas, antiinflamatorias y antipiréticas. La inhibición de biosíntesis de prostaglandinas, que ha sido demostrada experimentalmente, se considera una importante característica para su mecanismo de acción. Las prostaglandinas desempeñan un papel esencial en la causalidad de la inflamación, del dolor y de la fiebre. Tramadol
Mecanismo de acción: Tramadol es un analgésico de acción central. Es un agonista puro, no selectiva sobre los receptores opioides µ, δ y κ, con mayor afinidad por los receptores µ. Otros mecanismos que contribuyen a su efecto analgésico son la inhibición de la recaptación neuronal de noradrenalina, así como la intensificación de la liberación de serotonina.
Propiedades farmacocinéticas
Diclofenaco
El diclofenaco es absorbido casi por completo en el tracto gastrointestinal, sin embargo, este tiene un extensivo primer paso en el hígado, en donde solo entre 50-60% lleva a la circulación sistémica sin sufrir ningún cambio. Se une en grandes proporciones, pero reversiblemente a las proteínas plasmáticas, principalmente a la albúmina. Las concentraciones plasmáticas son de 0.15 – 105 mcg/mL, esta se une de un 99 – 99.8% a las proteínas en estudios in vitro. El diclofenaco y sus metabolitos atraviesan la barrera placentaria en ratas y ratones. El metabolismo exacto de diclofenaco no ha sido completamente elucidado, pero la droga es rápidamente metabolizada por el hígado. Este presenta hidroxilación y una subsecuente conjugación con ácido glucurónico, ácido sulfúrico, taurina amida y otros ligandos biogénicos. La droga también se conjuga sin cambios. La hidroxilación del anillo aromático diclorofenil resulta en la formación de 4-hidroxidiclofenaco (metabolito principal) y 3-hidroxidiclofenaco, para luego ambos ser conjugados. También puede sufrir hidroxilación en el anillo fenilacetico y subsecuente conjugación para formar 5-hidroxidiclofenaco y 4,5-dihidroxidiclofenaco. Estudios en animales indican que 4-hidroxidiclofenaco tiene el 3% de potencia antiinflamatoria del diclofenaco y un 6 veces la potencia antiinflamatoria de la aspirina. 3-Hidroxidiclofenaco puede tener cierta actividad antiinflamatoria, pero otros metabolitos parecen ser farmacológicamente inactivos.
Tramadol
Absorbido inmediatamente luego de administración oral, pero está sujeto a efecto de primer paso.
La absorción no se ve alterada por la comida. Por lo que la biodisponibilidad luego de esto es de 70 a 75%. La unión a proteínas plasmáticas es cerca del 20%. El tramadol es metabolizado en N- y O-desmetilación mediante el citocromo P450 isoenzimas CYP34A y CYP2D6 y glucuronidación o sulfatación en el hígado. El metabolito O-desmetilado es farmacológicamente activo. Tramadol es excretado principalmente en la orina como sus metabolitos. Esta extensamente distribuido, atraviesa la placenta y aparece en pequeñas cantidades en la leche materna. La vida media es de aproximadamente 6 horas.
CONTRAINDICACIONES:
Hipersensibilidad al diclofenaco, tramadol u otro componente de la formula. Historia de asma, urticaria u otro tipo de reacciones alérgicas luego de tomar aspirina u otros antiinflamatorios no esteroideos.
Está contraindicado en pacientes con fallo cardíaco moderado a severo, enfermedad coronaria, enfermedad arterial periférica o enfermedad cerebrovascular. Debe ser utilizada con precaución en pacientes con factores de riesgo significantes para eventos cardiovasculares como hipertensión, hiperlipidemia, diabetes mellitus. Además, está contraindicado en pacientes con enfermedad renal o hepática severa.
Está contraindicado en sangrado gastrointestinal, úlcera gastrointestinal, enfermedad de Crohn, colitis ulcerosa, desórdenes de coagulación o tratamiento con anticoagulantes, porfiria, proctitis, en situaciones de intoxicaciones agudas por alcohol, hipnóticos, analgésicos, opioides u otros psicótropos. Pacientes en tratamiento con inhibidores de la MAO o que los hayan tomado durante los últimos 14 días y pacientes que presentan epilepsia no controlada adecuadamente con tratamiento para síndrome de abstinencia a opiáceos.
REACCIONES ADVERSAS:
Las reacciones adversas más frecuentes del TRADOXIL D son náuseas y mareos, las cuales se presentan en más del 10% de los pacientes. A nivel gastrointestinal se presentan a nivel gastrointestinal: úlceras pépticas, perforación o hemorragia gastrointestinal, en algunos casos mortales, especialmente en los ancianos. También se han notificado vómitos, diarrea, flatulencia, estreñimiento, constipación, dispepsia, dolor abdominal, melena, hematemesis, estomatitis ulcerosa, exacerbación de colitis ulcerosa y enfermedad de Crohn. Se ha observado menos frecuentemente la aparición de gastritis.
Las frecuencias se definen de la siguiente forma:
• Muy frecuentes: ≥1/10
• Frecuentes: ≥ 1/100, <1/10
• Poco frecuentes: ≥1/1.000, <1/100
• Raras: ≥1/10.000, <1/1.000
• Muy raras: <1/10.000
• Frecuencia no conocida: no puede estimarse a partir de los datos disponibles.
Trastornos de la sangre y del sistema linfático Muy raras: trombocitopenia, leucopenia, anemia (inclusive anemia hemolítica y anemia aplásica), agranulocitosis.
Trastornos del sistema inmunológico
Raras: hipersensibilidad anafiláctica y reacciones anafilactoides (inclusive hipotensión y shock).
Muy raras: angioedema (inclusive edema facial). Trastornos psiquiátricos
Muy raras: desorientación, depresión, insomnio, pesadillas, irritabilidad, trastornos psicóticos.
Trastornos cardíacos
Poco frecuentes: Relativas a la regulación cardiovascular (palpitaciones, taquicardia). Infarto de miocardio, insuficiencia cardíaca, palpitaciones, dolor torácico. Raras: Bradicardia.
Exploraciones complementarias
Raras: Presión arterial aumentada.
Trastornos vasculares
Poco frecuentes: relativas a la regulación cardiovascular (hipotensión postural o colapso cardiovascular.
Muy raras: hipertensión, vasculitis.
Trastornos del metabolismo y de la nutrición
Raras: alteraciones del apetito.
No conocida: hipoglucemia.
Trastornos respiratorios, torácicos y mediastínicos
Raras: depresión respiratoria, disnea.
Muy raras: neumonitis.
Tras la administración de dosis que sobrepasan considerablemente las dosis recomendadas y la administración concomitante con otros medicamentos con acción depresora central, puede presentarse una depresión respiratoria.
Trastornos del sistema nervioso
Muy frecuentes: mareos.
Frecuentes: cefaleas, somnolencia.
Raras: parestesia, temblor, convulsiones, contracciones involuntarias de los músculos, alteraciones de la coordinación, síncope, trastornos del habla.
Muy raras: meningitis, disgeusia, accidente cerebrovascular, ansiedad, alteraciones de la memoria.
Se han comunicado convulsiones tras la administración de dosis altas de tramadol o tras el tratamiento concomitante con otros medicamentos que puedan reducir el umbral convulsivo.
Trastornos psiquiátricos
Raras: alucinaciones, estado de confusión, alteraciones del sueño, delirio, ansiedad y pesadillas.
Pueden presentarse reacciones adversas psíquicas tras la administración de tramadol, cuya intensidad y naturaleza varían independientemente. Éstas incluyen alteraciones del estado de ánimo (generalmente euforia, ocasionalmente disforia), cambios en la actividad (generalmente disminuida, ocasionalmente aumentada), y alteraciones de la capacidad cognitiva y sensorial (como alteraciones en la percepción de la toma de decisiones). Pueden originarse síntomas del síndrome de abstinencia al medicamento, similares a los que aparecen tras la retirada síntomas del síndrome de abstinencia al medicamento, similares a los que aparecen tras la retirada de opioides: agitación, ansiedad, nerviosismo, insomnio, hipercinesia, temblor y síntomas gastrointestinales. Otros síntomas que han aparecido en muy raras ocasiones al interrumpir el tratamiento con tramadol son: ataques de pánico, ansiedad intensa, alucinaciones, parestesia, tinnitus y síntomas inusuales del sistema nervioso central (es decir, estado de confusión delirios, despersonalización, desrealización y paranoia).
Trastornos oculares
Raros: miosis, midriasis, visión borrosa.
Muy raras: diplopía.
Trastornos del oído y del laberinto
Frecuentes: vértigo.
Muy raras: tinnitus, alteración del oído.
Trastornos gastrointestinales
Frecuentes: náuseas, vómitos, diarrea, dispepsia, dolor abdominal, flatulencia, disminución del apetito, estreñimiento, sequedad de boca.
Poco frecuentes: arcadas, malestar gastrointestinal (sensación de presión en el estómago, hinchazón). Raras: Gastritis, hemorragia gastrointestinal, hematemesis, diarrea hemorrágica, melena, úlcera gástrica o intestinal (con o sin sangrado o perforación).
Muy raras: Colitis (inclusive colitis hemorrágica y exacerbación de la colitis ulcerativa o enfermedad de Crohn), estreñimiento, estomatitis, glositis, alteración esofágica, enfermedad diafragmática intestinal, pancreatitis.
Frecuencia no conocida: colitis isquémica.
Trastornos de la piel y del tejido subcutáneo Frecuentes: hiperhidrosis, erupción.
Poco frecuentes: reacciones dérmicas (por ejemplo, prurito, erupción cutánea, urticaria).
Muy raras: dermatitis ampollosas incluyendo el Síndrome de Stevens Johnson y la necrolisis epidérmica tóxica (Síndrome de Lyell), eczema, eritema, eritema multiforme, dermatitis exfoliativa, alopecia, reacción de fotosensibilidad, púrpura, púrpura de Henoch-Schonlein, prurito.
Trastornos musculoesqueléticos y del tejido conectivo
Raras: debilidad motora.
Trastornos hepatobiliares
Frecuentes: aumento de transaminasas séricas.
Raras: hepatitis con o sin ictericia, alteración hepática.
Casos asilados: hepatitis fulminante, necrosis hepática, insuficiencia hepática.
Trastornos renales y urinarios
Raras: trastornos de micción (disuria y retención urinaria).Muy raras: fallo renal aguda, hematuria, proteinuria, síndrome nefrótico, nefritis túbulo-intersticial, necrosis papilar renal.
Trastornos del sistema inmune
Raras: reacciones alérgicas (disnea, broncoespasmo, sibilancias, edema angioneurótico) y anafilaxia.
Trastornos generales y alteraciones en el lugar de administración
Frecuentes: fatiga.
Raras: edema.
Incompatibilidades: No refiere.
Efectos sobre la capacidad para conducir y manejar maquinara: Los analgésicos opioides (tramadol) pueden disminuir la capacidad mental y/o física necesaria para realizar tareas potencialmente peligrosas (por ejemplo, conducir un coche o utilizar máquinas), especialmente al inicio del tratamiento, tras un aumento de la dosis, tras un cambio de formulación y/o al administrarlo conjuntamente con otros medicamentos. Se debe advertir a los pacientes que no conduzcan ni utilicen máquinas si sienten somnolencia, mareo o alteraciones visuales mientras toman TRADOXIL D, o hasta que se compruebe que la capacidad para realizar actividades no queda afectada. Esto es aún más probable con la administración conjunta de alcohol y otros psicótropos.
INTERACCIONES MEDICAMENTOSAS Y DE OTRO GÉNERO:
Interacciones con otros medicamentos y otras formas de interacción: El diclofenaco se une en altas proporciones a las proteínas séricas, por lo que puede desplazar otros medicamentos. Estudios in vitro sugieren que el diclofenaco desplaza en cantidades mínimas a algunas drogas (prednisolona, salicilatos, tolbutamida, Warfarina), sin embargo, el diclofenaco puede ser desplazado por dosis altas de drogas ionizadas (salicilatos).
• Inhibidores de la enzima convertidora de angiotensina y antagonistas del receptor de angiotensina II: existe evidencia que el uso concomitante de estos medicamentos puede reducir la respuesta del agente antihipertensivo.
• Anticoagulantes: el uso concomitante está asociado a un mayor riesgo de sangrado gastrointestinal comparado con el uso de uno de los medicamentos por sí solo. Debido a que el diclofenaco puede causar sangrado gastrointestinal, inhibir la agregación plaquetaria y prologar el tiempo de coagulación, este debe ser utilizado con precaución en pacientes con uso concomitante de algún anticoagulante (por ejemplo, Warfarina).
• Diuréticos: pacientes que están siendo tratados con diuréticos tienen mayor riesgo de desarrollar enfermedad renal secundaria a la disminución de la presión sanguínea renal resultante de la inhibición de prostaglandinas producida por los AINES. En pacientes con hipertensión, el efecto antihipertensivo de la hidroclorotiazida es atenuado por el diclofenaco. El uso concomitante de diclofenaco y diuréticos ahorradores de potasio pueden estar asociados al aumento de concentraciones de potasio sérico.
• Agentes antiinflamatorios no esteroideos: su uso concomitante con diclofenaco aumenta el riesgo de efectos gastrointestinales serios.
• Metrotexato: toxicidad severa, algunas veces fatal ocurre con el uso concomitante de diclofenaco, la cual está asociada a la elevación de concentraciones séricas de metrotexato.
• Ciclosporina: el uso concomitante aumenta el efecto nefrotóxico de la ciclosporina, lo cual se debe a la inhibición de la prostaglandina renal.
• Litio: diclofenaco aumenta las concentraciones plasmáticas de litio y reduce la eliminación renal. El mecanismo involucrado en la disminución de la eliminación de litio es desconocido, pero ha sido atribuido a la inhibición de la síntesis de prostaglandinas la cual puede interferir en dicho proceso.
• Quinolona: la combinación de quinolonas y AINES puede incrementar el riesgo de estimulación del Sistema Nervioso Central, pero se requiere de estudios adicionales.
• Antiácidos: la administración hidróxido de aluminio y magnesio retrasa la absorción de diclofenaco.
• Otras drogas: el uso concomitante de drogas ulcero génicas como los corticosteroides durante tratamiento con AINES puede incrementar el riesgo de ulceración.
• No debe combinarse con inhibidores de la MAO. Se han observado interacciones con peligro para la vida y que afectan al sistema nervioso central, a la función respiratoria y cardiovascular, en pacientes tratados con inhibidores de la MAO en los 14 días previos a la utilización del opioide petidina. No se puede descartar que se produzcan las mismas interacciones con inhibidores de la MAO, durante el tratamiento con TRADOXIL D.
• La administración concomitante de TRADOXIL D con otros medicamentos depresores del sistema nervioso central, incluido el alcohol, puede potenciar los efectos sobre el sistema nervioso central.
• La administración concomitante o previa de carbamacepina (inductor enzimático) puede disminuir el efecto analgésico y reducir la duración de la acción.
• TRADOXIL D puede provocar convulsiones e incrementar el potencial de originar convulsiones de los inhibidores selectivos de la recaptación de serotonina (ISRS), inhibidores de la recaptación de serotonina/norepinefrina (IRSN), antidepresivos tricíclicos, antipsicóticos y otros medicamentos que reducen el umbral convulsivo (tales como bupropion, mirtazapina, tetrahidrocannabinol).
• El uso concomitante de TRADOXIL D y medicamentos serotoninérgicos tales como, inhibidores selectivos de la recaptación de serotonina (ISRS), inhibidores de la recaptación de serotonina/noradrenalina (IRSN), inhibidores de la MAO, antidepresivos tricíclicos y mirtazapina puede causar toxicidad por serotonina. Los síntomas del síndrome serotoninérgico pueden ser, por ejemplo: Clonus espontáneo, Clonus ocular inducible con agitación y diaforesis, Temblor e hiperreflexia, Hipertonía y temperatura corporal por encima de 38 ºC y clonus ocular inducible. La retirada de los medicamentos serotoninérgicos produce una rápida mejoría. El tratamiento depende de la naturaleza y gravedad de los síntomas.
• Otros medicamentos conocidos como inhibidores de la CYP34A, tales como ketoconazol, eritromicina, ritonavir, quinidina, paroxetina, fluoxetina, sertralina, amitriptilina e isoniacida pueden inhibir el metabolismo de tramadol (N-desmetilación) y probablemente también el metabolismo del metabolito activo O-desmetilado. No se ha estudiado la importancia clínica de este tipo de interacción. En un número limitado de estudios, la administración pre o posquirúrgica del antiemético ondansetrón (antagonista 5-HT3), aumentó el requerimiento de tramadol en pacientes con dolor posquirúrgico.
INFORMACIÓN COMPLEMENTARIA:
Fecha de revisión del texto y versión del documento: Junio 2019.
RECOMENDACIONES:
Advertencias y precauciones especiales de empleo: Múltiples preparaciones que contienen diclofenaco no deben ser usadas concomitantemente. Los pacientes deben ser informados que el diclofenaco como otros antiinflamatorios no esteroideos, no son libres de potenciales efectos adversos, incluyendo algunos que pueden causar incomodidad, y aquellos con efectos más severos (sangrado gastrointestinal, infarto agudo al miocardio, derrame cerebral) que pueden causar hospitalización y pueden incluso ser fatales.
Los antiinflamatorios no esteroideos aumentan el riesgo de eventos cardiovasculares trombóticos.
Para minimizar el riesgo potencial de efectos cardiovasculares se debe utilizar la dosis efectiva mínima y el tratamiento con la menor duración posible. Debe evitarse en pacientes con infarto agudo al miocardio reciente, a menos que los beneficios de la terapia sobrepasen el riesgo.
El uso concomitante con aspirina aumenta el riesgo de eventos gastrointestinales serios. El riesgo potencial de efectos gastrointestinales serios debe ser considerado en pacientes recibiendo tratamiento crónico. Este debe ser utilizado bajo supervisión en pacientes con historia de enfermedad gastrointestinal. Para minimizar el potencial riesgo de efectos adversos se debe utilizar la dosis efectiva mínima y el tratamiento con la menor duración posible.Debe ser utilizado con precaución en pacientes que pueden verse afectados con la prolongación de tiempo de coagulación (pacientes recibiendo tratamiento anticoagulante), debido a que puede inhibir la función plaquetaria.
Únicamente puede ser administrado con precaución especial en pacientes con dependencia a opioides, con traumatismo craneoencefálico, shock, nivel de consciencia disminuido de origen desconocido, trastornos en el centro respiratorio o de la función respiratoria, o con presión intracraneal elevada.
Debe administrarse con especial precaución en pacientes con depresión respiratoria, si se administran concomitantemente fármacos depresores del Sistema Nervioso Central, o si la dosis administrada es marcadamente superior a la recomendada, ya que no puede excluirse que se produzca depresión respiratoria.Se han comunicado convulsiones en pacientes tratados con tramadol en los niveles de dosis recomendados. Este riesgo puede aumentar si se supera el límite superior de la dosis máxima diaria recomendada (400mg). Adicionalmente, TRADOXIL D puede incrementar el riesgo de que el paciente presente crisis epilépticas si está recibiendo otra medicación que reduzca el umbral convulsivo. El tramadol solo debe ser utilizado en pacientes epilépticos o susceptibles de presentar crisis epilépticas, si las circunstancias lo requieren.
Puede desarrollarse tolerancia y dependencia psíquica y física, en especial después del uso a largo plazo. En los pacientes con tendencia al abuso o la dependencia de medicamentos, solo debe ser administrado durante períodos corto y bajo estricto control médico.
Cuando un paciente ya no necesite tratamiento con TRADOXIL D, puede ser aconsejable reducir de forma gradual la dosis para prevenir los síntomas de abstinencia.Metabolismo del CYP2D6
El tramadol es metabolizado por la enzima hepática CYP2D6. Si un paciente presenta una deficiencia o carencia total de esta enzima, es posible que no se obtenga un efecto analgésico adecuado. Los cálculos indican que hasta el 7 % de la población de raza blanca puede presentar esta deficiencia. Sin embargo, si el paciente es un metabolizador ultrarápido, existe el riesgo de desarrollar efectos adversos de toxicidad por opioides, incluso a las dosis prescritas de forma habitual. Los síntomas generales de la toxicidad por opioides son confusión, somnolencia, respiración superficial, pupilas contraídas, náuseas, vómitos, estreñimiento y falta de apetito. En los casos graves, esto puede incluir síntomas de depresión circulatoria y respiratoria, que puede ser potencialmente mortal y muy rara vez mortal.
Embarazo y lactancia
Diclofenaco: Estudios de reproducción en conejos, ratas y ratones en dosis hasta 10 y 20mg/kg diario, respectivamente, no se tiene evidencia de teratogenicidad, sin embargo, estas dosis produjeron toxicidad materna y fetal.
Estos efectos en humanos en trabajo de parto actualmente no se conocen. No existen estudios adecuados y controlados del uso de diclofenaco en mujeres embarazadas. El diclofenaco será utilizado en mujeres embarazadas solo si es beneficio justifica el posible riesgo para el feto.
El diclofenaco se distribuye en la leche materna. Debido al potencial riesgo de reacciones adversas en niños en período de lactancia, se debe decidir si descontinuar la lactancia o el medicamento, tomando en cuenta la importancia del medicamento en la mujer.
Tramadol: El tramadol cruza la barrera placentaria, por lo que debe ser utilizado en el embarazo únicamente si el beneficio justifica el riesgo potencial en el feto. Estudios han demostrado que el tramadol es embriotóxico y fetotóxico en ratones, ratas y conejos en dosis tóxicas maternas (3 a 15 veces la dosis máxima de humanos), sin embargo, no demostró ser teratogénico a estas dosis. En dosis tóxicas maternas la embrio y fetotoxicidad incluye pérdida de peso en el feto y aumento en el número de costillas. El uso a largo plazo durante el embarazo puede provocar dependencia física síntomas de síndrome de abstinencia en el recién nacido.
El tramadol es distribuido en la leche materna. Debido a que la seguridad del tramadol en infantes y neonatos no ha sido evaluada, la droga no es recomendada en medicación preoperatoria y post parto en mujeres lactantes.
DOSIS Y VÍA DE ADMINISTRACIÓN:
Posología y forma de administración
Vía de administración: Oral.
Adultos y adolescentes mayores a 17 años: La dosis inicial es de 1 tableta al día (25mg de tramadol clorhidrato /25mg Diclofenaco sódico), la cual puede ir incrementándose 25 mg (1 tableta) cada 3 días en dosis separadas, hasta alcanzar un máximo de 1 tableta cada 6 horas (100 mg de tramadol clorhidrato/100mg Diclofenaco sódico).
MANIFESTACIONES Y MANEJO DE LA SOBREDOSIFICACIÓN O INGESTA ACCIDENTAL:
Sobredosificación
Diclofenaco
La sobredosis de diclofenaco produce manifestaciones que son extensiones de los efectos adversos del medicamento. Perdida de la conciencia, incremento de la presión intracraneal y neumonitis por aspiración fueron reportados en hombres de 17 años, quienes murieron 2 días luego de haber consumido 5g de diclofenaco. No se presentaron signos ni síntomas de toxicidad fueron observados en pacientes que consumieron 3.75 – 4 g de diclofenaco. Sin embargo, vómitos y náusea se presentaron en adolescentes que ingirieron 2.37g de diclofenaco. Tratamiento: Para tratar la sobredosis, las medidas generales deben incluir vaciar el estómago mediante inducción de vómito o lavado gástrico, seguido de tratamiento sintomático y de soporte.
La administración de carbón activado puede ser de utilidad para minimizar la absorción de diclofenaco y la reabsorción de la circulación enterohepática. Diuresis forzada, alcalinización de la orina, hemodiálisis, puede no ser de beneficio para eliminar el medicamento ya que este se une altamente a proteínas plasmáticas. Si se utiliza la diuresis forzada para mejorar la excreción de la droga, se deben controlar los fluidos y el balance de electrolitos, debido a que puede existir perturbaciones serias de electrolitos y retención de líquidos.
Tramadol
La sobredosis produce los siguientes efectos: bradicardia (dolor de pecho o incomodidad, mareo o desmayo, latidos lentos o irregulares, cansancio inusual), piel fría y húmeda, coma (cambio en la conciencia o perdida de conciencia), confusión, convulsiones, muerte*, mareo severo, nerviosismo, flacidez musculoesquelética, respiración lenta, debilidad severa, epilepsia.
*La muerte debido a tramadol ha sido reportado por el abuso y mal uso del tramadol por ingesta, inhalación o inyección de tabletas trituradas. Además, se reporta que la sobredosis mortal aumenta cuando es utilizado concomitantemente con alcohol u otros depresores del SNC, incluyendo opioides.
Tratamiento: Para disminuir la absorción se debe realizar un lavado gástrico. En cuanto al tratamiento especifico se debe administrar un antagonista opioide como la naloxona, la cual puede revertir algunos síntomas de sobredosificación del tramadol, esta se debe administrar con precaución ya que puede precipitar episodios epilépticos. Para tratar la epilepsia causada por la toxicidad del tramadol se debe tratar con Diazepam. En cuanto al tratamiento de soporte se debe hidratar, corregir el balance electrolítico, oxigenar y la ventilación es esencial para mantener las funciones vitales del paciente. La hemodiálisis no es recomendada en sobredosis pues remueve menos del 7% de la dosis administrada en un período de 4 horas.
PRESENTACIÓN:
Naturaleza y contenido del envase
Envase: Blister PVC/PE/PVDC claro y aluminio laqueado.Muestra médica: Caja con 2, 4 y 5 tabletas.
Farmacia: Caja con 10, 20, 30 y 50 tabletas.
Hospitalaria: Caja con 100 tabletas.
RECOMENDACIONES SOBRE ALMACENAMIENTO:
Precauciones especiales de conservación: Consérvese en un lugar seco a temperatura no mayor de 30 ºC.
Período de validez: 24 meses
BIBLIOGRAFÍA:
Datos preclínicos de seguridad
Diclofenaco:
Los datos preclínicos obtenidos de estudios de toxicidad aguda y repetida, así como de estudios de genotoxicidad y cancerogénesis parecen indicar que el diclofenaco no presenta un riesgo específico para humanos a las dosis terapéuticas utilizadas. En los estudios preclínicos estándar en animales no hubo evidencia de potencial teratógeno de diclofenaco en ratones, ratas o conejos. Sin embargo, diclofenaco puede afectar negativamente a la gestación y/o desarrollo del embrión/ feto en mujeres. En ratas, diclofenaco no influyó en la fertilidad de los animales genitores, a excepción de un mínimo efecto fetal, a dosis tóxicas maternas. El desarrollo prenatal, perinatal y posnatal de las crías no se vio afectado. Sin embargo, el diclofenaco puede alterar la fertilidad en mujeres. La administración de AINEs, incluido diclofenaco, inhibe la ovulación en conejos, la implantación y placentación en ratas, y produce el cierre prematuro del conducto arterial en ratas preñadas.
Diclofenaco, a dosis tóxicas maternas, se ha asociado en ratas a distocia, gestación prolongada, disminución de la supervivencia fetal y retraso del crecimiento intrauterino. Los mínimos efectos de diclofenaco en la reproducción y parto, así como en la constricción del conducto arterial en el útero son consecuencias farmacológicas de esta clase de inhibidores de la síntesis de prostaglandinas. Tramadol:
Tras la administración repetida oral y parenteral de tramadol durante 6 -26 semanas a ratas y perros, así como durante 12 meses por vía oral a perros, no se detectó ninguna alteración relacionada con la sustancia en los análisis hematológicos, clínico-químicos ni en el examen histológico. Únicamente tras la administración de dosis muy elevadas, considerablemente superiores al rango terapéutico, se presentaron síntomas nerviosos centrales: agitación, salivación, convulsiones y reducción de la ganancia de peso.
Ratas y perros toleraron, sin reacción alguna, dosis orales de 20 mg/kg y 10 mg/kg de peso corporal respectivamente, y los perros toleraron dosis administradas por vía rectal de 20 mg/kg de peso corporal. En ratas, dosis de tramadol desde 50 mg/kg/día en adelante causaron efectos tóxicos en madres y aumentaron la tasa de mortalidad en neonatos. Se produjo un retraso del desarrollo de las crías, manifestado por trastornos de la osificación y retraso en la apertura de la vagina y de los ojos. La fertilidad de los machos y hembras no se vio afectada. En conejos hubo efectos tóxicos en las madres y anomalías en el esqueleto de las crías con dosis de 125 mg/kg/día y superiores. En algunos de los ensayos in-vitro se observaron indicios de efectos mutagénicos. Los ensayos in vivo no demuestran tales efectos. De acuerdo con el conocimiento actual, tramadol puede ser considerado como una sustancia sin efectos mutagénicos. Se han realizado estudios sobre el potencial cancerígeno de hidrocloruro de tramadol en ratas y ratones. El estudio en ratas no mostró evidencia de incremento, relacionado con la sustancia, de la incidencia de tumores. En el estudio realizado con ratones se observó una mayor incidencia de adenomas hepatocelulares en los machos (aumento no significativo dependiente de la dosis a partir de 15 mg/Kg. de peso) y un incremento de tumores pulmonares (significativo, pero no dosis dependiente) en las hembras de todos los grupos de dosificación.
Referencias bibliográficas:
1. Martindale. (2017). The Complete Drug Reference. 39th Edition. Great Britain: Pharmaceutical Press.
2. Drug Information for the Health Care Professional. (2007). USP DI. 27th Edition. Vol. I. EE.UU.:Thomson Micromedex.
3. AHFS Drug Information. (2017). American Hospital Formulary Service. United States of America: American Society of Health-System Pharmacists.
4. Vademécum Internacional. (2007). Especialidades farmacéuticas y Biológicas. Productos y Artículos de Parafarmacia, Métodos de Diagnóstico. 48a edición. España: CMP MEDICOM Editorial, S.A.
5. Agencia española de medicamentos y productos sanitarios. AEMPS. Ficha técnica disponible en: https://cima.aemps.es/cima/pdfs/es/ft/62016/FT_62016.html.pdf
6. Agencia española de medicamentos y productos sanitarios. AEMPS. Ficha técnica disponible en: https://cima.aemps.es/cima/pdfs/es/ft/64442/FT_64442.html.pdf
LUMINOVA PHARMA GROUP