
POMALYST®
POMALIDOMIDA
Cápsulas duras
1 Envase(s), 21 Cápsulas duras, 1 /2 /3 /4 Miligramos
COMPOSICIÓN:
Fórmula
Cápsula de 1 mg
Cápsula dura con la tapa opaca de color azul oscuro y cuerpo opaco de color amarillo con la inscripción “POML” en tinta blanca y la inscripción “1 mg” en tinta negra.
Cada CÁPSULA de 1 mg contiene:
Pomalidomida 1 mg
Excipientes:
Manitol 53,68 mg
Almidón Pregelatinizado(1) 70,00 mg
Estearil Fumarato de Sodio 0,32 mg
(1)Almidón Pregelatinizado (Almidón de maíz)
Composición de la cápsula:
Gelatina 37,482 mg
Dióxido de Titanio 0,359 mg
Indigotina, (E 132) 0,106 mg
Óxido de Hierro amarillo, (E 172) 0,054 mg
Composición de la Tinta de la cápsula:
Tinta blanca:
Goma laca, dióxido de titanio (E171), simeticona, propilenglicol (E1520) hidróxido de amonio (E527), Alcohol Isopropílico y N-Butanol.
Tinta negra:
Goma laca, óxido de hierro negro (E172), propilenglicol (E1520) hidróxido de amonio (E527), agua, Etanol absoluto, N-Butanol y alcohol Isopropílico.
Cápsula de 2 mg
Cápsula dura con la tapa opaca de color azul oscuro y cuerpo opaco de color naranja con la inscripción “POML 2 mg” en tinta blanca.
Cada CÁPSULA de 2 mg contiene:
Pomalidomida 2 mg
Excipientes:
Manitol 107,36 mg
Almidón Pregelatinizado(1) 140,00 mg
Estearil Fumarato de Sodio 0,64 mg
(1)Almidón Pregelatinizado (Almidón de maíz)
Composición de la cápsula:
Gelatina 59,494 mg
Dióxido Titanio 0,867 mg
Óxido de Hierro amarillo, (E 172) 0,459 mg
Indigotina, (E 132) 0,171 mg
Eritrosina, (E127) 0,009 mg
Composición de la Tinta de la cápsula:
Tinta blanca:
Goma laca, dióxido de titanio (E171), simeticona, propilenglicol (E1520) hidróxido de amonio (E527), Alcohol Isopropílico y N-Butanol.
Cápsula de 3 mg
Cápsula dura con la tapa opaca de color azul oscuro y cuerpo opaco de color verde con la inscripción “POML 3 mg” en tinta blanca.
Cada CÁPSULA de 3 mg contiene:
Pomalidomida 3 mg
Excipientes:
Manitol 75,75 mg
Almidón Pregelatinizado(1) 100,80 mg
Estearil Fumarato de Sodio 0,45 mg
(1)Almidón Pregelatinizado (Almidón de maíz)
Composición de la cápsula:
Gelatina 59,849 mg
Dióxido Titanio 0,866 mg
Indigotina, (E 132) 0,188 mg
Óxido de Hierro amarillo, (E 172) 0,077 mg
Composición de la Tinta de la cápsula:
Tinta blanca:
Goma laca, dióxido de titanio (E171), simeticona, propilenglicol (E1520) hidróxido de amonio (E527), Alcohol Isopropílico y N-Butanol.
Cápsula de 4 mg
Cápsula dura con la tapa opaca de color azul oscuro y cuerpo opaco de color azul con la inscripción “POML 4 mg” en tinta blanca.
Cada CÁPSULA de 4 mg contiene:
Pomalidomida 4 mg
Excipientes:
Manitol 101,00 mg
Almidón Pregelatinizado(1) 134,40 mg
Estearil Fumarato de Sodio 0,60 mg
(1)Almidón Pregelatinizado (Almidón de maíz)
Composición de la cápsula:
Gelatina 59,672 mg
Dióxido Titanio 1,101 mg
Indigotina, (E 132) 0,171 mg
Azul brillante FCF , (E 133) 0,056 mg
Composición de la Tinta de la cápsula:
Tinta blanca:
Goma laca, dióxido de titanio (E171), simeticona, propilenglicol (E1520) hidróxido de amonio (E527), Alcohol Isopropílico y N-Butanol.
INDICACIONES TERAPÉUTICAS:
Acción terapéutica: Agente inmunomodulador, código ATC: L04AX06.Venta bajo receta médica.
Indicaciones: POMALYST® en combinación con dexametasona está indicado en el tratamiento de los pacientes adultos con mieloma múltiple resistente al tratamiento y recidivante que hayan recibido al menos dos tratamientos previos, incluyendo lenalidomida y bortezomib, y que hayan experimentado una progresión de la enfermedad en el último tratamiento.
MECANISMO DE ACCIÓN:
Acción farmacológica
Mecanismo de acción: Pomalidomida es un medicamento con actividad tumoricida directa contra el mieloma, con actividad inmunomoduladora y que es capaz de inhibir el apoyo de las células del estroma para el crecimiento de las células cancerosas del mieloma múltiple. En concreto, pomalidomida inhibe la proliferación e induce la apoptosis de las células hematopoyéticas tumorales. Además, pomalidomida inhibe la proliferación de las líneas celulares de mieloma múltiple resistentes a lenalidomida y presenta un efecto sinérgico con dexametasona tanto en las líneas celulares de mieloma múltiple resistentes a lenalidomida como en a sensibles a lenalidomida para inducir la apoptosis de las células tumorales. Pomalidomida potencia la inmunidad celular mediada por los linfocitos T y por los linfocitos natural killer (NK) e inhibe la producción de citocinas proinflamatorias (p. ej. TNF-a e IL-6) por los monocitos. Pomalidomida también inhibe la angiogénesis mediante el bloqueo de la migración y adhesión de células endoteliales.
Acción farmacocinética
Absorción: Pomalidomida se absorbe alcanzando una concentración plasmática máxima (Cmáx) a las 2 o 3 horas y, por lo menos, un 73 % se absorbe después de administrar una dosis única por vía oral. El área bajo la curva (AUC) de pomalidomida aumenta, aproximadamente, lineal y proporcionalmente con los incrementos de la dosis. Tras la administración de múltiples dosis, pomalidomida tiene una ratio de acumulación del 27 al 31% en el AUC. La administración conjunta con una comida rica en grasas y rica en calorías reduce la tasa de absorción, disminuyendo la Cmáx plasmática media en aproximadamente, un 27 %, pero con un efecto mínimo sobre la extensión de la absorción global con una disminución del 8% en el AUC media. Por tanto, pomalidomida puede administrarse con o sin alimentos.
Distribución: Pomalidomida tiene un volumen de distribución aparente (Vd) medio de entre 62 y 138 litros en estado estable. En el semen de sujetos sanos pomalidomida se distribuye a una concentración de aproximadamente el 67% del nivel de plasma a las 4 horas posteriores a la administración (aproximadamente Tmáx) tras 4 días de administración de 2 mg una vez al día. La unión in vitro de los enantiómeros de pomalidomida a las proteínas plasmáticas en humanos oscila entre el 12 % y el 44 % y no es dependiente de la concentración. Biotransformación: En sujetos sanos que han recibido una dosis única por vía oral de [14C] pomalidomida (2 mg), pomalidamida es la mayor sustancia circulante (aproximadamente, el 70% de la radioactividad del plasma) in vivo. No se hallaron metabolitos en concentración >10% relativos a la radioactividad total o relacionada en plasma.Las rutas metabólicas principales de la radioactividad excretada son los procesos de hidroxilación con la posterior glucuronidación, o hidrólisis. Los estudios in vitro identificaron al CYP1A2 y al CYP3A4 como las enzimas primarias implicadas en la hidroxilación de pomalidomida mediada por CYP, con contribuciones menores adicionales del CYP2C19 y CYP2D6. Pomalidomida es también un sustrato de la glicoproteína-P in vitro. La administración concomitante de pomalidomida con el potente inhibidor del CYP3A4/5 y de la Gp-P, ketoconazol, o con el potente inductor del CYP3A4/5, carbamazepina, no demostró ningún efecto clínicamente relevante en la exposición a pomalidomida. La administración concomitante de pomalidomida con el inhibidor potente del CYP1A2, fluvoxamina, en presencia de ketoconazol, incrementó la exposición media a pomalidomida en un 107 %, con un intervalo de confianza del 90 % [del 91 % al 124 %], frente a pomalidomida más ketoconazol. En un segundo estudio realizado para evaluar la contribución a los cambios del metabolismo de un inhibidor del CYP1A2 solo, la administración conjunta de fluvoxamina sola con pomalidomida aumentó la exposición media a pomalidomida en un 125 % con un intervalo de confianza del 90 % [del 98 % al 157 %] frente a pomalidomida administrada en monoterapia. Si se administran inhibidores potentes del CYP 1A2 (p. ej., ciprofloxacino, enoxacino y fluvoxamina) de forma concomitante con pomalidomida , se debe reducir la dosis de pomalidomida en un 50 %. La administración de pomalidomida a fumadores, sabiendo que el tabaquismo induce la isoforma CYP 1A2, no tuvo ningún efecto clínicamente relevante en la exposición a pomalidomida frente a la exposición a pomalidomida observada en los no fumadores.
Según los datos in vitro, pomalidomida no es un inhibidor o inductor de las isoenzimas del citocromo P-450 y no inhibió ninguno de los fármacos transportadores que fueron estudiados. No se espera que pomalidomida pueda causar interacciones medicamentosas clínicamente relevantes cuando se administra de forma concomitante con sustratos de estas rutas.
Eliminación: En sujetos sanos pomalidomida se elimina con una mediana de semivida plasmática de aproximadamente, 9,5 horas y de unas 7,5 horas en pacientes con mieloma múltiple. Pomalidomida tiene una media de aclaramiento corporal total (C1/F) de aproximadamente, 7-10 1/h.
Tras una dosis única por vía oral de [14 C] pomalidomida (2 mg) en sujetos sanos, aproximadamente, el 73% y el 15% de la dosis radioactiva se eliminó por la orina y las heces, respectivamente con aproximadamente, el 2 % y el 8 % del radiocarbono administrado eliminado como pomalidomida en orina y heces.
Pomalidomida se metaboliza ampliamente antes de la excreción, con los metabolitos resultantes eliminados principalmente por la orina. Los tres metabolitos predominantes en la orina (formados mediante hidrólisis o hidroxilación con posterior glucuronidación) representan aproximadamente, el 23 %, 17 % y 12 %, respectivamente, de la dosis en la orma.
Los metabolitos dependientes del CYP representan aproximadamente, el 43 % de la radiactividad total excretada, mientras que los metabolitos hidrolíticos no dependientes del CYP representan el 25 %, y la excreción de pomalidomida inalterada representa el 1O % (2 % en orina y 8 % en heces).
Farmacocinética poblacional: Según análisis de farmacocinética poblacional basado en un modelo bicompartimental, los sujetos sanos y los pacientes con mieloma múltiple mostraron aclaramiento aparente (C1/F) y volumen de distribución aparente en el compartimento central (V2/F) comparables. En tejidos periféricos, pomalidomida fue absorbida preferentemente por los tumores con un aclaramiento de distribución aparente en el compartimento periférico (Q/F) y un volumen de distribución aparente en el compartimento periférico (V3/F) 3,7 veces y 8 veces mayor, respectivamente, comparado con los sujetos sanos.
Población pediátrica: No existen datos disponibles sobre la administración de pomalidomida en pacientes niños o adolescentes (<18 años de edad).
Población de edad avanzada: Según análisis de farmacocinética poblacional en sujetos sanos y en pacientes con mieloma múltiple, no se observó una influencia significativa de la edad (19-83 años) en el aclaramiento oral de pomalidomida.En los estudios clínicos los pacientes de edad avanzada (> 65 años) expuestos a pomalidomida no requirieron ningún ajuste de dosis.
Insuficiencia renal: Los análisis de farmacocinética poblacional mostraron que los parámetros farmacocinéticos de pomalidomida no se vieron afectados de forma destacable en los pacientes con insuficiencia renal (definida mediante el aclaramiento de la creatinina o el Filtrado Glomerular Estimado [FGe]) en comparación con los pacientes con la función renal normal (CrCl ≥60 ml/minuto). La exposición media a pomalidomida normalizada según el AUC fue del 98,2 % con un intervalo de confianza del 90 % [77,4 % al 120,6 %] en los pacientes con insuficiencia renal moderada (FGe 2:30 a ::;45 ml/minuto/ 1,73 m2) en comparación con los pacientes con la función renal normal. La exposición media a pomalidomida normalizada según el AUC fue del 100,2% con un intervalo de confianza del 90% [79,7% al 127,0 %] en los pacientes con insuficiencia renal grave que no precisaban diálisis (CrCl <30 o FGe <30 ml/minuto/1,73 m2) en comparación con los pacientes con la función renal normal. La exposición media a pomalidomida normalizada según el AUC aumentó en un 35,8 %con un IC del 90 % [7,5 % al 70,0 %] en los pacientes con insuficiencia renal grave que precisaban diálisis (CrCl <30 mi/minuto con necesidad de diálisis) en comparación con los pacientes con la función renal normal. Los cambios medios en la exposición a pomalidomida en cada uno de estos grupos de insuficiencia renal no son de una magnitud que requiera un ajuste de la dosis.
Insuficiencia hepática: Los parámetros farmacocinéticos cambiaron modestamente en los pacientes con insuficiencia hepática (definida mediante los criterios de Child-Pugh) en comparación con los sujetos sanos. La exposición media a pomalidomida aumentó en un 51 % con un intervalo de confianza del 90 % [del 9 % al 11O %] en los pacientes con insuficiencia hepática leve en comparación con los sujetos sanos. La exposición media a pomalidomida aumentó en un 58% con un intervalo de confianza del 90 % [del 13 % al 119 %] en los pacientes con insuficiencia hepática moderada en comparación con los sujetos sanos. La exposición media a pomalidomida aumentó en un 72 % con un intervalo de confianza del 90 % [del 24 % al 138 %] en los pacientes con insuficiencia hepática grave en comparación con los sujetos sanos. Los aumentos medios en la exposición a pomalidomida en cada uno de estos grupos de insuciencia hepática no son de una magnitud que requiera un ajuste del esquema de tratamiento o de la dosis (ver Posología, dosificación y administración).
Farmacodinamia
Estudios clínicos
Eficacia clínica y seguridad: Se evaluó la eficacia y seguridad de pomalidomida en combinaci ón con dexame-tasona en un ensayo de fase 111, multicéntrico, aleatorizado y abierto (CC-4047-MM-003), donde se comparó el tratamiento de pomalidomida más una dosis baja de dexametasona (Pom + LD-Dex) frente a una dosis alta de dexametasona sola (HD-Dex) en pacientes adultos con mieloma múltiple en recaída y refractario que ya habían recibido al menos dos tratamientos previos, incluyendo lenalidomida y bortezomib , y que habían mostrado progresión de la enfermedad durante el último tratamiento. En el estudio participaron un total de 455 pacientes: 302 en el grupo Pom + LD-Dex y 153 en el grupo HD-Dex. La mayoría de los pacientes eran varones (59 %) y caucásicos (79 %); la mediana de edad de toda la población era de 64 años (mín, máx: 35, 87 años). Los pacientes del grupo Pom + LD-Dex tomaron 4 mg de pomalidomida por vía oral en los días del 1 al 21 en cada ciclo de 28 días. Se administró la dosis de LD-Dex (40 mg) una vez al día en los días 1, 8, 15 y 22 de un ciclo de 28 días. En el grupo HD-Dex, los pacientes tomaron dexametasona (40 mg) una vez al día en los días del 1 al 4, del 9 al 12 y del 17 al 20 en un ciclo de 28 días. Los pacientes mayores de 75 años iniciaron el tratamiento con dexametasona 20 mg. Los pacientes continuaron con el tratamiento hasta la progresión de la enfermedad.
La variable principal de eficacia fue la Supervivencia Libre de Progresión (SLP) de acuerdo con los criterios del International Myeloma Working Group (IMWG). Para la población por intención de tratar (IDT), la mediana del tiempo de SLP según revisión del Independent Review Adjudication Committee (IRAC) basada en los criterios del IMWG fue de 15,7 semanas (IC de 95 %: 13,0; 20,1) en el grupo Pom + LD-Dex; la tasa estimada de supervivencia libre de eventos a las 26 semanas fue del 35,99 % (± 3,46 %). En el grupo HD-Dex, la mediana del tiempo de SLP fue de 8,0 semanas (IC de 95 %: 7,0; 9,0); la tasa estimada de supervivencia libre de eventos a las 26 semanas fue del 12,15 % (± 3,63 %).
Se evaluó la SLP en varios subgrupos relevantes: sexo, raza, estatus de rendimiento ECOG, factores de estratificación (edad, población con enfermedad, terapias antimieloma previas [2, >2]), parámetros de relevancia pronóstica seleccionados (niveles basales de beta-2 microglobulina, niveles basales de albúmina , insuficiencia renal basal y riesgo citogenético) y exposición y refractariedad a terapias antimieloma previas. Independientemente del subgrupo evaluado, la SLP fue generalmente, consistente con la observada en población por 1 DT en ambos grupos de tratamiento.
En la tabla 1 se resumen los resultados de la supervivencia libre de progresión para la población por IDT. La figura 1 presenta la curva de Kaplan-Meier de la SLP para la población por IDT.
|
Tabla 1: Tiempo de Supervivencia Libre de Progresión según revisión del IRAC basada en los criterios IMWG |
||
|
Pom+LD-Dex (N=302) |
HD-Dex (N=153) |
|
|
Supervivencia libre de progresión (SLP), n |
302 (100,0) |
153 (100,0) |
|
Censurado , n (%) |
138 (45,7) |
50 (32,7) |
|
Progresión/muerte, n (%) |
164 (54,3) |
103 (67,3) |
|
Tiempo de supervivencia libre de progresión (semanas) |
||
|
Medianaa |
15,7 |
8,0 |
|
[IC de 95 % bilateral]b |
[13,0; 20,1] |
[7,0; 9,0] |
|
Razón de riesgo (Hazard Ratio) (Pom+LD-Dex: HD-Dex) [IC de 95 % bilateral]c |
0,45 [0,35; 0,59] |
|
|
Valor P (bilateral) de la prueba de log-rankd |
<0,001 |
|
|
Nota: IC = Intervalo de Confianza; IRAC = Comité Independiente Revisor de Evaluación |
||
|
a La mediana está basada en la estimación de Kaplan-Meier. |
||
|
b Intervalo de confianza de 95 % de la mediana del tiempo de supervivencia libre de progresión. |
||
|
c Basado en el modelo de riesgos proporcionales de Cox que compara las funciones de riesgo asociadas con los grupos de tratamiento, estratificados por edad (≤75 frente a >75), población con la enfermedad (refractario a lenalidomida y bortezomib frente a no refractario a estos dos medicamentos), y número de terapias antimieloma previas (=2 frente a >2). |
||
|
d El valor P está basado en la prueba de log-rank estratificada con los mismos factores de estratificación arriba mencionados para el modelo de Cox. |
||
Figura 1: Supervivencia Libre de Progresión según la revisión de respuesta del IRAC basada en los criterios IMWG (prueba de log-rank estratificada) (población por IDT)
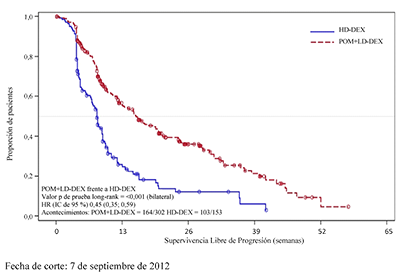
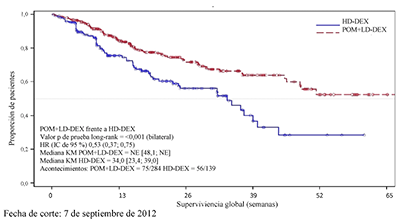
La variable secundaria clave fue la supervivencia global (SG). Un total de 226 pacientes (74,8 %) del grupo Pom + LD-Dex y 95 pacientes (62,1 %) del grupo HD-Dex vivían en el momento de la fecha de corte (7 de septiembre de 2012). La mediana del tiempo de supervivencia global según las estimaciones Kaplan-Meier no fue alcanzado por el grupo Pom + LD Dex, pero podría esperarse que fuera al menos de 48 semanas, que corresponde al umbral más bajo del IC de 95 %. La mediana del tiempo de SG del grupo HD-Dex fue de 34 semanas (IC de 95 %: 23,4; 39,9). La tasa libre de eventos al año fue del 52,6% (± 5,72 %) para el grupo Pom + LD Dex y del 28,4% (± 7,51 %) para el grupo HD-Dex. La diferencia en términos de SG entre los dos grupos de tratamiento fue estadísticamente significativa (p <0,00 1).
La Tabla 2 resume los resultados de supervivencia global para la población por IDT. La curva Kaplan-Meier de SG para la población por IDT se presenta en la Figura 2.
Basándose en los resultados de las variables SLP y SG, el Comité de Monitorización de Datos para este estudio recomendó que se completara el estudio y que los pacientes en el grupo HD-Dex fueran cruzados al grupo Pom + LD-Dex.
|
Tabla 2: Supervivencia global: población PoriDT |
|||
|
Estadísticas |
Pom+LD-Dex (N=302) |
HD-Dex (N=153) |
|
|
N |
302 (100,0) |
153 (100,0) |
|
|
Censurado |
n (%) |
226(74,8) |
95(62,1) |
|
Muerto |
n (%) |
76 (25,2) |
58 (37,9) |
|
Tiempo de supervi-vencia (semanas) |
Medianaa |
NE |
34,0 |
|
IC de 95 % bilateral b |
[ 48,1; NE] |
[ 23,4; 39,9] |
|
|
Razón de riesgo (Hazard Ratio) (Pom+LD-Dex:HD-Dex) [IC de 95 % bilateral c] |
0,53 [ 0,37; 0,74] |
||
|
Valor P (bilateral) de la prueba de log-rank0 |
<0,001 |
||
|
Nota : IC = Mtervalo de Confianza; NE = no estimable. |
|||
|
a La mediana está basada en la estimación de Kaplan-Meier. |
|||
|
b Intervalo de confianza de 95 % sobre la mediana del tiempo de supervivencia global. |
|||
|
e Basado en el modelo de riesgos proporcionales de Cox que compara las funciones de riesgo asociadas con los grupos de tratamiento. |
|||
|
d El valor P está basado en la prueba de log-rank no estratificada. |
|||
Figura 2. Curva de Kaplan-Meier de la Supervivencia Global (Población por IDT)
CONTRAINDICACIONES:
- Embarazo .
- Mujeres con capacidad de gestación , a menos que se cumplan todas las condiciones del programa de prevención de embarazo.
- Pacientes varones incapaces de seguir o cumplir las medidas anticonceptivas requeridas.
- Hipersensibilidad al principio activo o a alguno de los excipientes.
REACCIONES ADVERSAS:
Resumen del perfil de seguridad
Las reacciones adversas notificadas con mayor frecuencia en los estudios clínicos han sido los trastornos de la sangre y del sistema linfático, incluyendo anemia (45,7 %), neutropenia (45,3 %) y trombocitopenia (27 %); trastornos generales y alteraciones en el lugar de la administración, incluyendo fatiga (28,3 %), pirexia (21 %) y edema periférico (13 %); e infecciones e infestaciones incluyendo neumonía (10,7 %). Las reacciones adversas relacionadas con neuropatía periférica fueron notificadas en el 12,3 % de los pacientes y las reacciones adversas de embolismo o tromboembolismo venoso fueron notificadas en el 3,3 % de los pacientes. Las reacciones adversas de grado 3 o 4 más frecuentes estaban relacionadas con trastornos de la sangre y del sistema linfático, incluyendo neutropenia (41,7 %), anemia (27 %) y trombocitopenia (20,7 %); infecciones e infestaciones, incluyendo neumonía (9 %); y trastornos generales y alteraciones en el lugar de la administración, incluyendo fatiga (4,7 %), pirexia (3 %) y edema periférico (1,3 %). La reacción adversa grave notificada con mayor frecuencia fue la neumonía (9,3 %). Otras reacciones adversas graves notificadas incluyen neutropenia febril (4,0 %), neutropenia (2,0 %), trombocitopenia (1,7 %) y reacciones adversas de TEV (1,7 %). Se observó que las reacciones adversas tendían a ocurrir con mayor frecuencia dentro de los primeros 2 ciclos de tratamiento con pomalidomida.
Lista tabulada de reacciones adversas
En el estudio aleatorizado CC-4047-MM-003, un total de 302 pacientes con mieloma múltiple en recaída y refractario fueron tratados con 4 mg de pomalidomida administrada una vez al día durante 21 días en cada ciclo de 28 días, en combinación con una dosis baja semanal de dexametasona.
Las reacciones adversas observadas en los pacientes tratados con pomalidomida y dexametasona se incluyen a continuación, según el sistema de clasificación por órganos (SOC por sus siglas en inglés) y la frecuencia para todas las reacciones adversas y para las reacciones adversas de grado 3 o 4.
Las frecuencias de las reacciones adversas son las notificadas en el grupo de pomalidomida más dexametasona del estudio CC-4047-MM-003 (n=302) y de los datos poscomercialización. Las reacciones adversas se presentan en orden decreciente de gravedad dentro de cada intervalo de SOC y de frecuencia. Las frecuencias se definen, según las guías actuales, como: muy frecuentes (≥1/10); frecuentes (≥1/100 a < 1/10) y poco frecuentes (≥1/1.000 a <1/100).
|
Clasificación de órganos / Término preferido |
Todas las reacciones adversas/Frecuencia |
Reacciones adversas de Grado 3-4/Frecuencia |
|
Infecciones e infestaciones |
Muy frecuentes Neumonía (infecciones bacterianas, víricas y fúngicas, incluidas las infecciones oportunistas) Frecuentes Sepsis neutropénica Bronconeumonía Bronquitis Infección del tracto respiratorio Infección del tracto respiratorio superior Nasofaringitis Herpes zóster Frecuencia no conocida Reactivación de la hepatitis B |
Frecuentes Sepsis neutropénica Neumonía (infecciones bacterianas, víricas y fúngicas, incluidas las infecciones oportunistas) Bronconeumonía Infección del tracto respiratorio Infección del tracto respiratorio superior Poco frecuentes Bronquitis Herpes zóster Frecuencia no conocida Reactivación de la hepatitis B |
|
Neoplasias benignas, malignas y no especificadas (incl. quistes y pólipos) |
Poco frecuentes Carcinoma de piel de células Basales Carcinoma de piel de células escamosas |
Poco frecuentes Carcinoma de piel de células Basales Carcinoma de piel de células escamosas |
|
Trastornos de la sangre y del sistema linfático |
Muy frecuentes Neutropenia Trombocitopenia Leucopenia Anemia Frecuentes Neutropenia febril Pancitopenia* |
Muy frecuentes Neutropenia Trombocitopenia Anemia Frecuentes Neutropenia febril Leucopenia Pancitopenia* |
|
Trastornos del metabolismo y de la nutrición |
Muy frecuentes Disminución del apetito Frecuentes Hiperpotasemia Hiponatremia Hiperuricemia * Poco frecuentes Síndrome de lisis tumoral* |
Frecuentes Hiperpotasemia Hiponatremia Hiperuricemia* Poco frecuentes Disminución del apetito Síndrome de lisis tumoral* |
|
Trastornos psiquiátricos |
Frecuentes Estado de confusión |
Frecuentes Estado de confusión |
|
Trastornos del sistema nervioso |
Frecuentes Disminución del nivel de conciencia Neuropatía sensitiva periférica Mareo Temblor Hemorragia intracraneal* Poco frecuentes Accidente cerebrovascular* |
Frecuentes Disminución del nivel de conciencia Poco frecuentes Neuropatía sensitiva periférica Mareo Temblor Accidente cerebrovascular* Hemorragia intracraneal* |
|
Trastornos del oído y del laberinto |
Frecuentes Vértigo |
Frecuentes Vértigo |
|
Trastornos vasculares |
Frecuentes Trombosis venosa profunda |
Poco frecuentes Trombosis venosa profunda |
|
Trastornos cardíacos |
Frecuentes Insuficiencia cardíaca* Fibrilación auricular* Infarto de miocardio* |
Frecuentes Insuficiencia cardíaca* Fibrilación auricular* Poco frecuentes Infarto de miocardio* |
|
Trastornos del sistema inmunológico |
Frecuentes Angioedema* Urticaria* |
Poco frecuentes Angioedema* Urticaria* |
|
Trastornos respiratorios, torácicos y mediastínicos |
Muy frecuentes Disnea Tos Frecuentes Embolia pulmonar Epistaxis* Enfermedad pulmonar intersticial* |
Frecuentes Disnea Poco frecuentes Embolia pulmonar Tos Epistaxis* Enfermedad pulmonar intersticial* |
|
Trastornos gastrointestinales |
Muy frecuentes Diarrea Náuseas Estreñimiento Frecuentes Vómitos Hemorragia gastrointestinal |
Frecuentes Diarrea Vómitos Estreñimiento Poco frecuentes Náuseas Hemorragia gastrointestinal |
|
Trastornos hepatobiliares |
Poco frecuentes Hiperbilirrubinemia Hepatitis* |
Poco frecuentes Hiperbilirrubinemia |
|
Trastornos de la piel y del tejido subcutáneo |
Frecuentes Erupción Prurito No conocidos Reacción farmacológica con eosinofilia y síntomas sistémicos * Necrolisis epidérmica toxica* Síndrome de Stevens-Johnson * |
Frecuentes Erupción No conocidos Reacción farmacológica con eosinofilia y síntomas sistémicos* Necrolisis epidérmica tóxica* Síndrome de Stevens-Johnson * |
|
Trastornos musculoesqueléticos y del tejido conjuntivo |
Muy frecuentes Dolor óseo Espasmos musculares |
Frecuentes Dolor óseo Poco frecuentes Espasmos musculares |
|
Trastornos renales y urinarios |
Frecuentes Insuficiencia renal Retención urinaria |
Frecuentes Insuficiencia renal Poco frecuentes Retención urinaria |
|
Trastornos del aparato reproductor y de la mama |
Frecuentes Dolor pélvico |
Frecuentes Dolor pélvico |
|
Trastornos generales y alteraciones en el lugar de la administración |
Muy frecuentes Fatiga Pirexia Edema periférico |
Frecuentes Fatiga Pirexia Edema periférico |
|
Exploraciones complementarias |
Frecuentes Disminución del recuento de neutrófilos Disminución del recuento de leucocitos Disminución del recuento de plaquetas Aumento de la alanina aminotransferasa Aumento del ácido úrico en sangre* |
Frecuentes Disminución del recuento de neutrófilos Disminución del recuento de leucocitos Disminución del recuento de plaquetas Aumento de la alanina aminotransferasa Poco frecuentes Aumento del ácido úrico en sangre* |
|
*Identificados a partir de los datos poscomercialización; las frecuencias se basan en los datos de los ensayos clínicos. |
||
Descripción de reacciones adversas seleccionadas Teratogenicidad
Pomalidomida está relacionada estructuralmente con talidomida. Talidomida es un principio activo con acción teratogénica conocida en humanos, que causa defectos de nacimiento graves que pueden poner en peligro la vida del niño. Pomalidomida tiene un efecto teratogénico en ratas y conejos cuando se administra durante el período de mayor organogénesis. Si se toma pomalidomida durante el embarazo, se espera un efecto teratogénico de pomalidomida en los seres humanos.
Neutropenia y trombocitopenia
El 45,3 % de los pacientes que recibieron pomalidomida más dosis bajas de dexametasona (Pom + LD-Dex) experimentó neutropenia, frente al 19,5 % de los pacientes que recibieron dosis altas de dexametasona (HD-Dex). La neutropenia fue de grado 3 o 4 en un 41,7 % de los pacientes que recibieron Pom + LD-Dex frente al 14,8 % de los que recibieron HD-Dex. En los pacientes tratados con Pom + LD-Dex, la neutropenia fue grave en una minoría (2,0 % de los pacientes), no tuvo como consecuencia la suspensión del tratamiento, y se asoció con la interrupción del tratamiento en un 21,0 % de los pacientes y con una reducción de la dosis en un 7,7 % de los pacientes. El 6,7 % de los pacientes que recibieron Pom + LD-Dex experimentó Neutropenia Febril (NF), frente a ninguno de aquellos que recibieron HD-Dex. Todos los casos fueron notificados como de grado 3 o 4. La NF fue notificada como grave en un 4,0 % de los pacientes. Asimismo, la NF se asoció con una interrupción de la dosis en un 3,7 % de los pacientes, con una reducción de la dosis en un 1,3 % de los pacientes y con ningún caso de suspensión del tratamiento. El 27,0 % de los pacientes que recibieron Pom + LD-Dex experimentó trombocitopenia frente a un 26,8 % de los pacientes que recibieron HD-Dex. La trombocitopenia fue de grado 3 o 4 en un 20,7 % de los pacientes que recibieron Pom + LD-Dex frente a un 24,2 % de los que recibieron HD-Dex. En los pacientes tratados con Pom + LD-Dex, la trombocitopenia fue grave en un 1,7 % de los pacientes, conllevó una reducción de la dosis en un 6,3 % de los pacientes, una interrupción de la dosis en un 8 % de los pacientes y la suspensión del tratamiento en un 0,7 % de los pacientes.
Infección
La infección fue la toxicidad no hematológica más frecuente, con una incidencia del 55,0 % en los pacientes que recibieron Pom + LD-Dex frente al 48,3 % en los pacientes que recibieron HD-Dex. Aproximadamente, la mitad de dichas infecciones fueron de grado 3 o 4; un 24,0 % en los pacientes tratados con Pom + LD-Dex y un 22,8 % en los pacientes tratados con HD-Dex. Entre los pacientes tratados con Pom + LD-Dex las infecciones notificadas con mayor frecuencia fueron la neumonía y la infección del tracto respiratorio superior (en un 10,7 % y un 9,3 % de los pacientes, respectivamente); con un 24,3 % de las infecciones notificadas clasificadas como graves o mortales (grado 5) en el 2,7 % de los pacientes tratados. En los pacientes tratados con Pom + LD-Dex las infecciones conllevaron la suspensión de la dosis en un 2,0 % de los pacientes, la interrupción del tratamiento en un 14,3 % de los pacientes y la reducción de la dosis en un 1,3 % de los pacientes.
Eventos tromboembólicos
El 3,3 % de los pacientes que recibieron Pom + LD-Dex y un 2,0 % de los pacientes que recibieron HD-Dex experimentaron un embolismo o tromboembolismo venoso. El 1,3 % de los pacientes que recibieron Pom + LD-Dex experimentó reacciones de grado 3 o 4 frente a ningún caso entre los pacientes que recibieron HD-Dex. En los pacientes tratados con Pom + LD-Dex, el TEV se notificó como grave en el 1,7 %, no se notificó ninguna reacción adversa mortal en los estudios clínicos y el TEV no se asoció con suspensión de la dosis. La profilaxis con ácido acetilsalicílico (y otros anticoagulantes en pacientes de alto riesgo) fue obligatoria para todos los pacientes participantes en los estudios clínicos. Se recomienda terapia anticoagulante (a no ser que esté contraindicada). Neuropatía periférica
Se excluyó de los estudios clínicos a los pacientes con neuropatía periférica en curso de grado ≥2. El 12,3 % de los pacientes que recibieron Pom + LD-Dex experimentaron una neuropatía periférica, la mayoría de grado 1 o 2, frente a un 10,7 % de los pacientes que recibieron HD-Dex. El 1,0 % de los pacientes que recibieron Pom + LD-Dex experimentó reacciones de grado 3 o 4 frente al 1,3 % de los pacientes que recibieron HD-Dex. En los estudios clínicos, ninguna de las neuropatías periféricas se notificó como grave en los pacientes tratados con Pom + LD-Dex y la neuropatía periférica condujo a la suspensión de la dosis en un 0,3 % de los pacientes.
La mediana del tiempo hasta la aparición de la neuropatía fue de 2,1 semanas, con una variación de 0,1 a 48,3 semanas. La mediana del tiempo hasta la aparición fue inferior en los pacientes que recibieron HD-Dex comparado con los pacientes tratados con Pom+LD-Dex (1,3 semanas frente a 2,1 semanas). La mediana del tiempo hasta la desaparición de los síntomas fue de 22,4 semanas en los pacientes que recibieron Pom+LD-Dex y de 13,6 semanas en los pacientes que recibieron HD-Dex. El límite inferior del intervalo de confianza del 95 % fue de 5,3 semanas en los pacientes tratados con Pom+LD-Dex y de 2,0 semanas en los pacientes que recibieron HD-Dex.
Hemorragia
Se han notificado trastornos hemorrágicos con pomalidomida, especialmente, en pacientes con factores de riesgo tales como medicamentos concomitantes que aumentan el riesgo de hemorragia. Los eventos hemorrágicos incluyen epistaxis, hemorragia intracraneal y hemorragia gastrointestinal.
Reacciones alérgicas y reacciones cutáneas graves Se ha informado angioedema y reacciones cutáneas graves que incluyen SJS, TEN y DRESS con el uso de pomalidomida. Los pacientes con antecedentes de erupción cutánea grave asociada con lenalidomida o talidomida no deben recibir pomalidomida.
Notificación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico, farmacéutico o enfermero, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
Para más información, llame al Departamento Científico: Teléfono PBX 5005005 , E.mail: farmacovigilancia@medicamenta.com.ec
Efectos sobre la capacidad para conducir y utilizar máquinas
La influencia de POMALYST sobre la capacidad para conducir y utilizar máquinas es pequeña o moderada. Se han notificado casos de fatiga, disminución del nivel de conciencia, confusión y mareo relacionados con el uso de pomalidomida. Si notan estos efectos, se debe advertir a los pacientes de que no deben conducir automóviles, utilizar máquinas o realizar cualquier actividad peligrosa durante su tratamiento con pomalidomida.
INTERACCIONES MEDICAMENTOSAS Y DE OTRO GÉNERO:
Interacciones medicamentosas
Efecto de POMALYST sobre otros medicamentos No se espera que pomalidomida pueda causar interacciones medicamentosas farmacocinéticas clínicamente relevantes debido a la inhibición o inducción de la isoenzima P450, o inhibición de transportadores cuando se administra de forma concomitante con sustratos de estas enzimas o transportadores. No se ha evaluado clínicamente el potencial de estas interacciones medicamentosas, incluyendo el posible impacto de pomalidomida en la farmacocinética de los anticonceptivos orales combinados.
Efecto de otros medicamentos sobre POMALYST Pomalidomida se metaboliza parcialmente por CYP1A2 y CYP3A4/5.También es un sustrato de la glicoproteína P. La administración concomitante de pomalidomida con ketoconazol, inhibidor potente del CYP3A4/5 y de la Gp-P, o con el inductor potente del CYP3A4/5, carbamazepina, no demostró ningún efecto clínicamente relevante a la exposición a pomalidomida. La administración concomitante de pomalidomida con el inhibidor potente del CYP1A2 fluvoxamina en presencia de ketoconazol, incrementó la exposición media a pomalidomida en un 107 %, con un intervalo de confianza del 90 % [del 91 % al 124 %], frente a pomalidomida más ketoconazol. En un segundo estudio realizado para evaluar la contribución a los cambios del metabolismo de un inhibidor del CYP1A2 solo, la administración conjunta de fluvoxamina sola con pomalidomida aumentó la exposición media a pomalidomida en un 125 % con un intervalo de confianza del 90 % [del 98 % al 157 %] frente a pomalidomida administrada en monoterapia. Si se administran inhibidores potentes del CYP1A2 (p. ej., ciprofloxacino, enoxacino y fluvoxamina) de forma concomitante con pomalidomida, se debe reducir la dosis de pomalidomida en un 50 %.
Dexametasona
La administración concomitante de múltiples dosis de hasta 4 mg de pomalidomida con dexametasona de 20 mg a 40 mg (un inductor leve a moderado de varias enzimas CYP, incluido el CYP3A) en pacientes con mieloma múltiple no tuvo ningún efecto sobre la farmacocinética de pomalidomida frente a pomalidomida administrada sola. Se desconoce el efecto de dexametasona sobre la warfarina. Se aconseja realizar una monitorización rigurosa de la concentración de warfarina durante el tratamiento.
INFORMACIÓN COMPLEMENTARIA:
Fecha de última revisión: 04/2018.
PAÍS DE PROCEDENCIA: Suiza.
ELABORADO POR: CELGENE INTERNATIONAL SARL (Route de Perreux I, 2017, Boudry, Suiza).
PARA: CELGENE EUROPE LIMITED (1 Longwalk Road, Stockley Park, Uxbridge UB11 1DB, Reino Unido).
ACONDICIONADO EN URUGUAY POR:
ADIUM PHARMA S.A., Ruta 8, Km 17500 Zonamerica, Montevideo, República Oriental del Uruguay.
MEDICAMENTA
Casilla 17-21-027 Quito, Ecuador
RECOMENDACIONES:
Advertencias y precauciones:
Teratogenicidad Pomalidomida no debe tomarse durante el embarazo ya que es esperable un efecto teratogénico. Pomalidomida está relacionada estructuralmente con talidomida. Talidomida es un teratógeno conocido en humanos, que causa defectos congénitos de nacimiento graves que pueden poner en peligro la vida del niño. Pomalidomida tiene un efecto teratogénico en ratas y conejos cuando se administra durante el período de mayor organogénesis. Todas las pacientes deben cumplir las condiciones del Programa de Prevención de Embarazo a menos que exista evidencia fiable de que la paciente no tiene capacidad de gestación.
Criterios para mujeres que no tienen capacidad de gestación
- Se considera que una mujer que sea paciente o bien pareja de un paciente no tiene capacidad de gestación si cumple como mínimo con uno de los siguientes criterios:Edad ≥50 años y con amenorrea natural durante ≥1 año*.
- Insuficiencia ovárica prematura confirmada por un ginecólogo especialista.
- Salpingooforectomía bilateral o histerectomía previas.
- Genotipo XY, síndrome de Turner, agenesia uterina.
*La amenorrea que pueda aparecer después de un tratamiento oncológico o durante la lactancia no descarta la capacidad de gestación.
Asesoramiento: En mujeres con capacidad de gestación, pomalidomida está contraindicada a menos que la paciente cumpla todas las condiciones que se indican a continuación:
- Comprende el riesgo teratogénico esperado para el feto.
- Comprende la necesidad de utilizar dos (2) métodos anticonceptivos eficaces, sin interrupción, desde 4 semanas antes de iniciar el tratamiento, durante la duración completa del mismo y 4 semanas después de finalizarlo.
- Incluso si una mujer con capacidad de gestación tiene amenorrea, debe seguir todos los consejos sobre anticoncepción eficaz.
- Debe ser capaz de cumplir las medidas anticonceptivas eficaces.
- Está informada y comprende las potenciales consecuencias del embarazo, y la necesidad de consultar rápidamente a un especialista si hay riesgo de embarazo.
- Comprende la necesidad de comenzar a utilizar métodos anticonceptivos tan pronto como se le dispense pomalidomida y tras haber obtenido un resultado negativo en la prueba de embarazo.
- Comprende la necesidad de realizar pruebas de embarazo y acepta hacérselas cada 4 semanas, excepto en el caso de que se halla sometido previamente a una ligadura de trompas de eficacia confirmada.
- Confirma que comprende los peligros y las precauciones necesarias asociadas al uso de pomalidomida.
El médico prescriptor debe comprobar que, en el caso de las mujeres con capacidad de gestación:
- La paciente cumple las condiciones del Programa de Prevención de Embarazo, incluida la confirmación de que tiene un nivel de comprensión adecuado.
- La paciente ha aceptado las condiciones mencionadas anteriormente.
En el caso de pacientes varones que toman pomalidomida, los datos farmacocinéticos han demostrado que pomalidomida está presente en el semen humano. Como medida de precaución, todos los pacientes varones que tomen pomalidomida deben cumplir los siguientes requisitos:
- Comprender el riesgo teratogénico esperado si tiene relaciones sexuales con una mujer embarazada o que tenga capacidad de gestación.
- Comprender la necesidad del uso de preservativos si tiene relaciones sexuales con una mujer embarazada o con una mujer con capacidad de gestación que no utiliza métodos anticonceptivos eficaces, durante el tratamiento y durante los 7 días posteriores a la interrupción de la dosis y/o el cese del tratamiento. Los varones vasectomizados deben utilizar preservativos si tienen relaciones sexuales con una mujer embarazada o que tenga capacidad de gestación ya que la pomalidomida puede estar presente en el semen aún en ausencia de espermatozoides.
- Comprender que si su pareja se queda embarazada mientras él está tomando pomalidomida o durante los 7 días posteriores a la suspensión del tratamiento con pomalidomida, debe informar inmediatamente a su médico y es recomendable derivar a su pareja a un médico especialista o con experiencia en teratología para su evaluación y asesoramiento.
Anticoncepción
Las mujeres con capacidad de gestación deben usar dos (2) métodos anticonceptivos eficaces desde 4 semanas antes del tratamiento, durante el tratamiento y hasta 4 semanas después del tratamiento con pomalidomida, e incluso en el caso de interrupción de la administración, a menos que la paciente se comprometa a mantener una abstinencia sexual absoluta y continua, que será confirmada mensualmente. Si la paciente no utiliza dos (2) métodos anticonceptivos eficaces, debe ser derivada a un profesional sanitario debidamente capacitado con objeto de que reciba asesoramiento para empezar a utilizar métodos anticonceptivos. Los siguientes métodos pueden considerarse ejemplos de métodos anticonceptivos adecuados:
- Dispositivo intrauterino (DIU)
- Sistema de liberación intrauterino de levonorgestrel
- Sistemas “depot” de liberación de acetato de medroxiprogesterona
- Ligadura de trompas
- Relaciones sexuales sólo con varones vasectomizados; la eficacia de la vasectomía debe confirmarse mediante dos análisis de semen negativos
- Inhibidores de la ovulación que contienen progestágeno solo (p. ej. desogestrel)
Debido al riesgo aumentado de Tromboembolismo Venoso (TEV) en pacientes con mieloma múltiple que toman pomalidomida y dexametasona, no se recomienda el uso concomitante de anticonceptivos orales combinados. Si una paciente está tomando anticonceptivos orales combinados, debe cambiar a uno de los métodos anticonceptivos eficaces enumerados anteriormente. El riesgo aumentado de tromboembolismo venoso se mantiene durante un período de 4 a 6 semanas después de suspender el tratamiento con anticonceptivos orales combinados. La eficacia de los anticonceptivos esteroideos puede verse reducida durante el tratamiento concomitante con dexametasona. Los dispositivos intrauterinos y los sistemas de liberación intrauterinos de levonorgestrel se asocian con un mayor riesgo de infección en el momento de la colocación y con hemorragia vaginal irregular. En especial en las pacientes con neutropenia debe considerarse el uso profiláctico de antibióticos.
La colocación de dispositivos intrauterinos de liberación de cobre no está recomendada, debido al potencial riesgo de infección en el momento de su colocación y a la pérdida de sangre menstrual, que pueden suponer un peligro para las pacientes con neutropenia grave o trombocitopenia grave.
Pruebas de embarazo
Las mujeres con capacidad de gestación deben efectuarse pruebas de embarazo con una sensibilidad mínima de 50 mUI/ml bajo supervisión médica y conforme a la práctica habitual, tal como se explica a continuación. Este requisito incluye a las mujeres con capacidad de gestación que practican una abstinencia sexual absoluta y continua. Idealmente, la prueba de embarazo, la prescripción y la dispensación deben realizarse el mismo día. Pomalidomida se debe dispensar a las mujeres con capacidad de gestación en un plazo de siete días tras la prescripción. Antes de iniciar el tratamiento
Debe efectuarse una prueba de embarazo bajo supervisión médica durante la consulta, en el momento de prescribir pomalidomida o en los tres días anteriores a la visita al médico prescriptor, siempre que la paciente haya estado usando dos (2) métodos anticonceptivos eficaces durante al menos 4 semanas. La prueba debe garantizar que la paciente no esté embarazada cuando inicie el tratamiento con pomalidomida.
Seguimiento y finalización del tratamiento
Se debe repetir cada 4 semanas una prueba de embarazo bajo supervisión médica, y realizar otra 4 semanas después de la finalización del tratamiento, excepto en el caso de que la paciente se haya sometido a una ligadura de trompas de eficacia confirmada. Estas pruebas de embarazo deben efectuarse el mismo día de la consulta en que se prescriba el medicamento o en los tres días anteriores a la visita al médico prescriptor.
Varones
Pomalidomida está presente en el semen humano durante el tratamiento. Como medida de precaución, y teniendo en cuenta las poblaciones especiales con un tiempo de eliminación potencialmente prolongado, como la insuficiencia renal, todos los pacientes varones que tomen pomalidomida, incluyendo a aquellos que se hayan sometido a una vasectomía, deben usar preservativos durante todo el tratamiento, durante la interrupción de la administración y hasta 7 días después del final del tratamiento, si su pareja está embarazada o tiene capacidad de gestación y no está usando ningún método anticonceptivo. Los pacientes varones no deben donar semen o esperma durante el tratamiento (períodos de interrupción de la dosis incluidos) ni en el plazo de 7 días después de la suspensión del tratamiento con pomalidomida.
Precauciones adicionales
Se debe indicar a los pacientes que no den nunca este medicamento a otra persona y que devuelvan las cápsulas sin usar al final del tratamiento. Los pacientes no deben donar sangre, semen o esperma durante el tratamiento (períodos de interrupción de la dosis incluidos) ni en el plazo de 7 días después de la suspensión del tratamiento con pomalidomida.
Material educativo, restricciones de prescripción y dispensación
Con objeto de ayudar a los pacientes a evitar la exposición fetal a pomalidomida, el Titular de la Autorización de Comercialización distribuirá material educativo a los profesionales sanitarios, destinado a reforzar las advertencias acerca de la teratogenicidad esperada de pomalidomida y a proporcionar asesoramiento sobre anticoncepción antes de iniciar el tratamiento y sobre la necesidad de realizar pruebas de embarazo. El médico debe informar a la paciente acerca del riesgo teratogénico esperado y de las estrictas medidas de prevención de embarazo, especificadas en el Programa de Prevención de Embarazo así como proporcionar a la paciente un folleto informativo adecuado, una tarjeta de paciente y/o una herramienta equivalente conforme al sistema nacional implementado de tarjeta del paciente. Se ha implementado un sistema de distribución nacional controlado. El sistema de distribución controlada incluye el uso de una tarjeta del paciente y/o un herramienta equivalente para el control de la prescripción y/o dispensación, así como la recolección de datos detallados en relación con la indicación terapéutica, para monitorizar el uso en una indicación no autorizada dentro del territorio nacional. Idealmente, la prueba de embarazo, la prescripción y la dispensación deben realizarse el mismo día. La dispensación de pomalidomida en mujeres con capacidad de gestación debe hacerse dentro de los 7 días de prescripción y tras haber obtenido un resultado negativo en la prueba de embarazo supervisada por un médico. Las prescripciones a mujeres con capacidad de gestación deben tener una cantidad máxima de una (1) caja/frasco y las prescripciones para el resto de pacientes pueden tener una cantidad máxima de tres (3) cajas/frascos.
Eventos hematológicos
La reacción adversa hematológica de grado 3 o 4 notificada con mayor frecuencia en pacientes con mieloma múltiple en recaída/refractario fue la neutropenia, seguido de anemia y trombocitopenia. Se debe monitorizar a los pacientes en busca de posibles reacciones adversas hematológicas, especialmente neutropenia. Se debe advertir a los pacientes que informen rápidamente acerca de los episodios febriles que presenten. Los médicos deben estar atentos a los signos de hemorragia en los pacientes, incluyendo epistaxis, especialmente en el caso de medicación concomitante conocida por aumentar el riesgo de sangrado (ver Reacciones adversas). Debe efectuarse a los pacientes un hemograma completo semanal en el momento basal, durante las primeras 8 semanas y después mensualmente. Puede ser necesaria una modificación de la dosis. Los pacientes pueden requerir el uso de hemoderivados y/o factores de crecimiento.
Eventos tromboembólicos
Se han observado eventos tromboembólicos venosos (predominantemente trombosis venosa profunda y embolia pulmonar) y eventos trombóticos arteriales en pacientes tratados con pomalidomida en combinación con dexametasona. Los pacientes con factores de riesgo conocidos de tromboembolismo, incluida una trombosis previa, deben estar estrechamente monitorizados. Se deben tomar medidas para intentar minimizar todos los factores de riesgo modificables (p. ej. tabaquismo, hipertensión e hiperlipidemia). Se aconseja a médicos y pacientes que estén atentos a los signos y síntomas de tromboembolismo. Se debe advertir a los pacientes que soliciten atención médica si presentan síntomas como respiración entrecortada, dolor torácico o edema de las extremidades. Es recomendable el uso de terapia anticoagulante (si no está contraindicada), como el ácido acetilsalicílico, warfarina, heparina o clopidogrel, especialmente en pacientes con factores de riesgo trombótico adicionales. Después de una cuidadosa evaluación de los factores de riesgo subyacentes del paciente individual, se debe tomar una decisión respecto al uso de medidas profilácticas. En los estudiosclínicos los pacientes recibieron ácido aceltilsalicílico profiláctico o terapia antitrombótica alternativa. El uso de agentes eritropoyéticos conlleva un riesgo de eventos trombóticos incluyendo tromboembolismo. Por lo tanto, deben emplearse con precaución los agentes eritropoyéticos así como otros agentes que puedan aumentar el riesgo de eventos tromboembólicos.
Neuropatía periférica
Se excluyó de los estudios clínicos con pomalidomida a los pacientes con neuropatía periférica en curso de grado ≥2. Se deben adoptar las precauciones adecuadas al considerar el tratamiento de estos pacientes con pomalidomida.
Disfunción cardíaca significativa
Se excluyó de los estudios clínicos con pomalidomida a los pacientes con una disfunción cardíaca significativa (insuficiencia cardíaca congestiva [Clase III o IV de la NY Heart Association]; infarto de miocardio dentro de los 12 meses desde el inicio del estudio; angina de pecho inestable o mal controlada). Se han notificado acontecimientos de insuficiencia cardíaca, que incluyen insuficiencia cardíaca congestiva y edema pulmonar (ver Reacciones adversas), especialmente, en pacientes con enfermedad cardíaca preexistente o factores de riesgo cardíacos. Se deben adoptar las precauciones adecuadas al considerar el tratamiento de estos pacientes con pomalidomida, incluido el control periódico para detectar la presencia de signos y síntomas de insuficiencia cardíaca.Síndrome de lisis tumoral
Puede producirse un síndrome de lisis tumoral. Los pacientes con mayor riesgo de sufrir un síndrome de lisis tumoral son aquellos que presentan una carga tumoral elevada antes del tratamiento. Se debe monitorizar estrechamente a estos pacientes y se deben adoptar las precauciones adecuadas.
Segundas neoplasias malignas primarias
Se han notificado segundas neoplasias malignas primarias, como cáncer de piel no melanoma, en pacientes en tratamiento con pomalidomida (ver Reacciones adversas). Los médicos deben evaluar cuidadosamente a los pacientes antes y durante el tratamiento, utilizando pruebas estándar de detección de cáncer por si aparecieran segundas neoplasias malignas primarias e instaurar el tratamiento indicado.
Reacciones alérgicas y reacciones severas en la piel
Se han notificado angioedema y reacciones dermatológicas graves incluyendo SJS, TEN y DRESS con el uso de pomalidomida. Los prescriptores deben informar a los pacientes acerca de los signos y síntomas de estas reacciones y se les debe pedir que busquen atención médica inmediatamente si desarrollan estos síntomas. Pomalidomida debe suspenderse por erupción exfoliativa o ampollosa, o si se sospecha SJS, TEN o DRESS, y no se debe reanudar después de la interrupción de estas reacciones.Se excluyó de los estudios clínicos a los pacientes con antecedentes de reacciones alérgicas graves asociadas a talidomida o lenalidomida. Estos pacientes pueden presentar un mayor riesgo de reacciones de hipersensibilidad y no deben tomar pomalidomida. Se debe considerar la interrupción o suspensión de pomalidomida si se presenta exantema de grado 2 o 3. Se debe suspender definitivamente el tratamiento con pomalidomida si se presenta angioedema.
Mareo y confusión
Se han notificado mareo y estados de confusión con pomalidomida. Los pacientes deben evitar las situaciones en que el mareo o la confusión puedan representar un problema y no tomar otros medicamentos que puedan causar mareo o confusión sin solicitar antes consejo médico.
Enfermedad Pulmonar Intersticial (EPI)
Se han observado EPI y acontecimientos asociados que incluyen casos de neumonitis con pomalidomida. Se debe realizar una evaluación cuidadosa de los pacientes que presenten un inicio repentino o empeoramiento inexplicable de los síntomas pulmonares para descartar la EPI. Se debe interrumpir la administración de pomalidomida durante la investigación de estos síntomas y, si se confirma la EPI, debe iniciarse un tratamiento adecuado. Únicamente se debe reanudar pomalidomida después de una evaluación exhaustiva de los beneficios y los riesgos.
Trastornos hepáticos
Se han observado concentraciones notablemente elevadas de alanina aminotransferasa y bilirrubina en los pacientes tratados con pomalidomida (ver Reacciones adversas). Se han notificado también casos de hepatitis que provocaron la suspensión de pomalidomida. Se recomienda controlar periódicamente la función hepática durante los primeros 6 meses de tratamiento con pomalidomida y, posteriormente, cuando esté clínicamente indicado. Infecciones
Se han notificado rara vez casos de reactivación de la hepatitis B en pacientes en tratamiento con pomalidomida combinado con dexametasona que habían sido previamente infectados por el virus de la hepatitis B (VHB). Algunos de estos casos han evolucionado a fallo hepático agudo, dando lugar a la suspensión de pomalidomida. Se debe determinar el estado del virus de la hepatitis B antes de iniciar el tratamiento con pomalidomida. Se recomienda que los pacientes que den un resultado positivo en la prueba de infección por VHB se pongan en contacto con un médico con experiencia en el tratamiento de la hepatitis B. Se debe tener precaución cuando se administre pomalidomida en combinación con dexametasona en pacientes previamente infectados por el VHB, incluidos los pacientes anti-Bc positivos pero con HBsAg negativos. Se debe monitorizar estrechamente a estos pacientes para detectar signos y síntomas de infección activa por el VHB durante todo el tratamiento.
Aumento de la mortalidad en pacientes con mieloma múltiple cuando se agrega pembrolizumab a un análogo de talidomida y dexametasona
En dos ensayos clínicos aleatorizados en pacientes con mieloma múltiple, la adición de pembrolizumab a un análogo de la talidomida más dexametasona, un uso para el cual no está indicado el anticuerpo bloqueante PD-1 o PD-L1, dio como resultado un aumento de la mortalidad. No se recomienda el tratamiento de pacientes con mieloma múltiple con un anticuerpo bloqueante PD-1 o PD-L1 en combinación con un análogo de la talidomida más dexametasona fuera de los ensayos clínicos controlados.
Fertilidad, embarazo y lactancia
Mujeres con capacidad de gestación / Anticonceptivos en varones y mujeres
Las mujeres con capacidad de gestación deben utilizar dos (2) métodos anticonceptivos efectivos. Si una mujer tratada con pomalidomida se queda embarazada, se debe suspender el tratamiento y derivar a la paciente a un médico especialista o con experiencia en teratología, para su evaluación y asesoramiento. Si un paciente varón toma pomalidomida y su pareja queda embarazada, se recomienda derivar a la mujer a un médico especialista o con experiencia en teratología, para su evaluación y asesoramiento. Pomalidomida está presente en el semen humano. Como medida de precaución, todos los pacientes varones que tomen pomalidomida deben usar preservativos durante todo el tratamiento, durante la interrupción de la administración y hasta 7 días después del final del tratamiento, si su pareja está embarazada o tiene capacidad de gestación y no está usando ningún método anticonceptivo.
Embarazo
Se espera un efecto teratogénico de pomalidomida en humanos. Pomalidomida está contraindicada durante el embarazo y en mujeres con capacidad de gestación, a menos que se cumplan todas las condiciones para la prevención del embarazo.
Lactancia
Se desconoce si pomalidomida se excreta en la leche materna. Se detectó la presencia de pomalidomida en la leche de ratas que estaban siendo amamantadas tras administrar el medicamento a la madre. Debido a las posibles reacciones adversas en lactantes asociadas a pomalidomida, se debe decidir si es necesario suspender la lactancia o suspender el tratamiento tras considerar la importancia del tratamiento para la madre.
Fertilidad
Se sabe que pomalidomida tiene un efecto negativo sobre la fertilidad y que es teratogénica en los animales. Tras su administración a conejas preñadas, pomalidomida atravesó la placenta y se detectó en la sangre fetal.
Carcinogénesis, mutagénesis y fertilidad
Datos preclínicos sobre seguridad
Estudios de toxicidad de dosis repetidas
La administración crónica de pomalidomida en ratas en dosis de 50, 250 y 1000 mg/kg/día durante 6 meses fue bien tolerada. No se detectó ningún efecto adverso hasta los 1000 mg/kg/día (una tasa de exposición 175 veces más elevada que la dosis clínica de 4 mg).
Se evaluó pomalidomida en monos en estudios de dosis repetidas de hasta 9 meses de duración. En estos estudios, los monos mostraron una mayor sensibilidad a los efectos de pomalidomida que las ratas. Las toxicidades primarias observadas en monos estuvieron relacionadas con los sistemas hematopoyético/linforreticular. En el estudio de 9 meses en monos con dosis de 0,05, 0,1 y 1 mg/kg/día se observó morbilidad y eutanasia temprana de 6 animales a dosis de 1 mg/kg/día que fueron atribuidas a los efectos inmunosupresores (infección por estafilococos, reducción de los linfocitos en sangre periférica, inflamación crónica del intestino grueso, reducción histológica de los linfocitos e hipocelularidad de la médula ósea) a exposiciones elevadas de pomalidomida (15 veces la tasa de exposición comparada con una dosis clínica de 4 mg). Dichos efectos inmunosupresores provocaron la eutanasia temprana de 4 monos debido a su mal estado de salud (heces líquidas, inapetencia, ingesta de alimentos reducida y pérdida de peso); la evaluación histopatológica de estos animales demostró inflamación crónica del intestino grueso y atrofia vellosa del intestino delgado. Se observó infección por estafilococos en 4 monos; 3 de éstos respondieron al tratamiento con antibióticos y uno murió sin tratamiento. Además, resultados consistentes con la leucemia mielógena aguda llevaron a la eutanasia de un mono; las observaciones clínicas y la patología clínica y/o alteraciones de la médula ósea observadas en este animal eran consistentes con inmunosupresión. La proliferación mínima o leve en los conductos biliares con incrementos asociados de la ALP y de la GGT también se observaron a dosis de 1 mg/kg/día. La evaluación de los animales recuperados indicó que todos los resultados relacionados con el tratamiento eran reversibles a las 8 semanas del cese de la administración, excepto la proliferación de los conductos biliares intrahepáticos observada en 1 animal en el grupo de 1 mg/kg/día. El nivel sin efecto adverso observado (NOAEL) fue de 0,1 mg/kg/día (una tasa de exposición relativa de 0,5 veces comparada con la dosis clínica de 4 mg).
Genotoxicidad/carcinogenicidad
Pomalidomida no resultó mutagénica en los ensayos de mutaciones bacterianas y de los mamíferos, y no indujo aberraciones cromosómicas en los linfocitos de sangre periférica en humanos así como tampoco a la formación de micronúcleos en eritrocitos policromáticos en la médula ósea de ratas a las que les fueron administradas dosis de hasta 2000 mg/kg/día. No se han realizado estudios de carcinogenicidad.
Fertilidad y desarrollo embrionario temprano En un estudio de fertilidad y desarrollo embrionario temprano en ratas, se administró pomalidomida a los machos y las hembras a dosis de 25, 250 y 1000 mg/kg/día. El examen uterino en el día de gestación 13 mostró una reducción de la cantidad media de embriones viables y un aumento en la pérdida post-implantación con todos los niveles de dosis. Por consiguiente, el NOAEL en estos eventos observados fue <25 mg/kg/día (con un AUC24h de 39960 ng*h/ml (nanogramo por hora/mililitros) para la dosis más baja evaluada y una tasa de exposición 99 veces relativa a la dosis clínica de 4 mg). Cuando los machos tratados en este estudio fueron apareados con hembras no tratadas, todos los parámetros uterinos fueron comparables a los controles. Según estos resultados, los efectos observados fueron atribuidos al tratamiento de las hembras.
Desarrollo embriofetal
Pomalidomida resultó ser teratógena en ratas y conejos cuando se administró durante el período de mayor organogénesis. En el estudio de toxicidad sobre el desarrollo embriofetal de la rata, se observaron malformaciones relacionadas con la ausencia de vejiga urinaria, ausencia de la glándula tiroidea, así como la fusión y la desalineación de los elementos vertebrales torácicos y lumbares (arcos centrales y/o neurales) a todos los niveles de dosis (25, 50 y 1000 mg/kg/día).
En este estudio no se observó toxicidad materna. Por ello, el NOAEL materno fue de 1000 mg/kg/día, y el NOAEL para la toxicidad de desarrollo fue <25 mg/kg/día (con un AUC24h de 34340 ng·h/ml en el día de gestación 17 para la dosis más baja evaluada y la tasa de exposición fue de 85 veces comparada con la dosis clínica de 4 mg). En conejos, pomalidomida a dosis entre los 10 y 250 mg/kg/día produjo malformaciones en el desarrollo embriofetal. Se observaron aumentos de las anomalías cardíacas a todas las dosis con aumentos significativos a 250 mg/kg/día. A dosis de entre 100 y 250 mg/kg/día se registró un ligero aumento de la pérdida post-implantación y un ligero descenso en el peso del feto. A dosis de 250 mg/kg/día, las malformaciones fetales incluyeron anomalías en las extremidades (extremidades anteriores y posteriores dobladas y/o giradas, ausencia de dígito o dígito libre) y malformaciones esqueléticas asociadas (metacarpiano no osificado, metacarpiano y falange no alineados, ausencia de dígito, falange no osificada y tibia corta no osificada o doblada); dilatación moderada de los ventrículos laterales del cerebro; ubicación anormal de la arteria subclavia derecha; ausencia de los lóbulos intermedios pulmonares; par de riñones desplazados hacia abajo; morfología hepática alterada; ausencia de osificación de la pelvis u osificación incompleta; aumento medio de las costillas torácicas supernumerarias y reducción media de los tarsales osificados. Además, se observó una ligera reducción en el incremento del peso materno, una reducción significativa de los triglicéridos, y una reducción significativa del peso absoluto y relativo del bazo a dosis de entre 100 y 250 mg/kg/día. El NOAEL materno fue de 10 mg/kg/día y el NOAEL del desarrollo fue de <10 mg/kg/día (con un AUC24h de 418 ng·h/ml en el día de gestación 19 para la dosis más baja evaluada, similar a la obtenida con una dosis clínica de 4 mg).
DOSIS Y VÍAS DE ADMINISTRACIÓN:
Posología, dosificación y administración: El tratamiento debe iniciarse y monitorizarse bajo la supervisión de médicos con experiencia en el tratamiento del mieloma múltiple.
Posología: La dosis inicial recomendada es de 4 mg de POMALYST una vez al día por vía oral, en los días del 1 al 21 de ciclos repetidos de 28 días. La dosis recomendada de dexametasona es de 40 mg por vía oral una vez al día, en los días 1, 8, 15 y 22 de cada ciclo de tratamiento. La posología se mantiene o modifica en función de los resultados clínicos y de laboratorio.
El tratamiento debe suspenderse si existe evidencia de progresión de la enfermedad.
Modificación o interrupción de la dosis de pomalidomida: Las instrucciones para la interrupción y reducción de la dosis de pomalidomida relacionada con reacciones adversas hematológicas se indican en la siguiente tabla:
|
Instrucciones para la modificación |
|
|
Toxicidad |
Modififación de la dosis |
|
Neutropenia |
|
|
RAN* <0,5X109/l o neutropenai febril (fiebre >38,5°C y RAN <1 x 109/l) |
Interrumpir el tratamiento con pomalidomida, control semanal del hemograma completo. |
|
RAN vuelve a >1 x109/l |
Reanudar el tratamiento con 3 mg de pomalidomida al día. |
|
Con cada disminución posterior a <0;5 x 109/l |
Interrumpir el tratamiento con pomalidomida. |
|
RAN vuelve a >1 x109/l |
Reanudar el tratamiento con 1 mg de pomalidomida que la dosis previa. |
|
Trombocitopenia |
|
|
Recuento de plaquetas <25 x109/l |
Interrumpir el tratamiento con pomalidomida, control semanal del hemograma completo. |
|
Recuento de plaquetas vuelve a >50 x 10 9/l |
Reanudar el tratamiento con 3 mg de pomalidomida al día. |
|
Con cada disminución posterior a <25 x 10 9/l |
Interrumpir el tratamiento con pomalidomida. |
|
Recuento de plaquetas vuelve a >50 x 10 9/l |
Reanudar el tratamiento con 1 mg menos de pomalidomida que la dosis previa. |
|
*RAN - Recuento Absoluto de Neutrófilos |
|
Para iniciar un nuevo ciclo de pomalidomida, el recuento de neutrófilos debe ser ≥1 x 109/l y el recuento de plaquetas debe ser ≥50 x 109/l.
En caso de neutropenia, el médico debe considerar el uso de factores de crecimiento.
En el caso de otras reacciones adversas de grado 3 o 4 relacionadas con pomalidomida, el médico debe considerar interrumpir el tratamiento y reanudarlo con un 1 mg menos que la dosis previa una vez que se haya disminuido la reacción adversa a un grado inferior o igual a 2.
Si la reacción adversa ocurre tras disminuciones de la dosis a 1 mg, entonces debe suspenderse el tratamiento con este medicamento.
Se debe considerar la interrupción o suspensión de pomalidomida en caso de exantema de grado 2-3. Se debe suspender el tratamiento con pomalidomida en caso de angioedema, exantema de grado 4 y exantema ampolloso o exfoliativo, y no se debe reanudar una vez suspendido por estas reacciones. Si se administran inhibidores potentes del CYP1A2 (p. ej., ciprofloxacino, enoxacino y fluvoxamina) de forma concomitante con pomalidomida, se debe reducir la dosis de pomalidomida en un 50 %.
|
Instrucciones para la modificación de la dosis de dexametasona |
|
|
Toxicidad |
Modificación de la dosis |
|
Dispepsia = grado 1-2 |
Mantener la dosis y tratar con antihistamínicos H2 o equivalentes. Reducir la dosis en un nivel de dosis si los síntomas persisten. Interrumpir la administración hasta que se controlen los síntomas. Añadir antihistamínicos H2 o equivalentes y reducir la dosis en un nivel cuando se reanude su administración. |
|
Dispepsia ≥ grado 3 |
|
|
Edema ≥ grado 3 |
Usar diuréticos según sea necesario y reducir la dosis en un nivel de dosis. |
|
Confusión o cambios en el estado de ánimo ≥ grado 2 |
Interrumpir la administración hasta que desaparezcan los síntomas. Cuando se reanude su administración reducir la dosis en un nivel de dosis. |
|
Debilidad muscular ≥ grado 2 |
Interrumpir la administración hasta que la debilidad muscular sea ≤ grado 1. Reiniciar la dosis con una reducción de un nivel. |
|
Hiperglucemia ≥ grado 3 |
Reducir la dosis en un nivel de dosis. Tratar con insulina o hipoglucemiantes orales según sea necesario. |
|
Pancreatitis aguda |
Suspensión de dexametasona del régimen de tratamiento del paciente. |
|
Otros efectos adversos relacionados con dexametasona ≥ grado 3 |
Interrumpir la administración de dexametasona hasta que los efectos adversos sean de grado≤ 2. Reanudar su administración con una reducción de un nivel de la dosis. |
Niveles de reducción de la dosis de dexametasona:
Niveles de reducción de la dosis (≤75 años de edad): dosis inicial= 40 mg; nivel de dosis -1= 20 mg; nivel de dosis -2= 1O mg en los días 1, 8, 15 y 22 de cada ciclo de tratamiento de 28 días.
Niveles de reducción de la dosis (>75 años de edad): dosis inicial= 20 mg; nivel de dosis -1= 12 mg; nivel de dosis -2= 8 mg en los días 1, 8, 15 y 22 de cada ciclo de tratamiento de 28 días.
Si la recuperación de las toxicidades tarda más de 14 días, la dosis de dexametasona se reducirá en un nivel de dosis.
Poblaciones especiales
Población pediátrica: No existe una recomendación de uso específica para POMALYST en niños de 0 a 17 años para la indicación del mieloma múltiple.
Pacientes de edad avanzada: No se requiere ningún ajuste de dosis de pomalidomida. En pacientes de >75 años de edad, la dosis inicial de dexametasona es de 20 mg una vez al día en los días 1, 8, 15 y 22 de cada ciclo de tratamiento de 28 días.
Insuficiencia renal: No se requiere ningún ajuste de dosis de pomalidomida en los pacientes con insuficiencia renal. Los días de hemodiálisis, los pacientes deben tomar la dosis de pomalidomida después de la hemodiálisis. Insuficiencia hepática: Los pacientes con una concentración sérica de bilirrubina total >2,0 mg/dl se excluyeron de los estudios clínicos. La insuficiencia hepática tiene un efecto modesto sobre la farmacocinética de pomalidomida (ver Acción farmacocinética). No se requiere ajustar la dosis inicial de pomalidomida en pacientes con insuficiencia hepática según definen los criterios de Child Pugh. Sin embargo, los pacientes con insuficiencia hepática deben ser monitorizados cuidadosamente por la aparición de reacciones adversas y se debe reducir la dosis o suspender la administración de pomalidomida según sea necesario.
Forma de administración: Vía oral.
POMALYST debe tomarse a la misma hora cada día. Las cápsulas no deben abrirse, romperse ni masticarse. Este medicamento debe tomarse entero, preferiblemente con agua, con o sin alimentos. Si el paciente olvida tomar una dosis de POMALYST un día, el paciente debe entonces tomar la próxima dosis al día siguiente a la hora habitual. Los pacientes no deben ajustar la dosis para compensar una dosis olvidada en días anteriores.
MANIFESTACIONES Y MANEJO DE LA SOBREDOSIFICACIÓN O INGESTA ACCIDENTAL:
Sobredosis y tratamiento: Se han evaluado dosis de pomalidomida de hasta 50 mg en dosis única en voluntarios sanos y 10 mg en múltiples dosis una vez al día en pacientes con mieloma múltiple sin que se haya notificado ningún caso de efecto adverso grave relacionado con sobredosis. Pomalidomida se eliminó mediante hemodiálisis.
En caso de sobredosis, se recomienda terapia de soporte.ANTE LA EVENTUALIDAD DE UNA SOBREDOSIFICACIÓN, CONCURRIR AL HOSPITAL MÁS CERCANO O COMUNICARSE CON LABORATORIOS MEDICAMENTA ECUATORIANA AL TELÉFONO PBX 5005005
PRESENTACIÓN:
POMALYST 1 mg cápsula dura: tapa opaca de color azul oscuro y cuerpo opaco de color amarillo con la inscripción “POML 1 mg”.
POMALYST 2 mg cápsula dura: tapa opaca de color azul oscuro y cuerpo opaco de color naranja con la inscripción “POML 2 mg”.
POMALYST 3 mg cápsula dura: tapa opaca de color azul oscuro y cuerpo opaco de color verde con la inscripción “POML 3 mg”.
POMALYST 4 mg cápsula dura: tapa opaca de color azul oscuro y cuerpo opaco de color azul con la inscripción “POML 4 mg”.
Cada envase contiene 21 cápsulas.
RECOMENDACIONES SOBRE ALMACENAMIENTO:
Conservación
Conservar a temperatura no mayor a 30 °C.
LEYENDAS DE PROTECCIÓN:
Todo medicamento debe mantenerse fuera del alcance de los niños.
Este medicamento se encuentra dentro del plan de farmacovigilancia activa, y presenta plan de gestión de riesgo.
Este medicamento solo debe utilizarse bajo estricto control y vigilancia médica y no puede repetirse sin nueva receta.