
PULMICORT 0,5 MG/ML
BUDESONIDA
Solución para nebulizador
1 Caja,20 Unidades monodosis,2 ml
Para visualizar el contenido completo de la IPPA (información para prescribir amplia), deberá iniciar sesión.
COMPOSICIÓN CUALITATIVA Y CUANTITATIVA: Cada unidad monodosis de 2 ml contiene 1 mg de budesonida.
LISTA DE EXCIPIENTES: Edetato disódico, cloruro de sodio, polisorbato 80, ácido cítrico anhidro, citrato de sodio, agua para preparaciones inyectables.
INDICACIONES TERAPÉUTICAS: Tratamiento del asma bronquial. Tratamiento de la laringotraqueobronquitis aguda (CRUP) en bebés y niños.
FORMA FARMACÉUTICA: Suspensión para nebulización estéril. Suspensión blanquecina en una unidad monodosis de plástico.
PROPIEDADES FARMACOCINÉTICAS
Absorción: La budesonida inhalada se absorbe rápidamente. La concentración plasmática máxima se alcanza 30 minutos después de empezar la nebulización.
Distribución y metabolismo: La unión a las proteínas plasmáticas representa aproximadamente un 90% y el volumen de distribución es de alrededor de 3 litros/kg. La budesonida es objeto de una extensa biotransformación hepática de primer paso (alrededor del 90%), convirtiéndose en metabolitos con una baja actividad glucocorticoide. La actividad glucocorticoide de los principales metabolitos, la 6-ß-hidroxibudesonida y la 16-a-hidroxiprednisolona, es inferior al 1% de la actividad de la budesonida.
Eliminación: La budesonida se elimina por metabolismo, catalizado principalmente por la enzima CYP3A4. Los metabolitos se eliminan en la orina en forma intacta o conjugada. Solo se han detectado cantidades insignificantes de budesonida intacta en la orina. La budesonida muestra una alta depuración sistémica (aproximadamente 1.2 litros/min) y su vida media de eliminación plasmática después de la administración intravenosa es de 4 horas en promedio. La farmacocinética de la budesonida es proporcional a la dosis dentro de los límites terapéuticos.
Se desconoce la farmacocinética de la budesonida en niños y en pacientes con insuficiencia renal. La exposición a la budesonida podría aumentar en los pacientes con insuficiencia hepática.
PROPIEDADES FARMACODINÁMICAS: La budesonida es un glucocorticoide con un potente efecto antiinflamatorio local.
Grupo farmacoterapéutico: Fármacos inhalados para enfermedades obstructivas de las vías respiratorias.
Código ATC: R03B A02.
No se conoce el mecanismo de acción preciso de los glucocorticoides en el tratamiento del asma. Es probable que revistan importancia sus efectos antiinflamatorios tales como la inhibición de la liberación de mediadores inflamatorios y la inhibición de la respuesta inmunitaria mediada por las citocinas. La actividad de la budesonida, medida según su afinidad por los receptores de glucocorticoides, es aproximadamente 15 veces mayor que la de la prednisolona.
La budesonida ejerce efectos antiinflamatorios que se manifiestan con una disminución de la obstrucción bronquial en las fases inmediata y retrasada de la reacción alérgica. En pacientes hiperreactivos, la budesonida reduce la sensibilidad de las vías respiratorias a la histamina y la metacolina.
Los estudios han demostrado que cuanto más pronto se inicie el tratamiento con la budesonida después de la aparición del asma, mejor será la función pulmonar.
Los estudios en voluntarios sanos mostraron que PULMICORT® Turbuhaler ejerce efectos en las concentraciones plasmáticas y urinarias de cortisol en función de la dosis. Con las dosis recomendadas, PULMICORT® Turbuhaler produce un efecto en la función suprarrenal significativamente menor que 10 mg de prednisona, según las pruebas de estimulación con ACTH.
En niños mayores de 3 años no se han detectado efectos sistémicos con dosis de hasta 400 microgramos al día. Con dosis de 400 a 800 microgramos al día pueden presentarse signos bioquímicos de un efecto sistémico. Con dosis diarias superiores a 800 mg tales signos son frecuentes. Esta información se aplica a PULMICORT® tanto en aerosol para inhalación como en polvo para inhalación.
Aunque tanto el asma en sí como los corticoesteroides inhalados pueden provocar un retraso del crecimiento, estudios a largo plazo han demostrado que los niños y adolescentes tratados con la budesonida inhalada alcanzan finalmente la estatura prevista a la edad adulta. Sin embargo, se ha observado una reducción inicial pequeña pero transitoria del crecimiento (de aproximadamente 1 cm), generalmente durante el primer año de tratamiento.
El tratamiento inhalado con la budesonida es eficaz para la prevención del asma provocada por el esfuerzo.
CONTRAINDICACIONES: Hipersensibilidad al medicamento, primer trimestre del embarazo, tuberculosis pulmonar activa o quiescente, status asmaticus. Adminístrese con precaución a pacientes con insuficiencia cardiaca congestiva grave e hipertensión arterial.
USO DURANTE EL EMBARAZO Y LA LACTANCIA
Embarazo: Los datos de aproximadamente 2000 embarazos no han revelado un aumento del riesgo de malformaciones a raíz del tratamiento con la budesonida. Los estudios en animales han demostrado que los glucocorticoides pueden provocar malformaciones (véase Datos de toxicidad preclínica), pero estos efectos no se consideran relevantes con la dosis recomendada para el ser humano.
Los estudios en animales también han revelado que la administración prenatal de un exceso de glucocorticoides puede contribuir a elevar el riesgo de retraso del crecimiento intrauterino, de enfermedad cardiovascular a la edad adulta, de alteraciones permanentes de la densidad de los receptores de glucocorticoides, y del metabolismo y el comportamiento de los neurotransmisores, con exposiciones inferiores a las producidas por dosis teratógenas.
Durante el embarazo, el objetivo debe ser administrar la dosis mínima de budesonida que sea eficaz, tomando en cuenta el riesgo de deterioro del asma.
Lactancia: La budesonida se excreta en la leche materna humana. Sin embargo, no se prevén efectos en el lactante si se usan dosis terapéuticas de PULMICORT® en suspensión para nebulización. PULMICORT® en suspensión para nebulización puede emplearse durante la lactancia, úsese solo si sus beneficios superan ampliamente sus riesgos.
EFECTOS SOBRE LA CAPACIDAD PARA CONDUCIR Y UTILIZAR MÁQUINAS: PULMICORT® no afecta la capacidad para conducir y utilizar máquinas.
REACCIONES ADVERSAS: Hasta el 10% de los pacientes tratados normalmente presentarán reacciones adversas de naturaleza local.
|
Reacciones frecuentes (>1/100) |
Vías respiratorias: |
Candidiasis orofaríngea, irritación leve de la garganta, tos, ronquera |
|
Reacciones |
Trastornos generales: |
Angioedema, reacción anafiláctica |
|
SNC: |
Nerviosismo, desasosiego, depresión, trastornos del comportamiento |
|
|
Piel: |
Urticaria, exantema, dermatitis, equimosis |
|
|
Vías respiratorias: |
Broncoespasmo |
En vista del riesgo de candidiasis orofaríngea, el paciente debe enjuagarse la boca con agua después de cada dosis.
Con los glucocorticoides inhalados pueden presentarse raramente signos o síntomas de efectos glucocorticoides sistémicos, lo cual puede incluir una disminución de la función suprarrenal y una reducción de la velocidad de crecimiento probablemente en función de la dosis, del tiempo de exposición, de la exposición previa y concomitante a corticoesteroides, y de la susceptibilidad individual.
Se han observado algunos casos de irritación facial al utilizar una mascarilla. Para evitar esta reacción, el paciente debe lavarse la cara después de usar la mascarilla.
INCOMPATIBILIDADES: PULMICORT® en suspensión para nebulización no debe mezclarse con medicamentos diferentes de los mencionados en el apartado Instrucciones para utilizar correctamente el nebulizador.
INTERACCIONES CON OTROS MEDICAMENTOS Y OTRAS FORMAS DE INTERACCIÓN: No se conocen interacciones clínicas importantes entre la budesonida y otros medicamentos antiasmáticos.
La administración concomitante de 200 mg de ketoconazol una vez al día aumentó seis veces en promedio las concentraciones plasmáticas de la budesonida oral (3 mg en una dosis única). Al administrar el ketoconazol 12 horas después de la budesonida, la concentración aumentó en promedio tres veces. Se carece de información acerca de esta interacción con la budesonida inhalada pero también se prevé un aumento considerable de las concentraciones plasmáticas con esta vía de administración. Esta combinación debe evitarse ya que no hay datos que permitan recomendar una determinada dosis. Si esto es imposible, el intervalo entre las administraciones del ketoconazol y de la budesonida debe ser lo más largo posible. También debe contemplarse una disminución de la dosis de budesonida. Otros inhibidores potentes de la enzima CYP3A4, como el itraconazol, también provocan aumentos pronunciados de las concentraciones plasmáticas de budesonida.
DATOS DE TOXICIDAD PRECLÍNICA: En estudios de toxicidad, la budesonida ha provocado únicamente los efectos esperados de los glucocorticoides.
La budesonida no ejerce efectos genotóxicos.
En estudios sobre la reproducción en animales, se demostró que los corticoesteroides como la budesonida provocan malformaciones (palatosquisis, malformaciones del esqueleto); sin embargo, estos resultados experimentales obtenidos en animales no parecen revestir importancia alguna para el ser humano al usar las dosis recomendadas.
ADVERTENCIAS Y PRECAUCIONES ESPECIALES DE EMPLEO: Para minimizar el riesgo de candidiasis en la cavidad bucal y la garganta, el paciente debe enjuagarse la boca con agua después de la administración de cada dosis.
Úsese durante la lactancia solo si sus beneficios superan ampliamente sus riesgos.
Debe evitarse el tratamiento concomitante con el ketoconazol, el itraconazol u otros inhibidores potentes de la enzima CYP3A4. Si esto es imposible, el intervalo entre las administraciones de los medicamentos debe ser lo más largo posible (véase Interacciones con otros medicamentos y otras formas de interacción).
Se necesita un cuidado particular en los pacientes que cambian de un tratamiento con corticoesteroides orales a PULMICORT® ya que el riesgo de deficiencia suprarrenal puede persistir durante un tiempo considerable. También pueden estar expuestos a este riesgo los pacientes que hayan necesitado un tratamiento de emergencia con dosis altas de corticoesteroides o un tratamiento prolongado con la máxima dosis recomendada de corticoesteroides inhalados. Tales pacientes pueden presentar signos y síntomas de insuficiencia suprarrenal en caso de estrés intenso. Durante los periodos de estrés o si se programa una cirugía, debe contemplarse la adición de un tratamiento con corticoesteroides sistémicos.
Al cambiar de un tratamiento con corticoesteroides orales a PULMICORT®, pueden reaparecer síntomas anteriores tales como dolor muscular y articular. En tales casos puede ser necesario aumentar temporalmente la dosis del corticoesteroide oral. Si en casos aislados se presentan cansancio, cefalea, náuseas, vómito o síntomas similares, debe sospecharse de un efecto insuficiente del corticoesteroide.
El cambio de un tratamiento con un corticoesteroide sistémico a PULMICORT® a veces revela la existencia de alergias, por ejemplo rinitis y eccema, que antes eran controladas por el tratamiento sistémico.
Se recomienda vigilar regularmente el crecimiento de los niños y adolescentes que reciben un tratamiento a largo plazo con corticoesteroides, independientemente de la vía de administración. Los beneficios del tratamiento con corticoesteroides deben sopesarse con respecto a los posibles riesgos de inhibición del crecimiento.
Como con otros tratamientos inhalados, puede ocurrir un broncoespasmo paradójico justo después de la administración. Si la reacción es intensa, debe reconsiderarse el tratamiento y, si es necesario, prescribir un tratamiento alternativo.
Debe indicarse a los pacientes que consulten a su médico si disminuye el efecto general del tratamiento porque las inhalaciones repetidas para ataques agudos de asma no deben retrasar la instauración de otro tratamiento importante. En caso de deterioro repentino, el tratamiento debe complementarse con la administración de corticoesteroides orales durante un periodo corto.
La disfunción hepática puede afectar la capacidad para eliminar la budesonida.
PRECAUCIONES ESPECIALES DE CONSERVACIÓN: No almacenar a más de 30 °C. No congelar.
Las unidades cerradas siempre deben conservarse en el sobre de aluminio y conservarse en posición recta en un lugar protegido de la luz.
Una vez abierto el sobre de aluminio, las unidades monodosis no usadas deben conservarse en el sobre para protegerlas de la luz.
Las unidades monodosis guardadas en un sobre abierto deben usarse en un plazo máximo de 3 meses. Una vez que se haya abierto una unidad monodosis, su contenido debe usarse en las 12 horas siguientes. Nótese que aunque se utilice solamente 1 ml, el volumen restante dejará de ser estéril.
Tamaño del envase: Consultar el tamaño del envase en la caja de cartón externa.
Modo de empleo de PULMICORT® para nebulización
1. Antes de utilizarla, agitar suavemente en círculos la unidad monodosis para poner el contenido en suspensión.
2. Sostener la unidad monodosis en posición vertical (véase el dibujo) y abrirla girando la aleta. .
3. Introducir perfectamente el extremo abierto de la unidad en el depósito del nebulizador y apretar suavemente.
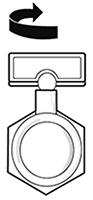
La unidad monodosis lleva una línea (solamente en el caso de PULMICORT® 0.25 mg/ml y 0.5 mg/ml) que indica el volumen de 1 ml al invertir la unidad monodosis boca abajo.
Si se va a utilizar solamente 1 ml, vaciar el contenido hasta que el nivel del líquido llegue a la línea indicadora.
Las unidades monodosis abiertas deben protegerse de la luz y utilizarse en un plazo máximo de 12 horas.
Nótese que aunque se utilice solamente 1 ml, el volumen restante dejará de ser estéril.
Antes de utilizar el resto del líquido, volver a poner en suspensión el contenido de la unidad monodosis agitándola suavemente en círculos.
NOTA
1. Enjuáguese la boca con agua después de cada administración.
2. Si utiliza una mascarilla, asegúrese de que esté bien ajustada durante la inhalación. Lávese la cara después del tratamiento.
Limpieza: La cámara del nebulizador y la boquilla (o la mascarilla) deben limpiarse después de cada administración. Lavar las piezas del nebulizador con agua caliente utilizando un detergente suave o siguiendo las instrucciones del fabricante. Enjuagarlas perfectamente y secarlas conectando la cámara del nebulizador al compresor o a la entrada de aire.
Venta con fórmula médica. Mantener fuera del alcance de los niños.
POSOLOGÍA Y FORMA DE ADMINISTRACIÓN: La dosis de la suspensión PULMICORT® para nebulización es individual. Las dosis diarias de hasta 1 mg pueden aplicarse en una sola administración. Las dosis mayores deben dividirse en dos administraciones al día.
Asma
Inicialmente debe utilizarse la dosis siguiente:
Niños mayores de 6 meses: de 0.25 a 0.5 mg al día. Si es necesario, la dosis puede aumentarse hasta 1 mg al día.
Adultos: de 1 a 2 mg al día.
Para el tratamiento de mantenimiento:
Niños mayores de 6 meses: de 0.25 a 2 mg al día.
Adultos: de 0.5 a 4 mg al día. En los casos muy graves, la dosis puede aumentarse aún más.
Laringotraqueobronquitis (crup): En bebés y niños con crup, la dosis usual consiste en una sola administración de 2 mg de budesonida nebulizada.
|
Cuadro de dosis |
||
|
Dosis (mg) |
Volumen de suspensión PULMICORT® para nebulización |
|
|
0.25 mg/ml |
0.5 mg/ml |
|
|
0.25 |
1 ml* |
— |
|
0.5 |
2 ml |
— |
|
0.75 |
3 ml |
— |
|
1 |
4 ml |
2 ml |
|
1.5 |
- |
3 ml |
|
2 |
- |
4 ml |
|
* debe diluirse a 2 ml con solución salina al 0.9% o con una solución para nebulización (véase Instrucciones para utilizar correctamente el nebulizador). |
||
La dosis de mantenimiento debe ser la más baja posible.
Después de la administración de una dosis única, el efecto normalmente se manifiesta en unas cuantas horas. El efecto terapéutico máximo se alcanza solamente después de varias semanas de tratamiento. PULMICORT® está indicado para la profilaxis pero su efecto no se ha comprobado en las afecciones agudas.
Cuando se desee obtener un mayor efecto terapéutico, generalmente es preferible aumentar la dosis de PULMICORT® en lugar de combinarlo con corticoesteroides orales a fin de limitar el riesgo de efectos secundarios sistémicos.
Pacientes dependientes de corticoesteroides orales: Para pasar de un tratamiento con corticoesteroides orales a PULMICORT®, el paciente debe encontrarse en un estado relativamente estable. Primero debe administrarse durante 10 días una dosis alta de PULMICORT® junto con la dosis del corticoesteroide oral que utilizaba el paciente. Luego la dosis debe reducirse progresivamente, por ejemplo por etapas mensuales de 2.5 mg de prednisolona o equivalentes, hasta llegar al nivel mínimo posible. En muchos casos el corticoesteroide oral puede suspenderse por completo.
Ya que la budesonida administrada con PULMICORT® en suspensión para nebulización llega a los pulmones con el aire inspirado, es importante que el paciente inhale tranquilamente y de manera regular por la boquilla del nebulizador.
Se carece de experiencia sobre el tratamiento en pacientes con disfunción hepática o renal. Ya que la budesonida se elimina principalmente por metabolismo hepático, es de esperarse que la exposición será mayor en pacientes con cirrosis hepática grave. .
Instrucciones para utilizar correctamente el nebulizador: PULMICORT® en suspensión para nebulización debe administrarse con un nebulizador mecánico equipado con una boquilla o una mascarilla adecuada. El nebulizador debe conectarse a un compresor con un flujo de aire adecuado (de 5 a 8 litros por minuto) y el volumen de llenado debe ser de 2 a 4 ml.
Nota: Es importante señalar al paciente que:
• Debe leer cuidadosamente el Modo de empleo de PULMICORT® en suspensión para nebulización.
• Los nebulizadores ultrasónicos no son adecuados para administrar PULMICORT® en suspensión para nebulización, por lo que no se recomiendan.
• PULMICORT® en suspensión para nebulización puede mezclarse con solución salina al 0.9% y con soluciones para nebulización de terbutalina, salbutamol, fenoterol, acetilcisteína, cromoglicato de sodio e ipratropio. La mezcla debe utilizarse en los siguientes 30 minutos.
• Debe enjuagarse la boca con agua después de inhalar la dosis prescrita a fin de minimizar el riesgo de aftas orofaríngeas.
• Debe lavarse la cara con agua después de usar la mascarilla para evitar una irritación.
• Debe limpiar y cuidar el nebulizador siguiendo las instrucciones del fabricante.
Los niños que no saben respirar por la boquilla pueden utilizar una mascarilla.
SOBREDOSIS: No se prevé que una sobredosis aguda de PULMICORT® en suspensión para nebulización, incluso muy alta, pueda causar problemas clínicos. Cuando se utilizan dosis altas de manera crónica, pueden tener lugar efectos glucocorticoides sistémicos tales como hipercortisolismo y depresión suprarrenal.
PRESENTACIÓN COMERCIAL: PULMICORT® 0,5 mg/mL esteril, caja por 20 unidades monodosis de 2 mL (Reg. San. INVIMA 2007M-006817-R1).
Fecha de revisión del texto: Octubre de 2011
Fecha de preparación de la versión: Junio de 2013
Fuente: RITA.000.160.217.5.0
Clave: 1-2013(2)
PULMICORT® es una marca registrada del grupo AstraZeneca.
© AstraZeneca 2011
AstraZeneca AB, Södertälje, Suecia
Mayor información Departamento Médico de
AstraZeneca Colombia, S. A. S.
Bogotá, D.C., Colombia
PLAZO DE CADUCIDAD: Consultar la fecha de caducidad en la caja de cartón externa.