
ELOCOM
MOMETASONA
Crema
, Tubo, Crema,15 g
Para visualizar el contenido completo de la IPPA (información para prescribir amplia), deberá iniciar sesión.
COMPOSICIÓN:
Crema: Cada g de ELOCOM® CREMA al 0,1% contiene: 1 mg de furoato de mometasona.
Loción: Cada g de ELOCOM® LOCIÓN al 0,1% contiene: 1 mg de furoato de mometasona.
FARMACOCINÉTICA PRECLÍNICA Y METABOLISMO: Se realizaron varios estudios para investigar la absorción, distribución, metabolismo y excreción del furoato de mometasona siguiendo varias vías de administración y en diferentes especies. El furoato de mometasona y/o sus metabolitos son rápida y extensamente distribuidos en la rata. El furoato de mometasona sufre un extenso metabolismo de primer paso y se excreta en forma de metabolitos principalmente por vía biliar, y de forma limitada en la orina.
INDICACIONES: Terapia corticoesteroide de la piel.
PARTICULARIDADES FARMACÉUTICAS:
Ingredientes activos: El furoato de mometasona (Figura 1.1), 9,21-dicloro-11ß-17-dihidroxi- 16a-metilpregna-1,4-dieno-3,20-diona-17-(2)-furoato, es un corticosteroide anti-inflamatorio sintético cuyo núcleo esteroide es el 16a-metil análogo de beclometasona, pero con un grupo 21-cloro y un (2)-furoato en la función 17-éster. La fórmula empírica es C27H30CI2O6 y peso molecular (PM) es 521,44.
Figura 1.1.
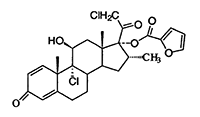
PROPIEDADES FARMACOCINÉTICAS: El grado de absorción percutánea de los corticosteroides tópicos está determinado por muchos factores, incluyendo el vehículo y la integridad de la barrera epidérmica y el uso de vendajes oclusivos. Los corticosteroides tópicos pueden ser absorbidos por la piel intacta normal. Inflamación y/u otros procesos de enfermedades en la piel aumentan la absorción percutánea. Los vendajes oclusivos aumentan sustancialmente la absorción percutánea de los corticosteroides tópicos.
Absorción: La absorción percutánea de furoato de 3H-mometasona fue estudiado en el hombre después de la aplicación tópica de las formulaciones en crema (0,1%) y ungüento (0,1%). Los resultados mostraron que sólo aproximadamente el 0,4% y el 0,7% del esteroide, respectivamente, fueron absorbidos sistémicamente después de 8 horas de contacto, sin oclusión, a través de la piel intacta de voluntarios normales. La absorción percutánea de furoato de 3H-mometasona también se estudió en pacientes con psoriasis después de una sola dosis de la aplicación tópica de la formulación de ungüento al 0,1% sobre un área 100 cm2.
Los resultados mostraron que sólo 1,3% de mometasona se absorbe sistémicamente después de 12 horas de la aplicación a través de la piel no ocluida. Se anticipa mínima absorción con la formulación de loción.
En los estudios sobre los efectos de mometasona furoato crema y ungüento en el eje hipotalámico-pituitario-adrenal (HPA), se aplicaron 15 gramos, dos veces al día durante 7 días a 6 pacientes con psoriasis o dermatitis atópica. La crema o ungüento se aplicó sin oclusión a por lo menos 30% de la superficie del cuerpo. Los resultados sugieren que el medicamento provocó un ligero descenso de la secreción de corticoides suprarrenales, aunque en ningún caso los niveles de cortisol en plasma van por debajo del límite inferior del rango normal.
Furoato de mometasona loción se aplicó en 15 ml dos veces al día (30 ml por día) a la piel enferma (pacientes con psoriasis del cuero cabelludo y cuerpo) de cuatro pacientes durante siete días, para estudiar sus efectos sobre el eje hipotálamo-pituitario-adrenal (HPA). Niveles de cortisol plasmático para cada uno de los cuatro pacientes se mantuvieron dentro del rango normal y cambiaron poco desde el valor inicial.
En un estudio con 24 niños (de 6 meses a 13 años de edad) con eczema atópico moderado a severo, se aplicó furoato de mometasona en crema una vez al día durante tres a seis semanas. No se utilizaron los apósitos oclusivos. Los niveles de cortisol en plasma para todos los pacientes permanecieron dentro o por encima del rango normal durante el curso del tratamiento. Los valores de laboratorio clínico de los niños en general, se mantuvieron dentro del rango normal. Hubo algunos valores de laboratorio que estaban fuera del rango normal durante el curso del tratamiento; sin embargo, el investigador no tuvo en cuenta que estos valores son de importancia clínica o indicativo de toxicidad del sistema de órganos específicos.
Distribución: Debido a la absorción insignificante de furoato de mometasona después de la administración tópica, la farmacocinética del fármaco se evaluó después de la administración intravenosa de furoato de mometasona. El volumen aparente de distribución era 917 litros, lo que indica que cualquier furoato de mometasona absorbido se distribuye ampliamente. En el plasma humano, el furoato de mometasona se une en más del 99%.
Metabolismo: Una vez absorbido, el furoato de mometasona se metaboliza rápida y extensivamente a múltiples metabolitos. Los múltiples metabolitos son más polares que el furoato de mometasona, y debido a su polaridad, no se considera que tienen actividad farmacológica. No se forma ningún metabolito principal. Después de la administración intravenosa, el aclaramiento total de furoato de mometasona fue 976 ml/min, lo que confirma un metabolismo extenso.
Excreción: Después de la administración intravenosa y basado en el modelado compartimental, la vida media efectiva de eliminación plasmática es de 5,8 horas. Cualquier cantidad absorbida del fármaco se excreta en forma de metabolitos principalmente por vía biliar, y de forma limitada, en la orina.
PROPIEDADES FARMACODINÁMICAS: La actividad farmacodinámica de ELOCOM® crema y loción está directamente relacionada con su componente activo, furoato de mometasona, y los vehículos.
Al igual que otros corticosteroides tópicos, el furoato de mometasona tiene efectos antiinflamatorios, antipruriginosos y propiedades vasoconstrictoras. El mecanismo de la actividad antiinflamatoria de los esteroides tópicos, en general, no está claro. Los corticosteroides, sin embargo, se cree que actúan por la inducción de proteínas inhibidoras de la fosfolipasa A2, llamadas colectivamente lipocortinas. Se ha postulado que estas proteínas controlan la biosíntesis de mediadores potentes de la inflamación, tales como prostaglandinas y leucotrienos, mediante la inhibición de la liberación de ácido araquidónico su precursor común. El ácido araquidónico es liberado de los fosfolípidos de membrana por la fosfolipasa A2.
El furoato de mometasona es un potente inhibidor de la producción in vitro de tres citoquinas inflamatorias que están implicados en la iniciación y el mantenimiento del estado inflamatorio: interleuquina 1 (IL-1), la interleuquina 6 (IL-6), y factor de necrosis tumoral a (TNF- a).
CONTRAINDICACIONES: Hipersensibilidad al medicamento, embarazo, lactancia, evítese la administración en zonas extensas especialmente en lactantes y en niños.
EVENTOS ADVERSOS: Las siguientes reacciones adversas locales se han reportado con formulaciones tópicas de mometasona furoato: prurito, reacciones en el lugar de aplicación, infecciones bacterianas, foliculitis, forunculosis, erupciones acneiformes y signos de atrofia de la piel.
Las reacciones adversas locales adicionales que se han comunicado con poca frecuencia, cuando se han utilizado corticosteroides tópicos dermatológicos según lo recomendado son: Ardor, irritación, sequedad, hipertricosis, hipopigmentación, dermatitis perioral, dermatitis alérgica de contacto, maceración de la piel, infección secundaria, estrías, miliaria.
DATOS DE SEGURIDAD PRECLÍNICA: No se demostraron efectos toxicológicos durante el curso de las pruebas preclínicas únicos a la exposición a furoato de mometasona. Todos los efectos observados son típicos de esta clase de compuestos y están relacionados con los efectos farmacológicos exagerados de los glucocorticoides.
Los estudios preclínicos demuestran que el furoato de mometasona está desprovisto de actividad androgénica, anti-androgénica, estrogénica o anti-estrogénica, pero, al igual que otros glucocorticoides, exhibe alguna actividad anti-uterotrófica y retrasa la abertura vaginal en modelos animales a altas dosis orales de 56 mg/kg/día y 280 mg/kg/día.
El furoato de mometasona no fue mutagénico en el ensayo de linfoma de ratón y el bioensayo de mutagenicidad en Salmonella/E. coli/microsomas de mamíferos. A dosis citotóxicas, furoato de mometasona sólo produjo un aumento de aberraciones cromosómicas in vitro en cultivos de células de ovario de hámster chino (CHO) en la fase de no activación, pero no en presencia de la fracción S9 de hígado de rata.
Sin embargo, furoato de mometasona no indujo aberraciones cromosómicas in vitro en una célula de pulmón de hámster chino (CHL)-ensayo de aberraciones cromosómicas, o in vivo en médula ósea de ratón de eritrocitos- ensayo de micronúcleos, en la rata ensayo de clastogenicidad en médula ósea, y el ensayo de clastogenicidad de células germinales masculinas en ratón.
El furoato de mometasona tampoco indujo la síntesis in vivo de ADN no programada en hepatocitos de rata. El hallazgo de aberraciones cromosómicas simples en la fase de no activación del ensayo de CHO se considera que está relacionado con la citotoxicidad y no se considera que es de importancia en la evaluación del riesgo de furoato de mometasona, debido a los resultados negativos en la fase S9 de este ensayo, los resultados negativos en un segundo ensayo in vitro de aberraciones cromosomales (ensayo CHL), y los resultados negativos en tres ensayos in vivo de aberraciones cromosómicas.
En los estudios de la función reproductiva, el furoato de mometasona subcutáneo fue bien tolerado a dosis de hasta 7,5 µg/kg. A 15 µg/kg, el furoato de mometasona causó gestación prolongada y ocurrió trabajo de parto prolongado y difícil con una reducción en la supervivencia de las crías y el peso corporal o la ganancia de peso corporal. No hubo ningún efecto sobre la fertilidad.
Al igual que otros glucocorticoides, el furoato de mometasona es un teratógeno en roedores y conejos. Se realizaron estudios de teratología en ratas, ratones y conejos por las rutas orales, tópicas y/o subcutáneas. Efectos observados fueron hernia umbilical en ratas, el paladar hendido en ratones, y agenesia de la vesícula biliar, hernia umbilical y patas delanteras flexionadas en conejos. También hubo reducciones en las ganancias de peso corporal materno, efectos sobre el crecimiento fetal (menor peso corporal fetal y/o retraso en la osificación) en ratas, conejos y ratones, y la reducción de supervivencia de las crías en ratones.
En un estudio de teratología oral en conejos, a 700 µg/kg, se observó el aumento de la incidencia de reabsorción y malformaciones, incluyendo paladar hendido y/o malformaciones de la cabeza (hidrocefalia o cabeza en forma de cúpula). Se observó fracaso del embarazo en la mayoría de los conejos a 2800 microgramos/kg.
La carcinogenicidad y potencial toxicológico de furoato de mometasona inhalado (aerosol con propulsor de CFC y tensioactivo) en concentraciones de 0,25 a 2,0 ug/I se investigó en estudios en ratones y ratas de hasta 24 meses. Se observaron efectos relacionados con glucocorticoides típicos, entre ellos varias lesiones no neoplásicas. No se detectó ninguna relación estadísticamente significativa dosis-respuesta para cualquiera de los tipos de tumores.
ADVERTENCIAS Y PRECAUCIONES: Si se desarrolla irritación o sensibilización con el uso de ELOCOM®, debe suspenderse su administración e instituirse el tratamiento apropiado.
En presencia de una infección dermatológica debe instituirse el uso de un agente antimicótico o antibacteriano apropiado. Si no ocurre respuesta favorable rápidamente, el corticosteroide debe suspenderse hasta que la infección se haya controlado adecuadamente.
La absorción sistémica de corticosteroides tópicos puede producir la supresión reversible del eje hipotalámico-pituitario-adrenal (HPA) con el potencial de insuficiencia glucocorticoide después de la retirada del tratamiento. Las manifestaciones de síndrome de Cushing, hiperglucemia y glucosuria también se pueden producir en algunos pacientes por absorción sistémica de corticosteroides tópicos durante el tratamiento. Los pacientes que se aplican un esteroide tópico en un área de gran superficie o áreas bajo oclusión deben ser evaluados periódicamente para pruebas de supresión del eje HPA. Cualquiera de los efectos secundarios que se comunican con la administración de corticosteroides sistémicos, incluso depresión adrenal, también puede ocurrir con la administración tópica de corticosteroides, especialmente en lactantes y niños.
Los pacientes pediátricos pueden ser más susceptibles a la toxicidad sistémica de dosis equivalentes debido a mayor superficie de la piel con relación a la masa corporal.
No existen estudios adecuados y bien controlados en mujeres embarazadas. Al igual que otros glucocorticoides, las formulaciones con furoato de mometasona se deben utilizar en mujeres embarazadas o en período de lactancia sólo si el beneficio potencial justifica el riesgo potencial para la madre, el feto o el lactante.
Los productos ELOCOM® no se recomiendan para el uso oftálmico.
DOSIFICACIÓN Y ADMINISTRACIÓN: Debe aplicarse una capa fina de ELOCOM® crema al 0,1% a las áreas cutáneas afectadas, una vez al día. Se debe aplicar unas gotas de ELOCOM® loción una vez al día en las áreas cutáneas afectadas, incluyendo lesiones en el cuero cabelludo, masajear suave y profundamente hasta hacer desaparecer la loción.
SOBREDOSIFICACIÓN: El uso excesivo y prolongado de corticosteroides tópicos puede deprimir la función hipotálamo-hipófisis-adrenal, causando insuficiencia adrenal secundaria.
Si se observa supresión del eje HPA, se debe hacer un intento de retirar el fármaco, para reducir la frecuencia de aplicación o para sustituir un esteroide menos potente.
Tratamiento: Está indicado el tratamiento sintomático apropiado. Los síntomas hipercorticoides agudos son virtualmente reversibles. En casos de toxicidad crónica se aconseja suspender lentamente el corticoide.
DESCRIPCIÓN DEL PRODUCTO: El furoato de mometasona es un corticosteroide sintético que presenta propiedades antiinflamatorias, antipruríticas y vasoconstrictoras, el cual es actualmente usado terapéuticamente para el tratamiento de dermatosis que responden a corticoesteroides tales como psoriasis y dermatitis atópica y dermatitis alérgica y/o irritante de contacto. La loción también puede ser aplicada a lesiones del cuero cabelludo.
ALMACENAMIENTO: Almacenar a temperatura inferior a 30 °C. Manténgase fuera del alcance de los niños. Venta bajo fórmula médica.
DISPONIBILIDAD: Crema, tubo por 15 g (Reg. San. INVIMA 2009 M-010864-R2). Loción, frasco aplicador por 30 mL. (Reg. San. INVIMA No. 2016M- 011679-R3).
Este documento fue revisado por última vez en Abril de 2014.
S-CCDS-MK0887-MTL-042014
MERCK SHARP & DOHME
Bogotá, D.C. - Colombia