
IMODIUM
LOPERAMIDA
Líquido
Frasco(s) , Solución oral , 2/10 mg/ml
Frasco(s), Solución oral, 2/15 mg/ml
CARACTERÍSTICAS FARMACÉUTICAS:
Incompatibilidades: Se desconocen.
Precauciones especiales para el almacenamiento: Consérvese a temperatura ambiente a no más de 30 ° y en lugar seco.
No se deje al alcance de los niños.
COMPOSICIÓN CUALITATIVA Y CUANTITATIVA:
— 2 mg de clorhidrato de loperamida (HCl) por cápsula o tableta.
— 2 mg de clorhidrato de loperamida (HCl)/10 ml de solución oral.
— 2 mg de clorhidrato de loperamida (HCl)/15 ml de líquido oral.
— 2 mg de clorhidrato de loperamida por gragea.
INDICACIONES TERAPÉUTICAS:
IMODIUM® 2 mg cápsulas blandas está indicado en adultos y adolescentes mayores de 12 años para el tratamiento sintomático de la diarrea aguda inespecífica.
PROPIEDADES FARMACOLÓGICAS:
Propiedades farmacodinámicas:
— Grupo farmacoterapéutico: Código ATC: A07 DA03
— Antipropulsivos: Loperamida se liga al receptor opiáceo en la pared intestinal. Por lo tanto, inhibe la liberación de acetilcolina y de prostaglandinas, con lo que reduce la peristalsis propulsiva y acelera el tiempo de tránsito intestinal. Loperamida aumenta el tono del esfínter anal, con lo que se reducen la incontinencia y la urgencia.
Propiedades farmacocinéticas:
— Absorción: La mayor parte de loperamida ingerida se absorbe a través del intestino, pero como resultado del metabolismo significativo de primer paso, la biodisponibilidad sistémica es sólo de 0,3% aproximadamente. Las formulaciones de loperamida HCl (cápsula dura y blanda, tableta recubierta y sin recubierta, tableta masticable y orodispersable, solución oral) son bioequivalentes en términos de tasa y grado de absorción de loperamida.
— Distribución: Los estudios de distribución en ratas muestran una alta afinidad por la pared intestinal, con una preferencia de unión a los receptores de la capa muscular longitudinal. La ligadura a proteína plasmática de loperamida es 95%, principalmente a albúmina. Ningún dato clínico ha mostrado que loperamida sea un sustrato de glicoproteína-P.
— Metabolismo: Loperamida es casi completamente extraída por el hígado, mientras que es metabolizada, conjugada y excretada predominantemente, por la bilis. La ruta metabólica principal de loperamida es la N-demetilación oxidativa y es mediada principalmente a través de la CYP3A4 y CYP2C8. Debido a este alto efecto de primer paso, las concentraciones plasmáticas de droga inalterada permanecen extremadamente bajas.
— Eliminación: La vida media de loperamida en humanos es de aproximadamente 11 horas, con un rango de 9-14 horas. La excreción de loperamida inalterada y de sus metabolitos ocurre principalmente a través de las heces.
— Población pediátrica: No se realizaron estudios farmacocinéticos en la población pediátrica. Se anticipa que el comportamiento farmacocinético de loperamida y las interacciones droga-droga con loperamida sean similares a los de adultos.
CONTRAINDICACIONES:
— Hipersensibilidad al principio activo o alguno de los componentes de la fórmula.
— Menores de 12 años de edad.
— Disentería aguda, caracterizada por la presencia de sangre en las heces y fiebre elevada (superior a 38 °C).
— Colitis ulcerosa aguda.
— Colitis pseudomembranosa asociada al tratamiento con antibióticos de amplio espectro.
— Pacientes con enterocolitis bacteriana causada por organismos invasivos como son Salmonella, Shiguella y Campylobacter.
— En general, IMODIUM® 2 mg cápsulas blandas no debe administrarse cuando se quiera evitar la inhibición del peristaltismo debido al posible riesgo de secuelas significativas incluido obstrucción intestinal, megacolon y megacolon tóxico.
EMBARAZO Y LACTANCIA: A pesar de que no existen indicios de que clorhidrato de loperamida posea propiedades teratogénicas o embriotóxicas, los beneficios terapéuticos previstos deberán ser ponderados a la luz de los daños potenciales antes de la administración de clorhidrato de loperamida durante el embarazo, en particular durante el primer trimestre.
Se pudieran presentar cantidades menores de loperamida en la leche materna. Por lo tanto, clorhidrato de loperamida no está recomendado durante la lactancia.
EFECTOS EN LA CAPACIDAD PARA CONDUCIR VEHÍCULOS Y PARA OPERAR MAQUINARIA: Puede ocurrir cansancio, vértigo o somnolencia en los cuadros de síndromes diarreicos tratados con clorhidrato de loperamida. Por lo tanto, se recomienda precaución cuando se conduzcan vehículos o se haga uso de maquinaria.
EFECTOS NO DESEADOS: En el transcurso de esta sección se presentan las reacciones adversas. Las reacciones adversas son eventos adversos que fueron considerados razonablemente asociados con el uso de loperamida basándose en la evaluación exhaustiva de la información disponible de eventos adversos. En casos individuales, no se puede establecer de modo confiable una relación causal con loperamida HCl. Más aún, debido a que los estudios clínicos se realizan bajo una amplia variedad de condiciones, las tasas de reacciones adversas observadas en los estudios clínicos de una droga no pueden ser comparadas directamente con las tasas de los estudios clínicos de otra droga y puede que no reflejen las tasas observadas en la práctica clínica.
Datos provenientes de estudios clínicos:
— Adultos y niños ≥12 años de edad:
• Diarrea aguda: La seguridad de loperamida HCl fue evaluada en 2.755 pacientes ≥12 años que participaron en 26 estudios clínicos controlados y no-controlados de loperamida HCl usada para el tratamiento de diarrea aguda. Las reacciones adversas (ADRs) reportadas por ≥1% de pacientes tratados con loperamida HCl se muestran en la Tabla 1.
|
Tabla 1. Reacciones adversas a la droga reportadas por ≥1% de pacientes tratados con loperamida HCl en 26 estudios clínicos de loperamida HCl en diarrea aguda. |
|
|
Clase sistema de órgano Reacción adversa a la droga |
Loperamida HCl (%) (N=2.755) |
|
Trastornos del sistema nervioso |
|
|
Cefalea |
1,2 |
|
Trastornos gastrointestinales |
|
|
Constipación |
2,7 |
|
Flatulencia |
1,7 |
|
Náuseas |
1,1 |
En la Tabla 2 se muestran las reacciones adversas a la droga reportadas por <1% de pacientes tratados con loperamida HCl (N=2.755) en la base de datos del estudio clínico anterior.
|
Tabla 2. Reacciones adversas a la droga reportadas por <1% de pacientes tratados con loperamida HCl en 26 estudios clínicos de loperamida HCl en diarrea aguda. |
|
Clase sistema de órgano Reacción adversa a la droga |
|
Trastornos del sistema nervioso Mareos |
|
Trastornos gastrointestinales Sequedad en la boca Dolor abdominal Vómitos Malestar abdominal Dolor abdominal superior Distensión abdominal |
|
Trastornos de la piel y tejido subcutáneo Urticaria |
— Diarrea crónica: La seguridad de loperamida HCl fue evaluada en 321 pacientes que participaron en 5 estudios clínicos controlados y no-controlados de loperamida HCl usada para el tratamiento de diarrea crónica. Los períodos de tratamiento oscilaron desde 1 semana hasta 52 meses.
|
Tabla 3. Reacciones adversas a la droga reportadas por ≥1% de pacientes tratados con loperamida HCl en 5 estudios clínicos de loperamida HCl en diarrea crónica. |
|
|
Clase sistema de órgano Reacción adversa a la droga |
Loperamida HCl (%) N=321) |
|
Trastornos del sistema nervioso Mareos |
1,2 |
|
Trastornos gastrointestinales Flatulencia Constipación Náuseas |
2,8 2,2 1,2 |
En la Tabla 4 se muestran las reacciones adversas a la droga reportadas por <1% de pacientes tratados con loperamida HCl (N=321) en la base de datos de los estudios clínicos anteriores.
|
Tabla 4. Reacciones adversas a la droga reportadas por <1% de pacientes tratados con loperamida HCl en 5 estudios clínicos de loperamida HCl en diarrea crónica. |
|
Clase sistema de órgano |
|
Trastornos del sistema nervioso Cefalea |
|
Trastornos gastrointestinales Dolor abdominal Sequedad en la boca Malestar abdominal Dispepsia |
— Niños menores de 12 años:
• Diarrea aguda: La seguridad de loperamida HCl fue evaluada en 607 pacientes con edades comprendidas entre 10 días a 13 años que participaron en 13 estudios clínicos controlados y no-controlados de loperamida HCl usada para el tratamiento de diarrea aguda. Las reacciones adversas reportadas por ≥1% de pacientes tratados con loperamida HCl se muestran en la Tabla 5.
|
Tabla 5. Reacciones adversas a la droga reportadas por ≥1% de pacientes <12 años tratados con loperamida HCl en 13 estudios clínicos de loperamida HCl en diarrea aguda. |
|
|
Clase sistema de órgano Reacción adversa a la droga |
Loperamida HCl (%) (N=607) |
|
Trastornos gastrointestinales |
|
|
Vómitos |
1,2 |
En la Tabla 6 se muestran las reacciones adversas a la droga reportadas por <1% de pacientes tratados con loperamida HCl (N=607) en la base de datos de los estudios clínicos anteriores.
|
Tabla 6. Reacciones adversas a la droga reportadas por <1% de pacientes tratados con loperamida HCl <12 años en 13 estudios clínicos de loperamida HCl en diarrea aguda |
|
Clase sistema de órgano Reacción adversa a la droga |
|
Trastornos del sistema nervioso Somnolencia Mareos Cefalea |
|
Trastornos gastrointestinales Náusea Dolor abdominal Constipación |
|
Trastornos de la piel y del tejido subcutáneo Urticaria |
Experiencia posterior a la comercialización: En las Tablas 7 y 9 se incluyen las primeras reacciones adversas a la droga identificadas durante la experiencia posterior a la comercialización con loperamida HCl. En cada tabla, las frecuencias son suministradas de acuerdo con las convenciones siguientes:
— Muy común (>1/10)
— Común (>1/100, < 1/10)
— Poco común (> 1/1.000, < 1/100)
— Rara (>1/10.000, < 1/1,000)
— Muy rara (<1/10.000), donde se incluyen los reportes aislados.
En las Tabla 7 y 8, las ADRs son presentadas por categoría de frecuencia basada en la incidencia en los estudios clínicos o en los estudios epidemiológicos, respectivamente.
|
Tabla 7: Reacciones adversas a la droga identificadas durante la experiencia posterior a la comercialización con loperamida HCl por categoría de frecuencia, estimada a partir de las tasas de reportes espontáneos en adultos y niños. |
|
|
Trastornos del sistema inmune |
|
|
Muy rara |
Reacción de hipersensibilidad, reacción anafiláctica (incluyendo shock anafiláctico) y reacción anafilactoide. |
|
Trastornos del sistema nervioso |
|
|
Muy rara |
Coordinación anormal, nivel deprimido de conciencia, hipertonía, pérdida de conciencia, somnolencia, estupor. |
|
Trastornos oculares |
|
|
Muy raro |
Miosis. |
|
Trastornos gastrointestinales |
|
|
Muy raros |
Ileo paralítico, megacolon (incluyendo magacolon tóxicoa), glosodiniab |
|
Trastornos de la piel y tejido subcutáneo |
|
|
Muy raros |
Angioedema, erupción bulosa (incluyendo síndrome de Stevens-Johnson, necrólisis epidérmico tóxico y eritema multiforme), prurito, urticaria |
|
Trastornos renales y urinarios |
|
|
Muy raros |
Retención urinaria |
|
Trastornos generales y condiciones en el sitio de administración |
|
|
Muy raro |
Fatiga |
|
a: Sección Advertencias especiales y precauciones especiales de uso. b: Reportado sólo para la tableta orodispersable. |
|
|
Tabla 8: Reacciones adversas a la droga identificadas durante la experiencia posterior a la comercialización con loperamida HCl por categoría de frecuencia, estimada a partir de los datos de los estudios clínicos o de los estudios de epidemiología en adultos y niños. |
|
|
Trastornos del sistema inmune |
|
|
Raras |
Reacción de hipersensibilidad, reacción anafiláctica (incluyendo shock anafiláctico) y reacción anafilactoide |
|
Trastornos del sistema nervioso |
|
|
Poco común |
Somnolencia |
|
Raras |
Coordinación anormal, nivel deprimido de conciencia, hipertonía, pérdida de conciencia, estupor |
|
Trastornos oculares |
|
|
Raro |
Miosis |
|
Trastornos gastrointestinales |
|
|
Raros |
Ileo (incluyendo íleo paralítico), megacolon (incluyendo magacolon tóxicoa), glosodiniab |
|
Trastornos de la piel y tejido subcutáneo |
|
|
Raros |
Angioedema, erupción bulosa (incluyendo síndrome de stevens-johnson, necrólisis epidérmico tóxico y eritema multiforme), prurito, urticaria |
|
Trastornos renales y urinarios |
|
|
Raros |
Retención urinaria |
|
Trastornos generales y condiciones en el sitio de administración |
|
|
Raro |
Fatiga |
|
a: Sección Advertencias especiales y precauciones especiales de uso. b: Reportado sólo para la tableta orodispersable. |
|
INTERACCIÓN CON OTROS MEDICAMENTOS Y OTRAS FORMAS DE INTERACCIÓN: No hay datos clínicos que sustenten que loperamida sea un sustrato para la glicoproteína-P. La administración concomitante de loperamida (dosis única de 16 mg) con quinidina o con ritonavir, ambos inhibidores de la glicoproteína-P, dio por resultado un aumento de entre 2 y 3 veces en los niveles plasmáticos de loperamida. Se desconoce la importancia clínica de esta interacción farmacocinética con los inhibidores de la glicoproteína P, en los casos en que se administra loperamida en las dosis recomendadas.
La administración concomitante de loperamida (dosis única de 4 mg) e itraconazol, un inhibidor de CYP3A4 y glicoproteína-P, dio por resultado un aumento de entre 3 y 4 veces en los niveles plasmáticos de loperamida. En el mismo estudio, un inhibidor de CYP2C8, gemfibrozil, aumentó los niveles de loperamida en aproximadamente el doble. La combinación de itraconazol y gemfibrozil dio como resultado un aumento de 4 veces de los niveles plasmáticos de loperamida y un aumento de 13 veces en la exposición plasmática total. Estos aumentos no se asociaron con efectos en el sistema nervioso central (SNC) de acuerdo a las mediciones en las pruebas psicomotoras (ej. adormecimiento subjetivo y en la Prueba de sustitución de símbolos dígitos).
La administración concomitante de loperamida (dosis única de 16 mg) y ketaconazol, un inhibidor de CYP3A4 y glicoproteína-P, dio por resultado un aumento de 5 veces en las concentraciones plasmáticas de loperamida. Este aumento no se asoció con un aumento de los efectos farmacodinámicos de acuerdo a lo medido mediante pupilometría.
El tratamiento concomitante con desmopresina oral dio por resultado un aumento de 3 veces en las concentraciones plasmáticas de desmopresina, presuntamente debido a una motilidad gastrointestinal más baja.
Se anticipa que las drogas con propiedades farmacológicas similares pueden potenciar el efecto de loperamida y que las drogas que aceleran el tránsito gastrointestinal puedan disminuir su efecto.
DATOS PRECLÍNICOS SOBRE SEGURIDAD: Estudios sobre toxicidad de dosis repetida crónica de loperamida de hasta 12 meses de duración en perros y de 18 meses en rata no han mostrado efectos tóxicos además de los relativos a disminución del aumento de peso y de consumo de alimento en dosis diarias de hasta 5 mg/kg/día (30 veces por encima del Nivel Máximo de Uso Humano (MHUL, por sus siglas en inglés) y de hasta 40 mg/kg/día (240 veces el MHUL) respectivamente. Los Niveles de Efecto No Tóxico (NTEL, por sus siglas en inglés) en los estudios mencionados fueron de 1.25 mg/kg/día (8 veces el MHUL) y de 10 mg/kg/día (60 veces el MHUL) en perros y ratas, respectivamente. Los resultados de estudios llevados a cabo in vivo e in vitro indicaron que loperamida no es genotóxico. No se observó potencial carcinogénico. En estudios sobre reproducción, donde ratas preñadas se dosificaron durante la preñez y/o lactancia, las dosis altas de loperamida (40 mg/kg/día-240 veces el MHUL) resultó en toxicidad materna y sobrevivencia reducida del feto/cachorro . Las dosis menores no causaron efectos en la salud materna o fetal y no afectaron el desarrollo peri y postnatal.
Se observaron efectos pre-clínicos únicamente en los casos de exposiciones consideradas suficientemente excesivas en relación con la exposición máxima humana, lo cual indica irrelevancia en la utilización clínica.
ADVERTENCIAS ESPECIALES Y PRECAUCIONES ESPECIALES PARA LA UTILIZACIÓN: Se debe suspender rápidamente el tratamiento con este medicamento si se presentara: Estreñimiento, distensión abdominal o subíleo.
Si no se observara mejoría clínica en 48 horas o si aparece fiebre, se interrumpirá el tratamiento con IMODIUM® 2 mg cápsulas blandas y evaluar la situación clínica.
Puesto que el tratamiento de la diarrea con loperamida es sólo sintomático, cuando sea posible, esta se debe tratar a partir de su causa. En pacientes con diarrea, especialmente ancianos y en niños menores de 12 años, se puede presentar depleción de fluidos y electrolitos. En tales casos, la medida terapéutica más importante es la administración de fluidos apropiados y la reposición de electrolitos. La deshidratación puede influir en la variabilidad de la respuesta de loperamida.
Los pacientes con SIDA tratados con IMODIUM® 2 mg cápsulas blandas para la diarrea deben suspender el tratamiento ante los primeros signos de la distensión abdominal. Se han reportado casos muy raros de megacolon tóxico en enfermos de SIDA tratados con loperamida para colitis infecciosa debida a patógenos virales o bacterianos.
Aunque no se dispone de datos farmacocinéticos en los pacientes con insuficiencia hepática IMODIUM® 2 mg cápsulas blandas debe usarse con precaución en estos pacientes dada la reducción del metabolismo de primer paso. Se vigilará estrechamente a los pacientes con disfunción hepática en busca de signos de toxicidad de SNC. IMODIUM® 2 mg cápsulas blandas se admistrará bajo supervisión médica a los pacientes con disfunción hepática grave.
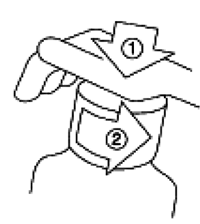
INSTRUCCIONES DE USO/MANEJO: El frasco de solución/líquido oral viene con una tapa/tasa de medición a prueba de niños, y se debe abrir como se indica a continuación:
— Empuje la tapa/taza plástica a rosca hacia abajo mientras que la gira en sentido de las aguas del reloj.
Tabletas orodispersables: Las tabletas orodispersable son frágiles y no debe ser empujadas para sacarlas del blíster ya que se pueden dañar. Para extrar las tabletas orodispersables del blíster se debe:
— Halar el borde de la lámina de aluminio.
— Separar por completo la lámina de aluminio.
— Presionar hacia afuera la tableta.
— Extraer la tableta.
POSOLOGÍA Y MODO DE ADMINISTRACIÓN:
— Tabletas orodispersables: La tableta orodispersable debe ser colocada sobre la lengua. Ella se disolverá y será tragada con la saliva. No es necesario ingerir líquido con la tableta orodispersable.
— Cápsulas y tabletas: Las tabletas y cápsulas deben ser tomadas con líquido.
Adultos y adolescentes mayores de 12 años: Iniciar el tratamiento tomando 2 cápsulas y continuarlo con 1 cápsula después de cada deposición diarréica.
No tomar más de 8 cápsulas al día.
La duración máxima de tratamiento será de 2 días.
Población pediátrica: IMODIUM® 2 mg cápsulas blandas está contraindicado en menores de 12 años.
Insuficiencia hepática: Aunque no se dispone de datos farmacocinéticos en los pacientes con insuficiencia hepátoca IMODIUM® 2 mg cápsulas blandas debe usarse con precaución en estos pacientes da la reducción del metabolismo de primer paso.
SOBREDOSIS:
Síntomas: En caso de sobredosis (incluyendo una sobredosis relativa debida a disfunción hepática), puede presentarse depresión del sistema nervioso central (estupor, coordinación anormal, somnolencia, miosis, hipertonía muscular y depresión respiratoria), retención urinaria e íleo paralítico. Los infantes pudieran ser más sensibles a presentar efectos sobre el SNC en comparación con los adultos.
Tratamiento: Si llegasen a presentarse síntomas de sobredosis, se puede administrar naloxona como antídoto. En vista de que la duración de la acción de clorhidrato de loperamida es más prolongada que la de naloxona (1 a 3 horas), pudiera indicarse el tratamiento repetido de naloxona. Por lo tanto, el paciente debe ser monitoreado cuidadosamente por lo menos durante 48 horas a fin de detectar una posible depresión del SNC.
TIPO Y CONTENIDO DEL ENVASE: Las cápsulas y tabletas son suministradas en empaques tipo blíster. Las tabletas masticables son suministrada en empaques tipo blíster o en frascos.
La solución oral/líquida (2 mg/15 ml y 2 mg/10 ml) es suministrada en frascos con una tapa o taza de medición, respectivamente.
PRESENTACIÓN:
Clorhidrato de loperamida Grageas: Caja con 12 y 60 grageas.
Fecha de revisión: 16 de Diciembre de 2010
CCDS - IMODIUM®- Diciembre 2010
JANSSEN PHARMACEUTICAL COMPANIES
PRESENTACIÓN FARMACÉUTICA Y DESCRIPCIÓN:
|
Forma farmacéutica |
Descripción |
|
Cápsula dura |
Polvo blanco en cápsulas con cuerpo gris oscuro y tapa verde. |
|
Cápsula dura |
Polvo blanco en cápsulas con cuerpo verde claro y tapa marrón. |
|
Cápsula blanda |
Cápsula suave, de gelatina, transparente, oval, azul. |
|
Gragea |
Gragea circular, biconvexa, de superficie lisa, color blanco a ligeramente amarillo, sabor dulce, libre de partículas extrañas. |
|
Tableta sin recubierta (también conocida como “comprimido”) |
Tableta en forma de cápsula, verde clara, con surco, grabada con “IMODIUM A-D” por un lado y con “2 MG” por el otro lado |
|
Tableta masticable |
Tableta verde clara, grabada con “IMO” por un lado y con surco y grabada con “2MG” por el otro lado del surco |
|
Tableta orodispersable |
Tableta circular, de color blanco a blancuzco, liofilizada |
|
Solución oral, 2 mg/10 ml |
Solución ligeramente viscosa, transparente de color rojo |
|
Líquido oral, 2 mg/15 ml |
Líquido opaco de color verde |
PRECAUCIONES ESPECIALES PARA EL ALMACENAMIENTO: Como se indica en el registro local. Mantener fuera del alcance de los niños.
Tabletas orodispersables. Almacenar en el empaque original para proteger de la humedad.