
ERANZ
DONEPECILO
Tabletas orales
Tabletas recubiertas, 5 Miligramos
Tabletas recubiertas, 10 Miligramos
Tabletas recubiertas, 10 Miligramos
FORMA FARMACÉUTICA Y FORMULACIÓN: ERANZ está disponible para la administración oral en Tabletas recubiertas que contienen 5 o 10 mg de clorhidrato de donepecilo.
Fórmula: Cada COMPRIMIDO contiene:
|
Clorhidrato de donepecilo |
5 mg |
|
Excipientes c.s.p |
1 tableta |
|
Clorhidrato de donepecilo |
10 mg |
|
Excipientes c.s.p |
1 tableta |
INDICACIONES: ERANZ está indicado para el tratamiento sintomático de la demencia de leve, moderadamente severa a severa del tipo Alzheimer.
FARaMCODINAMIA EN HUMANOS: Las teorías actuales sobre la patogénesis de los signos cognitivos y los síntomas en la enfermedad de Alzheimer atribuyen algunos de estos signos y síntomas a una deficiencia de la neurotransmisión colinérgica.
El clorhidrato de donepecilo es un inhibidor selectivo y reversible de acetilcolinesterasa que es la colinesterasa predominante a nivel cerebral y ejerce su efecto terapéutico al aumentar la función colinérgica. Esto se logra aumentando la concentración de acetilcolina por medio de la inhibición reversible de su hidrólisis por parte de la acetilcolinesterasa.
CONTRAINDICACIONES: ERANZ está contraindicado en los pacientes con una hipersensibilidad conocida al clorhidrato de donepecilo, a los derivados de la piperidina o a cualquier excipiente utilizado en la formulación.
ADVERTENCIAS
Anestesia: ERANZ, como inhibidor de la colinesterasa, probablemente exagere la relajación muscular de tipo succinilcolínico durante la anestesia.
Condiciones cardiovasculares: Debido a su acción farmacológica, los inhibidores de la colinesterasa pueden ejercer efectos vagotónicos sobre los nodos sinoatrial y atrioventricular (p. ej., bradicardia). Este efecto puede manifestarse como bradicardia o bloqueo cardiaco en pacientes con o sin anormalidades conocidas de fondo en la conducción cardiaca. Sin embargo suele ser más importantes en pacientes que tienen anormalidades conocidas como síndrome del sino enfermo o con problemas de conducción supraventricular, como los bloqueos sinoatrial o atrioventricular.
Condiciones gastrointestinales: Por medio de su acción primaria, puede esperarse que los inhibidores de la colinesterasa aumenten la secreción del ácido gástrico debido a un aumento de la actividad colinérgica. Por lo tanto, es necesario monitorear cuidadosamente a los pacientes para detectar síntomas de sangrado gastrointestinal activo u oculto, especialmente en aquellas personas con un mayor riesgo de desarrollar úlceras, p. ej., quienes tienen antecedentes de una enfermedad ulcerativa o quienes reciben concomitantemente agentes antiinflamatorios no esteroideos (AINES). Los estudios clínicos con ERANZ no han demostrado algún aumento de la incidencia de enfermedad por úlcera péptica o hemorragias gastrointestinales, en comparación con el placebo.
Como una consecuencia previsible de sus propiedades farmacológicas, se ha demostrado que ERANZ puede causar diarrea, náuseas y vómito. Cuando ocurren, estos efectos son más frecuentes con la dosis de 10 mg/día que con la dosis de 5 mg/día. En la mayoría de los casos, estos efectos han sido leves y transitorios, a veces con una duración de una a tres semanas y se han resuelto con el uso continuo de ERANZ.
Genitourinarios: Los agentes colinomiméticos pueden causar una obstrucción del flujo de vaciamiento vesical; sin embargo, este efecto no se ha observado en los estudios clínicos con ERANZ.
Condiciones neurológicas: Convulsiones: Se cree que los agentes colinomiméticos tienen cierto potencial para causar convulsiones generalizadas. Sin embargo, la actividad convulsiva también puede ser una manifestación de la enfermedad de Alzheimer.
Condiciones pulmonares: Debido a sus acciones colinomiméticas, los inhibidores de la colinesterasa deben recetarse cuidadosamente a los pacientes con antecedentes familiares de asma o de una enfermedad pulmonar obstructiva.
PRECAUCIONES
Interacciones medicamentosas (ver Farmacología clínica: Farmacocinética clínica: Interacciones medicamentosas).
Efecto de ERANZ sobre el metabolismo de otros medicamentos: No se han realizado estudios clínicos in vivo para investigar el efecto de ERANZ sobre el aclaramiento de medicamentos metabolizados por CYP 3A4 (p. ej., cisaprida, terfenadina) o por CYP 2D6 (p. ej., imipramina). Sin embargo, los estudios in vitro revelan una tasa de unión baja con estas enzimas (Ki media alrededor de 50-130 µM) lo que, dadas las concentraciones plasmáticas terapéuticas de donepecilo (164 nM), indica una baja probabilidad de interferencia.
No se sabe si ERANZ tiene algún potencial para inducir las enzimas hepáticas.
El potencial de ERANZ para la interacción de la teofilina, cimetidina, warfarina y digoxina, tioridazina risperidona y sertralia, se evaluó en estudios farmacocinéticos formales. No se observaron efectos significativos de ERANZ sobre la farmacocinética de estos medicamentos.
Efectos de otros medicamentos sobre el metabolismo de ERANZ: El ketoconazol y la quinidina, que son inhibidores de las isoenzimas CYP 450 3A4 y 2D6, respectivamente, inhiben el metabolismo del donepecilo in vitro. No se sabe si la quinidina causa un efecto clínico. En un estudio cruzado de 7 días de duración con 18 sujetos voluntarios sanos, el ketoconazol (200 mg qd) aumentó las concentraciones medias del donepecilo (5 mg qd) (ABC0-24 y Cmáx) en un 36%. No se sabe cuál es la relevancia clínica de este aumento de la concentración.
Los inductores de CYP 2D6 y CYP 3A4 (p. ej., fenitoína, carbamazepina, dexametasona, rifampicina y fenobarbital) podrían aumentar la tasa de eliminación de ERANZ.
Los estudios farmacocinéticos formales demostraron que el metabolismo de ERANZ no se afecta significativamente con la administración concurrente de la digoxina o cimetidina, tioridazina, risperidona y sertralina.
Uso con los agentes anticolinérgicos: Debido a su mecanismo de acción, los inhibidores de la colinesterasa tienen el potencial para interferir con la actividad de los medicamentos anticolinérgicos.
Uso con los agentes colinomiméticos y otros inhibidores de la colinesterasa: Puede esperarse un efecto sinérgico cuando se administran concurrentemente los inhibidores de la colinesterasa con la succinilcolina, agentes bloqueadores neuromusculares similares o agonistas colinérgicos como el betanecol.
PRECAUCIONES O RESTRICCIONES DE USO DURANTE EL EMBARAZO Y LA LACTANCIA:
Embarazo categoría C: No se cuenta con estudios adecuados o bien controlados con mujeres embarazadas. ERANZ debe usarse durante el embarazo solamente si el beneficio potencial justifica el riesgo potencial para el feto.
Madres lactantes
Lactancia: No se sabe si el donepecilo se excreta en la leche materna humana. ERANZ no tiene una indicación para usarse en mujeres lactantes.
EFECTOS SOBRE LA HABILIDAD PARA CONDUCIR U OPERAR MAQUINARIA: La demencia puede causar impedimentos para conducir o compromiso de la habilidad para utilizar maquinaria. Además, el clorhidrato de donepecilo puede causar fatiga, mareos y calambres musculares, principalmente cunado se inicia el tratamiento o cuando se aumenta la dosis.
PRECAUCIONES Y RELACIÓN CON EFECTOS DE CARCINOGÉNESIS, MUTAGÉNESIS, TERATOGÉNESIS Y SOBRE LA FERTILIDAD:
General: Pruebas experimentales extensas en animales han demostrado que el clorhidrato de donepecilo causa pocos efectos en comparación con los efectos farmacológicos esperados por los inhibidores de la colinesterasa.
Mutagenicidad: El donepecilo no fue mutagénico en el ensayo de mutación inversa de Ames en bacterias ni en un ensayo in vitro de mutación prospectiva en linfoma de ratón. En las pruebas de aberraciones cromosómicas en cultivos de células de pulmón de hámster chino (CHL, por sus siglas en inglés), se observaron algunos efectos clastogénicos. El donepecilo no fue clastogénico en la prueba de micronúcleos en ratones in vivo ni fue genotóxica en un ensayo in vivo de síntesis no programada del ADN en ratas. El donepecilo no afectó la fecundidad de las ratas en dosis de hasta de 10 mg/kg/día (aproximadamente 8 veces la dosis máxima recomendada en los seres humanos, sobre una base de mg/m2).
Carcinogenicidad: En un estudio de 88 semanas conducido en ratones CD-1 con dosis de clorhidrato de donepecilo de hasta 180 mg/kg/día (aproximadamente 1100 veces la dosis recomendada en humanos en mg/kg o 90 veces en una base de mg/m2) y en otro estudio de carcinogenicidad de 104 semanas en ratones Sprague-Dawley a dosis de hasta 30 mg/kg/día (aproximadamente 180 veces la dosis máxima recomendada en humanos en mg/kg o 30 veces la dosis en una base de mg/m2), no se encontró evidencia de un potencial carcinogénico en el clorhidrato de donepecilo.
Fertilidad: El clorhidrato de donepecilo no tienen efectos sobre la fertilidad a dosis de hasta 10 mg/kg/día (aproximadamente 8 veces la dosis máxima recomendada en humanos en una base de mg/m2) excepto por una ligera prolongación del ciclo estro en ratas. El clorhidrato de donepecilo no fue terotogénico en ratas o conejos y tuvo un ligero efecto sobre los nacimientos y la supervencia de los cachorros cuando se administró a ratas preñadas a dosis de hasta 10 mg/kg/día.
REACCIONES ADVERSAS
Enfermedad de Alzheimer leve a moderada Eventos adversos que requirieron la descontinuación del tratamiento: Las tasas de descontinuación en los ensayos clínicos controlados con ERANZ debida a los eventos adversos en los grupos con 5 mg/día fueron comparables a las de los grupos con el placebo en aproximadamente el 5%. La tasa de descontinuación fue mayor, del 13%, en los pacientes que recibieron el tratamiento escalado de 5 mg/día a 10 mg/día a lo largo de 7 días.
El Cuadro 1 presenta los eventos adversos más comunes que causaron la descontinuación, definidos como aquellos que ocurrieron en por lo menos el 2% de los pacientes y con una incidencia del doble de la incidencia observada en los pacientes que recibieron el placebo.
|
Cuadro 1. Efectos adversos más frecuentes, que llevaron a la descontinuación del tratamiento en estudios clínicos con controles por grupo de dosis |
|||
|
Grupo de dosis |
Placebo |
ERANZ 5 mg/día |
ERANZ 10 mg/día |
|
Pacientes randomizados |
355 |
350 |
315 |
|
Evento y % de descontinuación |
|||
|
Náuseas |
1% |
1% |
3% |
|
Diarrea |
0% |
<1% |
3% |
|
Vómito |
<1% |
<1% |
2% |
Eventos adversos clínicos relacionados con el uso de ERANZ y observados con mayor frecuencia: Los eventos adversos más comunes, definidos como los que ocurrieron con una frecuencia de por lo menos el 5% de los pacientes que recibieron 10 mg/día y con una tasa el doble que la del placebo, en gran parte pueden anticiparse por las acciones colinomiméticas de ERANZ. Entre ellos están las náuseas, diarrea, insomnio, vómito, calambres musculares, fatiga y anorexia. Con frecuencia, estos eventos adversos fueron leves y transitorios y se resolvieron durante la continuación del tratamiento con ERANZ sin necesidad de modificar la dosis.
Existen evidencias que sugieren que la frecuencia de estos eventos adversos comunes podría verse afectada por la velocidad de la titulación. Se realizó un estudio abierto con 269 pacientes que recibieron un placebo en los estudios de 15 y 30 semanas de duración. Estos pacientes fueron titulados a la dosis de 10 mg/día durante un periodo de 6 semanas. Las tasas de efectos adversos comunes fueron más bajas que las observadas en los pacientes titulados a 10 mg/día a lo largo de una semana en los estudios clínicos controlados y fueron comparables a las de los sujetos que recibieron 5 mg/día.
INTERACCIONES MEDICAMENTOSAS
Medicamentos altamente unidos a las proteínas plasmáticas: Se han realizado estudios in vitro de desplazamiento de medicamentos entre este medicamento altamente unido (96%) y otros, como la furosemida, digoxina y warfarina. En concentraciones de 0,3 a 10 µg/ml, ERANZ no afectó la unión de la furosemida (5 µg/ml), la digoxina (2 ng/ml) o la warfarina (3 µg/ml) a la albúmina humana. De igual forma, la unión de ERANZ con la albúmina humana no se vio afectada por la furosemida, digoxina o warfarina.
Efecto de ERANZ sobre el metabolismo de otros medicamentos: No se han realizado estudios clínicos in vivo para investigar el efecto de ERANZ sobre el aclaramiento de medicamentos metabolizados por CYP 3A4 (p. ej., cisaprida, terfenadina) o por CYP 2D6 (p. ej., imipramina). Sin embargo, los estudios in vitro revelan una baja tasa de unión con estas enzimas (Ki media alrededor de 50-130 µM) lo que, dadas las concentraciones plasmáticas terapéuticas de donepecilo (164 nM), indica una baja probabilidad de interferencia.
No se sabe si ERANZ tiene algún potencial para inducir las enzimas hepáticas.
El potencial de ERANZ para la interacción de la teofilina, cimetidina, warfarina, tioridazina, risperidona, sertralina y digoxina se evaluó en estudios farmacocinéticos formales. No se observaron efectos significativos de ERANZ sobre la farmacocinética de estos medicamentos.
En un estudio con pacientes con enfermedad de Parkinson con tratamiento con L-dopa/carbidopa, la administración de clorhidrato de donepecil por 21 días no tuvo efectos sobre los niveles sanguíneos de L-dopa/carbidopa. En este estudio tampoco se presentaron efectos sobre la actividad motora.
Efectos de otros medicamentos sobre el metabolismo de ERANZ: El ketoconazol y la quinidina, que son inhibidores de las isoenzimas CYP 450 3A4 y 2D6, respectivamente, inhiben el metabolismo del donepecilo in vitro. No se sabe si la quinidina causa un efecto clínico. En un estudio cruzado de 7 días de duración con 18 sujetos voluntarios sanos, el ketoconazol (200 mg qd) aumentó las concentraciones medias del donepecilo (5 mg qd) (ABC0-24 y Cmáx) en un 36%. No se sabe cuál es la relevancia clínica de este aumento de la concentración.
Estén otros inhibidores del CYP3A4, como el itraconazol y la eritromicina e inhibidores del CYP2D6, como la fluoxetina, que pueden inhibir el metabolismo del clorhidrato de donepecilo.
Los inductores de CYP 2D6 y CYP 3A4 (p. ej., fenitoína, carbamazepina, dexametasona, rifampicina, fenobarbital y alcohol) podrían aumentar la tasa de eliminación de ERANZ y reducir sus niveles plasmáticos. Sin embargo como no se conoce la magnitud de la inhibición o el efecto de inducción, tales combinaciones de drogas deben ser utilizadas con cuidado.
ERANZ tiene el potencial de interactuar con medicamentos con actividad anticolinérgica. Así mismo el producto tiene una actividad sinérgica con tratamientos concomitantes con medicamentos como succinilcolina y otros agentes bloqueadores neuromusculares. Existe también potencial de actividad sinérgica sobre agonistas colinérgicos o agentes beta bloqueadores que tienen efectos sobre la conducción cardiaca.
Los estudios farmacocinéticos formales demostraron que el metabolismo de ERANZ no se afecta significativamente con la administración concurrente de la digoxina, cimetidina thioridazina, risperidona, sertralina y cimetidina.
POBLACIONES ESPECIALES
Uso geriátrico: La enfermedad de Alzheimer es un trastorno que se presenta principalmente en las personas mayores de 55 años de edad. La edad media de los pacientes incluidos en los estudios clínicos con ERANZ fue de 73 años; el 80% de estos pacientes tenían entre 65 y 84 años de edad y el 49% de los pacientes tenían ≥ 75 años de edad. Los datos de eficacia y seguridad presentados en la sección de ensayos clínicos provienen de estos pacientes. No hubo diferencias estadísticamente significativas en la mayoría de los eventos adversos reportados por los grupos de pacientes ≥ 65 años y >65 años de edad.
Uso pediátrico: No se tienen estudios clínicos adecuados y bien controlados que documenten la seguridad y eficacia del clorhidrato de donepecilo.
DOSIS Y ADMINISTRACIÓN: ERANZ debe ser tomado oralmente, una vez al día. Se ha encontrado que la dosis clínicamente efectiva es de 5 a 10 mg para pacientes con enfermedad de leve a moderadamente severa, mientras que para pacientes con enfermedad severa la dosis clínicamente efectiva es de 10 mg.
El tratamiento debe iniciarse en 5 mg y puede aumentarse a 10 mg después de 4 a 6 semanas.
En Japón el tratamiento inició en 3 mg y fue incrementado a 5 mg después de 1 a 2 semanas. Para Alzheimer severo en pacientes en Japón, la dosis fue incrementada a 10 mg después de estar recibiendo 5 mg durante 4 semanas o más.
La dosis máxima recomendada diaria es de 10 mg. Dosis mayores a 10 mg/día no han sido estudiadas en estudios clínicos a larga escala.
Después de que se descontinúa el tratamiento se ha presenciado una disminución gradual de los efectos benéficos del clorhidrato de donepezil. No hay evidencia de efectos rebote después de una discontinuación abrupta del tratamiento.
Mantenimiento del tratamiento: El tratamiento puede ser continuado todo el tiempo que sea necesario mientras exista un beneficio para el paciente.
Insuficiencia renal y hepática: El esquema de dosificación descrito puede utilizarse en pacientes con insuficiencia renal o insuficiencia hepática leve debido a que el aclaramiento del clorhidrato de donepecilo no se ve afectado de manera significativa bajo esas condiciones.
SOBREDOSIS
Síntomas de sobredosificación: La sobredosis con inhibidores de la colinesterasa pueden resultar en crisis colinérgicas caracterizadas por naúsea severa, vómito, salivación, sudoración, bradicardia, hipotensión, depresión respiratoria, colpaso y convulsiones. Existe la posibildad de presentarse un incremento en la debilidad muscular que puede causar la muerte si se ven involucrados músculos de la respiración.
Tratamiento: Los anticolinérgicos terciarios, como la atropina, pueden usarse como antídoto contra la sobredosis de ERANZ. Se recomienda el sulfato de atropina por vía intravenosa hasta lograr el efecto: una dosis inicial de 1 a 2 mg IV y dosis subsiguientes según la respuesta clínica. Se han reportado respuestas atípicas de la presión arterial y la frecuencia cardiaca con otros colinomiméticos cuando se coadministran con anticolinérgicos cuaternarios tales como el glucopirrolato. No se sabe si ERANZ y/o sus metabolitos pueden eliminarse por medio de la diálisis (hemodiálisis, diálisis peritoneal o hemofiltración).
PFIZER
® Marca registrada
NOMBRE COMERCIAL Y GENÉRICO: ERANZ es el clorhidrato de donepecilo, conocido químicamente como clorhidrato de (±)-2,3 dihidro-5,6-dimetoxi-2-[[1-(fenilmetil)-4-piperidinil]metil]-1H-inden-1-ona.
Estructura química:
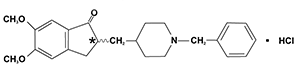
Clase terapéutica: Inhibidor de la acetilconlinesterasa cerebral.