
EMEND IV
APREPITANT
Inyectable I.V.
1 Caja, 1 Frasco(s), 150 mg,
INDICACIONES: EMEND® IV está indicado, en combinación con otros agentes antieméticos, para la prevención de náusea y vómito, agudos y tardíos asociados con los ciclos iniciales y subsecuentes de:
— Quimioterapia anticancerosa altamente emetogénica (véase Dosis y vía de administración).
— Quimioterapia anticancerosa moderadamente emetogénica (véase Dosis y vía de administración).
FARMACOCINÉTICA:
Absorción: Después de una dosis única, intravenosa, de 150 mg de fosaprepitant administrado como una infusión en 20 minutos, en voluntarios sanos, el promedio del ABC0-8 de aprepitant fue 35.0 mcg•hr/ml y la concentración máxima promedio fue 4.01 mcg/ml.
Distribución: Fosaprepitant se convierte rápidamente en aprepitant.
Aprepitant se une más del 95% a las proteínas plasmáticas. El media geométrica del volumen aparente de distribución en el estado de equilibrio (Vdss) es de aproximadamente 66 l en humanos.
Aprepitant atraviesa la placenta en ratas y atraviesa la barrera hematoencefálica en ratas y hurones. Los estudios PET en humanos indican que aprepitant atraviesa la barrerahematoencefálica (véase Farmacología clínica, mecanismo de acción).
Metabolismo: Fosaprepitant se convirtió rápidamente en aprepitant en incubación in vitro con preparados de hígado de especímenes no clínicos (rata y perro) y seres humanos. Por lo tanto, fosaprepitant experimentó la conversión rápida y casi completa de aprepitant en preparativos S9 de varios otros tejidos humanos, incluyendo los riñones, los pulmones y el íleon. Por lo tanto, parece que la conversión de fosaprepitant a aprepitant puede ocurrir en los tejidos extrahepáticos múltiples, además de en el hígado. En los seres humanos, fosaprepitant administrado por vía intravenosa se convirtió rápidamente en aprepitant en los 30 minutos siguientes al final de la infusión.
Aprepitant experimenta un extenso metabolismo. En adultos jóvenes sanos, aprepitant representa aproximadamente el 24% de la radiactividad plasmática durante 72 horas después de una dosis oral única de 300 mg de dosis de [14C]-aprepitant, lo que indica una importante presencia de metabolitos en el plasma. Siete metabolitos de aprepitant, que son sólo débilmente activos, se han identificado en el plasma humano. El metabolismo de aprepitant se produce en gran medida por oxidación en el anillo de morfolina y sus cadenas laterales. Los estudios in vitro con microsomas hepáticos humanos indicaron que aprepitant se metaboliza principalmente por CYP3A4 en el metabolismo del menor por CYP1A2 y CYP2C19, y el metabolismo no por la CYP2D6, CYP2C9, o CYP2E1.
Todos los metabolitos observados en la orina, las heces y plasma después de una dosis intravenosa de 100 mg de [14C]-fosaprepitant, también se observaron después de una dosis oral de [14C]-aprepitant. Tras la conversión de 245.3 mg de fosaprepitant dimeglumina (equivalente a 150 mg de ácidos de fosaprepitant) a aprepitant, 23.9 mg de ácido fosfórico y 95.3 mg de meglumina son liberados.
Eliminación: Tras la administración de una única dosis IV de 100 mg de [14C]-fosaprepitant a sujetos sanos, el 57% de la radiactividad se recuperó en la orina y el 45% en las heces.
Aprepitant se elimina principalmente por metabolismo, aprepitant no se excreta por vía renal. Tras la administración de una dosis oral única de 300 mg de [14C]-aprepitant a sujetos sanos, el 5% de la radiactividad se recuperó en la orina y el 86% en las heces.
La vida media terminal aparente de aprepitant varió aproximadamente de 9 a 13 horas.
CONTRAINDICACIONES: EMEND® IV está contraindicado en los pacientes con hipersensibilidad a EMEND® IV, a aprepitant, a polisorbato 80 o a cualquiera otro de los componentes del producto.
EMEND® IV no debe usarse simultáneamente con pimozida, terfenadina, astemizol o cisaprida. La inhibición de la isoenzima 3A4 del citocromo P450 (CYP3A4) por aprepitant puede aumentar las concentraciones plasmáticas de estos fármacos y causar reacciones graves o potencialmente mortales (véase Interacciones medicamentosas).
PRECAUCIONES/ADVERTENCIAS: Debido a que fosaprepitant se convierte con rapidez en aprepitant (un inhibidor de débil a moderado de la isoenzima CYP3A4), el fosaprepitant se debe usar con precaución en pacientes que están recibiendo medicamentos por vía oral que son metabolizados principalmente por la isoenzima CYP3A4 y con un rango terapéutico estrecho, tal como: Tacrolimus, sirolimus, everolimus, alfentanilo, diergotamina, ergotamina, fentanilo y quinidina; algunos fármacos quimioterapéuticos son metabolizados por la enzima CYP3A4 (véase Interacciones medicamentosas). La inhibición moderada de la isoenzima CYP3A4 por aprepitant y la inhibición débil de la isoenzima CYP3A4 por fosaprepitant 150 mg podría aumentar las concentraciones plasmáticas de estos fármacos administrados por vía oral (véase Interacciones medicamentosas). El efecto de aprepitant por vía oral en la farmacocinética de sustratos de la isoenzima CYP3A4 administrados por vía oral es más grande que el efecto de aprepitant por vía oral en la farmacocinética de sustratos de la isoenzima CYP3A4 administrados por vía intravenosa (véase Interaciones medicamentosas).
Han ocurrido reportes aislados de reacciones de hipersensibilidad inmediata, incluyendo ruborizaciones, eritema y disnea durante la infusión de fosaprepitant. Estas reacciones de hipersensibilidad, generalmente han respondido a la suspensión de la infusión y a la administración del tratamiento adecuado. No se recomienda reiniciar la infusión en pacientes que experimentaron reacciones de hipersensibilidad.
La administración conjunta de aprepitant con warfarina puede ocasionar una reducción clínicamente significativa en el rango internacional normalizado del tiempo de protrombina (INR por sus siglas en inglés). En los pacientes bajo tratamiento crónico con warfarina, se debe vigilar estrechamente el INR durante el periodo de dos semanas y en particular entre los 7 y 10 días, después de iniciar el régimen de fosaprepitant en cada ciclo de quimioterapia (véase Interacciones medicamentosas).
La eficacia de los anticonceptivos hormonales puede disminuir durante la administración y en los 28 días siguientes de la administración de fosaprepitant y aprepitant. Se deben usar métodos anticonceptivos alternativos o de respaldo durante el tratamiento con fosaprepitant o aprepitant y durante un mes después de la última dosis (véase Interacciones medicamentosas).
USO EN PACIENTES DE EDAD AVANZADA: En los estudios clínicos, la eficacia y la seguridad de aprepitant en los pacientes de edad avanzada (de 65 años o mayores) fueron comparables a las observadas en pacientes de menor edad (menores de 65 años). No es necesario ajustar la dosis en los pacientes de edad avanzada.
LACTANCIA: EMEND® IV (fosaprepitant), cuando se administra por vía intravenosa se convierte rápidamente en aprepitant.
El aprepitant es excretado en la leche de las ratas lactantes. No se sabe si este medicamento es excretado en la leche humana. Por lo tanto, no se recomienda la lactancia materna durante el tratamiento con EMEND® IV.
USO EN EMBARAZO: No hay estudios adecuados y bien controlados en mujeres embarazadas. EMEND® IV sólo se debe usar durante el embarazo si el posible beneficio justifica el riesgo potencial para la madre y el feto.
EFECTOS ADVERSOS: Debido a que fosaprepitant se convierte en aprepitant, las reacciones adversas asociadas con aprepitant, también se podrían esperar que ocurran con EMEND® IV.
La seguridad general del fosaprepitant se evaluó en aproximadamente 1,100 personas y la seguridad general de aprepitant se evaluó en aproximadamente 6,500 personas.
Prevención de náusea y vómito inducidos por quimioterapia (NVIQ)
Aprepitant por vía oral
Quimioterapia altamente emetogénica: En dos estudios clínicos bien controlados en pacientes que recibieron quimioterapia anticancerosa altamente emetogénica, 544 pacientes fueron tratados con aprepitant durante el ciclo 1 de quimioterapia y 413 de estos pacientes continuaron en la extensión de múltiples ciclos hasta seis ciclos de quimioterapia. Se administró aprepitant por vía oral combinado con ondansetrón y dexametasona en un régimen de 3 días y fue generalmente bien tolerado. La mayoría de las reacciones adversas reportadas en estos estudios clínicos se describieron como de intensidad leve a moderada.
En el ciclo 1, se reportaron reacciones adversas clínicas relacionadas con el medicamento en aproximadamente 19% de los pacientes tratados con el régimen de aprepitant de 3 días, en comparación con aproximadamente 14% de los pacientes que recibieron el tratamiento estándar. El tratamiento con aprepitant se suspendió debido a reacciones adversas clínicas relacionadas con el medicamento en aproximadamente 0.6% de los pacientes tratados con el régimen de aprepitant de 3 días, en comparación con aproximadamente 0.4% de los pacientes que recibieron el tratamiento estándar.
Las reacciones adversas más comunes reportadas en pacientes tratados con un régimen de aprepitant de 3 días y que a su vez fueron mayores que las reportadas con terapia estándar fueron: Hipo (4.6%), elevación del ALT (alanina aminotransferasa) (2.8%), dispepsia (2.6%), estreñimiento (2.4%), cefalea (2.0%) y disminución del apetito (2.0%).
Además, el perfil de las experiencias adversas en un estudio controlado con sustancias activas, en 1,169 pacientes que recibieron el régimen de aprepitant de 3 días y quimioterapia altamente emetogénica, generalmente fue similar al observado en otros estudios con quimioterapia altamente emetogénica con regímenes de aprepitant de 3 días.
Quimioterapia moderadamente emetogénica: En dos estudios clínicos bien controlados en pacientes que recibieron quimioterapia anticancerosa moderadamente emetogénica, 868 pacientes fueron tratados con el régimen de aprepitant de 3 días, durante el ciclo 1 de quimioterapia y 686 de estos pacientes continuaron en la extensión de múltiples ciclos hasta cuatro ciclos de quimioterapia. En ambos estudios se administró el régimen de aprepitant de 3 días por vía oral combinado con ondansetrón y dexametasona y fue generalmente bien tolerado. La mayoría de las reacciones adversas reportadas en este estudio clínico se describieron como de intensidad leve a moderada.
En el análisis combinado de los datos del ciclo 1, de estos dos estudios, se reportaron reacciones adversas relacionadas al medicamento en aproximadamente 14% de los pacientes tratados con un régimen de aprepitant de 3 días comparado con aproximadamente un 15% de los pacientes tratados con terapia estándar. Un 0.7% de los pacientes tratados con régimen de aprepitant de 3 días discontinuaron la terapia a causa de reacciones adversas relacionadas con el medicamento en comparación con un 0.2% de los pacientes tratados con terapia estándar.
La reacción adversa más comúnmente relacionada con el medicamento, reportada con una incidencia mayor en los pacientes tratados con el régimen de aprepitant de 3 días fue la fatiga (1.4%), comparado con la terapia estándar.
Quimioterapia alta y moderadamente emetogénica: Las siguientes reacciones adversas relacionadas con el medicamento se observaron en los pacientes tratados con el régimen de aprepitant con una mayor incidencia que con el tratamiento estándar:
[Comunes (mayor o igual a 1/100; menor a 1/10), Poco comunes (mayor a 1/1,000; menor a 1/100), Raros (mayor o igual a 1/10,000;, menor a 1/1,000)]
— Infección e infestaciones:
• Raros: Candidiasis, infección estafilocócica.
— Trastornos de la sangre y el sistema linfático:
• Poco comunes: Anemia, neutropenia febril.
— Trastornos del metabolismo y la nutrición:
• Común: Disminución del apetito.
• Raros: Polidipsia.
— Trastornos psiquiátricos:
• Poco comunes: Ansiedad.
• Raros: Desorientación, euforia.
— Trastornos del sistema nervioso:
• Poco Comunes: Mareos, somnolencia.
• Raros: Alteraciones del sueño, trastorno cognitivo, letargia, disgeusia.
— Trastornos oculares:
• Raros: Conjuntivitis.
— Trastornos del oído y el laberinto:
• Raros: Tinitus.
— Trastornos cardiacos:
• Poco común: Palpitaciones.
• Raros: Bradicardia, alteraciones cardiovasculares.
— Trastornos vasculares:
• Poco común: Sensación de calor.
— Trastornos respiratorios, torácicos y mediastínicos:
• Común: Hipo.
• Raros: Dolor orofaringeo, estornudos, tos, goteo retronasal, irritación de la garganta.
— Trastornos gastrointestinales:
• Comunes: Dispepsia.
• Poco comunes: Eructos, náusea, reflujo gastroesofágico, vómito, dolor abdominal, boca seca, flatulencia.
• Raros: Heces duras, perforación de úlcera duodenal, colitis neutropénica, estomatitis, distensión abdominal.
— Trastornos cutáneos y subcutáneos:
• Poco comunes: Erupción cutánea, acné.
• Raros: Fotosensibilidad, hiperhidrosis, seborrea, prurito, lesión cutánea.
— Trastornos musculoesqueléticos y del tejido conectivo:
• Raros: Espasmos musculares, debilidad muscular.
— Trastornos renales y urinarios:
• Poco comunes: Disuria.
• Raros: Poliaquiuria.
— Trastornos generales y del sitio de administración:
• Comunes: Fatiga.
• Poco comunes: Edema, malestar general.
• Raros: Edema, incomodidad torácica, alteraciones de la marcha.
— Análisis de laboratorio:
• Comunes: Elevación de la ALT (alanina aminotransferasa).
• Poco comunes: Elevación de la AST (aspartato aminotransferasa elevación de la fosfatasa alcalina,).
• Raros: Flujo urinario aumentado, glucosuria, hematuria microscópica, hiponatremia, pérdida de peso, descenso del conteo de neutrófilos.
Los perfiles de reacciones adversas en la extensión de múltiples ciclos, hasta por seis ciclos de quimioterapia alta y moderadamente emetogénicas, fueron generalmente similares a los observados en el ciclo 1.
En otro estudio de náusea y vómito inducidos por quimioterapia (NVIQ), se reportó un caso de síndrome de Stevens-Johnson como reacción adversa grave en un paciente que recibió aprepitant con la quimioterapia anticancerosa.
Fosaprepitant: En un estudio controlado con sustancia activa, en pacientes que recibieron quimioterapia altamente emetogénica, se evaluó la seguridad en 1,143 pacientes que recibieron el régimen de 1 día de EMEND® IV 150 mg comparado con 1,169 pacientes que recibieron el régimen de EMEND® (aprepitant) de 3 días. El perfil de seguridad fue generalmente similar al observado previamente en estudios con quimioterapia altamente emetogénica con aprepitant.
Las siguientes reacciones adversas, relacionadas al medicamento, clínicamente importantes ocurrieron con fosaprepitant 150 mg y no habían sido reportadas previamente en los estudios clínicos con el régimen de aprepitant de 3 días, tal como se describió arriba.
[Comunes (mayor o igual a 1/100, menor a 1/10) Poco comunes mayor a 1/1,000, menor a 1/100) Raros (mayor o igual a 1/10,000, menor a 1/1,000)]
— Trastornos generales y del sitio de administración:
• Poco comunes: Eritema, prurito o dolor en el sitio de la infusión.
• Raros: Induración en el sitio de la infusión.
— Investigaciones:
• Poco comunes: Elevación de la presión arterial.
— Trastornos de la piel y tejido subcutáneos:
• Poco comunes: Eritema.
— Trastornos vasculares:
• Poco comunes: Sofoco, tromboflebitis (predominantemente, tromboflebitis en el sitio de la infusión).
Otros estudios: También se han estudiado dosis únicas de EMEND® 40 mg para la prevención de náusea y vómito post operatorio (NVPO) en pacientes que no recibían quimioterapia bajo anestesia general. En estos estudios, se observaron reacciones adversas adicionales con una mayor incidencia que el comparador activo (ondansetrón) incluyeron: ALT elevada, dolor abdominal alto, sonidos intestinales anormales, disartria, disnea, hipoestesia, insomnio, miosis, náusea, incomodidad sensorial estomacal, agudeza visual reducida, sibilancias.
Además, dos eventos adversos serios fueron reportados en estudios clínicos en NVPO en pacientes que tomaban altas dosis de aprepitant: Un caso de estreñimiento y otro caso de sub ileo.
Se reportó un caso de angioedema y urticaria como reacción adversa seria en un paciente que recibió aprepitant en un estudio no relacionado con NVIQ ni NVPQ.
Experiencia Postcomercialización: Las siguientes reacciones adversas han sido identificadas durante la postcomercialización con aprepitant. Debido a que estas reacciones son reportadas voluntariamente por una muestra de población no determinada, no es posible generalmente un estimado confiable de la frecuencia o establecer una relación causal con el fármaco.
— Trastornos cutáneos y subcutáneos: Prurito, erupción, urticaria, raramente síndrome de Stevens-Johnson/necrolisis epidérmica tóxica.
— Trastornos del sistema inmunológico: Reacciones de hipersensibilidad, incluyendo reacciones anafilácticas.
Se han observado reacciones de hipersensibilidad inmediata durante la infusión de fosaprepitant, que incluyen lo siguiente: Sofoco, eritema, disnea (véase Precauciones).
INTERACCIONES MEDICAMENTOSAS: Tras la administración de fosaprepitant, es probable que ocurran interacciones medicamentosas con los fármacos que interactúan con aprepitant. La siguiente información se derivó a partir de datos con aprepitant por vía oral y de estudios realizados de fosaprepitant con administración conjunta con dexametasona, midazolam o diltiazem.
El aprepitant actúa como sustrato, inhibidor débil a moderado e inductor de la isoenzima CYP3A4. El aprepitant también actúa como inductor de la isoenzima CYP2C9.
EMEND® IV 150 mg, administrado como una dosis única, es un inhibidor débil de CYP3A4 y no induce la CYP3A4. Se anticipa que EMEND® IV 150 mg podría causar menor, o no mayor, inducción de la CYP2C9 que la ocasionada tras la administración de aprepitant.
EFECTOS DE OTROS FÁRMACOS SOBRE LA FARMACOCINÉTICA DE APREPITANT: El aprepitant es un sustrato de la isoenzima CYP3A4; por lo tanto, la administración conjunta de fosaprepitant o aprepitant con fármacos que inhiben la actividad de la CYP3A4 puede aumentar las concentraciones plasmáticas de aprepitant. Por lo que, se debe tener precaución al administrar fosaprepitant o aprepitant junto con inhibidores potentes de la CYP3A4 (p. ej., ketoconazol), pero la administración conjunta de aprepitant con inhibidores moderados de la CYP3A4 (p. ej., diltiazem) no provocó cambios significativos en las concentraciones plasmáticas.
El aprepitant es un sustrato de la isoenzima CYP3A4; por lo tanto, la administración de fosaprepitant o aprepitant junto con fármacos que inducen potentemente la actividad de la CYP3A4 (p. ej.: Rifampicina) puede disminuir las concentraciones plasmáticas de aprepitant y, en consecuencia, la eficacia.
Ketoconazol: Cuando se administró una sola dosis de 125 mg de aprepitant por vía oral el día 5 de un régimen de diez días con 400 mg/día de ketoconazol, un inhibidor potente de la CYP3A4, el ABC de aprepitant aumentó aproximadamente 5 veces, y su semivida terminal media aumentó aproximadamente tres veces. Se debe tener precaución al administrar fosaprepitant o aprepitant junto con inhibidores potentes de la CYP3A4.
Rifampicina: Cuando se administró una sola dosis de 375 mg de aprepitant por vía oral el día 9 de un régimen de 14 días con 600 mg/día de rifampicina, un inductor potente de la CYP3A4, el ABC de aprepitant se redujo aproximadamente 11 veces, y su semivida terminal media disminuyó aproximadamente 3 veces. La administración conjunta de fosaprepitant o aprepitant con fármacos que inducen la actividad de la CYP3A4 puede disminuir las concentraciones plasmáticas y, en consecuencia, la eficacia.
Otras interacciones
Diltiazem: En pacientes con hipertensión leve a moderada, la infusión de 100 mg de fosaprepitant en el curso de 15 minutos, simultánea con la administración de 120 mg de diltiazem tres veces al día, aumentó 1.5 veces el ABC de aprepitant y 1.4 veces el ABC de diltiazem. Los efectos farmacocinéticos ocasionaron una reducción ligera, pero clínicamente importante, de la presión arterial diastólica (reducción de 16.8 mmHg con fosaprepitant, comparada con 10.5 mmHg sin fosaprepitant) y pueden ocasionar una reducción ligera, pero clínicamente importante, de la presión arterial sistólica (reducción de 24.4 mmHg con fosaprepitant, comparada con 18.8 mmHg sin fosaprepitant), pero no hubo cambios clínicamente importantes en la frecuencia cardiaca ni en el intervalo PR, más allá de los cambios inducidos por diltiazem solo.
En el mismo estudio, la administración de aprepitant una vez al día (en una presentación en tableta, comparable con 230 mg de la presentación en cápsula), simultánea con la administración de 120 mg de diltiazem tres veces al día durante 5 días, aumentó al doble el ABC de aprepitant y 1.7 veces el ABC de diltiazem. Estos efectos farmacocinéticos no causaron cambios importantes en el electrocardiograma, la frecuencia cardiaca ni la presión arterial, mayores que los inducidos por diltiazem solo.
Paroxetina: La administración simultánea de dosis únicas diarias de aprepitant (en una presentación en tableta comparable con 85 mg o 170 mg de la presentación en cápsula), con 20 mg de paroxetina una vez al día, redujo el ABC aproximadamente 25% y la Cmáx aproximadamente 20%, tanto de aprepitant como de paroxetina.
EFECTOS DEL APREPITANT SOBRE LA FARMACOCINÉTICA DE OTROS FÁRMACOS: Aprepitant, al ser un inhibidor débil a moderado de la enzima CYP3A4 y EMEND® IV 150 mg, al ser un inhibidor débil de la CYP3A4, pueden aumentar las concentraciones plasmáticas de los medicamentos por vía oral, metabolizados por esa enzima, que se administren simultáneamente.
El fosaprepitant no se debe usar simultáneamente con pimozida, terfenadina, astemizol o cisaprida. La inhibición de la isoenzima CYP3A4 por aprepitant podría aumentar las concentraciones plasmáticas de estos fármacos y causar reacciones graves o potencialmente mortales (véase Contraindicaciones). Se Debe tener precaución durante la administración conjunta de fosaprepitant y la administración, por vía oral, de sustancias activas que se metabolizan principalmente a través de la enzima CYP3A4 y con un rango terapéutico estrecho tales como: Tacrolimus, sirolimus,everolimus, alfentanilo, diergotamina, ergotamina, fentanilo y quinidina (véase Precauciones/advertencias).
Se ha demostrado que aprepitant induce el metabolismo de la S(-) warfarina y de la tolbutamida, que se metabolizan por la isoenzima CYP2C9. La administración conjunta de fosaprepitant o aprepitant con estos u otros medicamentos que son metabolizados por la CYP2C9, como la fenitoína, puede disminuir las concentraciones plasmáticas de estos medicamentos.
Es poco probable que fosaprepitant o aprepitant interactúen con los fármacos que son sustratos del transportador de P-glucoproteínas, como lo demostró la nula interacción de aprepitant por vía oral con digoxina en un estudio clínico sobre interacciones medicamentosas.
Antagonistas de la 5-HT3: En los estudios clínicos sobre interacciones medicamentosas, aprepitant, cuando se administró en un régimen de 125 mg en el día 1 y 80 mg en los días 2 y 3, no tuvo efectos, de importancia clínica, sobre la farmacocinética de ondansetrón, granisetrón o hidrodolasetrón (el metabolito activo de dolasetrón).
Corticosteroides
Dexametasona: Cuando se administró fosaprepitant 150 mg como una dosis intravenosa única en el día 1, aumentó el ABC0-24hrs de dexametasona, un substrato de la isoenzima CYP3A4, aproximadamente 2 veces más en los días 1 y 2 cuando la dexametasona se administró conjuntamente con una dosis única de 8 mg por vía oral en los día 1, 2 y 3. La dosis oral de dexametasona en los días 1 y 2 se debe reducir aproximadamente en un 50% cuando se administra en conjunto con fosaprepitant 150 mg I.V. en el día 1, para alcanzar exposiciones de dexametasona similares a aquellas obtenidas cuando se administra sin fosaprepitant 150 mg.
El aprepitant por vía oral, cuando se da en un régimen de 125 mg en combinación con 20 mg de dexametasona por vía oral el día 1 y cuando se administró aprepitant por vía oral en dosis de 80 mg/día combinados con 8 mg de dexametasona por vía oral los días 2 al 5, aprepitant aumentó 2.2 veces el ABC de la dexametasona, un sustrato de la isoenzima CYP3A4, los Días 1 y 5. La dosis habitual de dexametasona se debe reducir en aproximadamente un 50% cuando se administra conjuntamente con un régimen de fosaprepitant 115 mg seguido por aprepitant, para lograr exposiciones de la dexametasona similares a las que se obtienen cuando se administra sin aprepitant. En los estudios clínicos para tratamiento de náusea y vómito inducidos por quimioterapia con aprepitant por vía oral, la dosis diaria de dexametasona administrada reflejauna reducción aproximada del 50% (véase Dosis y vía de administración).
Metilprednisolona: Cuando se administró aprepitant por vía oral en un régimen de 125 mg combinados con 125 mg de metilprednisolona por vía intravenosa el día 1 y aprepitant por vía oral en dosis de 80 mg/día combinados con 125 mg de metilprednisolona por vía intravenosa los días 2 y 3, aprepitant aumentó 1.3 veces el ABC de la metilprednisolona el día 1 y 2.5 veces el día 3. Las dosis habituales de metilprednisolona por vía intravenosa se deben reducir aproximadamente en un 25% y las dosis habituales de metilprednisolona por vía oral se deben reducirse aproximadamente en un 50%, cuando se administra conjuntamente con un régimen de fosaprepitant 115 mg, seguido por aprepitant, para lograr exposiciones de la metilprednisolona similares a las que se obtienen cuando se administra sin aprepitant.
Agentes quimioterapéuticos: En los estudios clínicos, se administró el régimen de aprepitant con los siguientes agentes quimioterapéuticos, que son metabolizados principalmente o en parte por la isoenzima CYP3A4: Etopósido, vinorelbina, docetaxel y paclitaxel. Las dosis de estos medicamentos no se ajustaron en virtud de las posibles interacciones farmacológicas.
Docetaxel: En un estudio farmacocinético separado, aprepitant por vía oral (en un régimen para NVIQ) no influyó en la farmacocinética de docetaxel.
Vinorelbina: En un estudio farmacocinético separado, aprepitant por vía oral (en un régimen para NVIQ) no influyó en la farmacocinética de vinorelbina.
Warfarina: Se administró una dosis única de 125 mg de aprepitant por vía oral el día 1 y 80 mg/día los días 2 y 3 a sujetos sanos estabilizados bajo tratamiento crónico con warfarina. Aunque aprepitant por vía oral no tuvo ningún efecto sobre el ABC de la warfarina R(+) o S(-) medida el día 3, cinco días después de terminar la administración de aprepitant por vía oral se observó una disminución de 34% en la concentración mínima de warfarina S(-) (un sustrato de la CYP2C9), acompañada de una reducción de 14% en el tiempo de protrombina (reportado como rango internacional normalizado, o INR). En los pacientes bajo tratamiento crónico con warfarina, se debe vigilar estrechamente el tiempo de protrombina (INR) durante el periodo de dos semanas, en particular entre los 7 y 10 días, después de iniciar cada ciclo de quimioterapia.
Tolbutamida: La administración de aprepitant por vía oral en dosis de 125 mg el día 1 y de 80 mg/día los días 2 y 3 redujo el ABC de la tolbutamida (un sustrato de la isoenzima CYP2C9) 23% el día 4, 28% el día 8 y 15% el día 15, cuando se administró una dosis de 500 mg de tolbutamida por vía oral antes de administrar el régimen de tres días de aprepitant por vía oral y los días 4, 8 y 15.
Anticonceptivos por vía oral: La administración de una cápsula de 100 mg de aprepitant por vía oral una vez al día durante 14 días junto con un anticonceptivo por vía oral con 35 mcg de etinilestradiol y 1 mg de noretindrona disminuyó 43% el ABC de etinilestradiol y 8% el ABC de noretindrona.
En otro estudio, se administró un anticonceptivo por vía oral que contenía etinilestradiol y noretindrona en dosis única los días 1 al 21 junto con aprepitant por vía oral, administrado en un régimen de 125 mg el día 8 y 80 mg/día los días 9 y 10 combinado con 32 mg de ondansetrón IV el día 8 y dexametasona por vía oral, 12 mg el día 8 y 8 mg/día los días 9, 10 y 11. En el estudio, el ABC de etinilestradiol disminuyó 19% el día 10 y las concentraciones mínimas de etinilestradiol se redujeron hasta 64% durante los días 9 al 21. Si bien aprepitant por vía oral no tuvo efecto alguno sobre el ABC de la noretindrona el día 10, hubo una reducción de hasta 60% en las concentraciones mínimas de noretindrona durante los días 9 al 21.
La eficacia de los anticonceptivos hormonales puede disminuir durante la administración de fosaprepitant o aprepitant y en los 28 días siguientes. Se deben usar métodos anticonceptivos alternativos o de respaldo durante el tratamiento con fosaprepitant o aprepitant y durante un mes después de la última dosis.
Midazolam: La administración de 150 mg de fosaprepitant IV el día 1, aumentó el ABC0-8 de midazolam aproximadamente 1.8 veces en el día 1 y no tuvo efectos (1.0 veces) en el día 4 cuando se administró midazolam conjuntamente a una dosis de 2 mg vía oral en los día 1 al 4. Fosaprepitant 150 mg IV es un inhibidor débil del sustrato de la isoenzima CYP3A4 en una dosis única en el día 1 sin evidencia de inhibición o inducción del CYP3A4 observada al día 4.
Además, cuando se administró fosaprepitant a una dosis de 100 mg durante 15 minutos junto con una dosis de midazolam de 2 mg, el ABC plasmático de midazolam aumentó 1.6 veces. El efecto no fue considerado clínicamente importante.
El ABC de midazolam aumentó 2.3 veces el día 1 y 3.3 veces el día 5, cuando se administró conjuntamente una dosis por vía oral única de 2 mg de midazolam los días 1 y 5 de un régimen de 125 mg de aprepitant por vía oral el día 1 y 80 mg/día los días 2 al 5. Se deben considerar los efectos potenciales del aumento de las concentraciones plasmáticas de midazolam o de otras benzodiacepinas que son metabolizadas por la CYP3A4 (alprazolam, triazolam) cuando se administren conjuntamente estos medicamentos con un régimen de tres días de fosaprepitant seguido por aprepitant.
En otro estudio en el que se administró midazolam por vía intravenosa, se administró aprepitant por vía oral en dosis de 125 mg el día 1 y de 80 mg/día los días 2 y 3, y se administraron 2 mg IV de midazolam antes de la administración del régimen de 3 días de aprepitant por vía oral y los días 4, 8 y 15. El aprepitant por vía oral aumentó 25% el ABC de midazolam el día 4 y disminuyó 19% el ABC de midazolam el día 8, en relación con la administración de aprepitant por vía oral los días 1 al 3. Estos efectos no se consideraron clínicamente importantes. El ABC de midazolam el día 15 fue similar al observado al inicio.
Se llevó a cabo un estudio adicional en el que se administró midazolam por vía intravenosa y aprepitant por vía oral. Se administraron 2 mg de midazolam por vía intravenosa 1 hora después de la administración por vía oral de una sola dosis de 125 mg de aprepitant. El ABC de midazolam en plasma aumentó 1.5 veces. Este efecto no se consideró clínicamente importante.
FARMACOLOGÍA CLÍNICA: Fosaprepitant, un profármaco de aprepitant, cuando se administra por vía intravenosa se convierte rápidamente en aprepitant, un antagonista de los receptores de la sustancia P de la neurocinasa 1 (NK1). Las concentraciones plasmáticas de fosaprepitant están por debajo del límite de cuantificación (10 ng/ml) en los 30 minutos del cumplimiento de la infusión.
Mecanismo de Acción: Fosaprepitant es un profármaco de aprepitant y de esa manera, sus efectos antieméticos se deben al aprepitant.
Aprepitant tiene un modo de acción único; es un antagonista selectivo de alta afinidad del receptor humano de la sustancia P de la neurocinasa 1 (NK-1). Detecciones contra análisis demostraron que aprepitant fue, al menos, 3,000 veces más selectivo por el receptor NK-1 sobre otras enzimas, transportadores, canales iónicos y receptores, incluyendo receptores de dopamina y serotonina que son el objetivo de las terapias NVIQ existentes.
Se ha demostrado pre-clínicamente, que los antagonistas del receptor NK1 inhiben la emesis inducida por agentes quimioterapéuticos citotóxicos, tales como cisplatino, a través de las acciones centrales. Estudios preclínicos y de tomografía de emisión de positrones (PET) en seres humanos, con aprepitant, han demostrado que penetra al cerebro y ocupa los receptores cerebrales NK-1. Los estudios preclínicos muestran que aprepitant tiene una larga duración de la actividad central, inhibe tanto la fase aguda como tardía de la emesis inducida por cisplatino y aumenta la actividad antiemética del antagonista del receptor 5-HT3, ondansetrón, y del corticosteroide dexametasona, contra la emesis inducida por cisplatino.
DOSIS Y VÍA DE ADMINISTRACIÓN: EMEND® IV (fosaprepitant) para administración intravenosa es un profármaco liofilizado del aprepitant (EMEND®), que contiene polisorbato 80 (PS80). EMEND® IV está disponible en 150 mg para infusión intravenosa (I.V.).
EMEND® IV 150 mg se administra, exclusivamente el día 1, en una infusión de 20 a 30 minutos, aproximadamente 30 minutos antes de la quimioterapia. No se administran cápsulas de EMEND® en los días 2 y 3. EMEND® IV debe administrarse junto con un corticosteroide y un antagonista de la 5-HT3, tal como se especifica en las tablas de abajo.
Régimen de dosificación recomendada para la prevención de náusea y vómito asociados con la quimioterapia anticancerosa altamente emetogénica:
|
Día 1 |
Día 2 |
Día 3 |
Día 4 |
|
|
EMEND® IV |
150 mg IV |
no |
no |
no |
|
Dexametasona** |
12 mg por vía oral |
8 mg por vía oral |
8 mg por vía oral, dos veces al día |
8 mg por vía oral, dos veces al día |
|
Ondansetrón† |
32 mg IV |
no |
no |
no |
|
**La dexametasona se debe administrar 30 minutos antes de la quimioterapia el Día 1, y por la mañana del Día 2 al Día 4. La dosis de dexametasona se debe administrar por la noche en los días 3 y 4. Se debe tomar en cuenta la dosis de dexametasona para las interacciones medicamentosas. †El ondansetrón se debe administrar 30 minutos antes de la quimioterapia el Día 1. |
||||
Régimen de dosificación para la prevención de náusea y vómito asociados con la quimioterapia anticancerosa moderadamente emetogénica:
|
Solo día 1 |
|
|
EMEND® IV |
150 mg IV |
|
Dexametasona** |
12 mg por vía oral |
|
Ondansetrón† |
8 mg por vía oral dos veces al día |
|
**La dexametasona se debe administrar 30 minutos antes de la quimioterapia el Día 1. Tomar en cuenta la dosis de dexametasona para las posibles interacciones farmacológicas. † Se debe administrar una cápsula de 8 mg de ondansetrón 30 a 60 minutos antes de la quimioterapia y una cápsula de 8 mg, 8 horas después de la primera dosis el Día 1. |
|
Preparación de EMEND® IV 150 mg para inyección :
— Introduzca 5 ml de solución salina en el frasco. Cuide que la solución salina escurra despacio por las paredes del frasco, para evitar la formación de espuma. Gire el frasco suavemente. No sacuda ni agite la solución salina en el frasco.
— Prepare una bolsa de infusión con 145 ml de solución salina.
— Extraiga todo el volumen del frasco e inyéctelo en la bolsa de infusión que contiene 145 ml de solución salina, para obtener un volumen total de 150 ml. Invierta la bolsa suavemente, dos o tres veces.
Una vez preparada, la solución con el medicamento se mantiene estable durante 24 horas a temperatura ambiente (a 25 °C o menos).
Los productos farmacéuticos parenterales deben someterse a inspección visual en busca de partículas flotantes y cambios de coloración antes de administrarlos, siempre que la solución y el recipiente lo permitan.
EMEND® IV es incompatible con cualquier solución que contenga cationes divalentes (p. ej., Ca2+, Mg2+), tales como la solución de Hartman y la solución de lactato de Ringer. EMEND® IV no debe reconstituirse ni mezclarse con soluciones con las cuales no se haya demostrado su compatibilidad física y química.
Información general: Véase Interacciones medicamentosas, para mayor información sobre la administración de EMEND® IV con corticosteroides.
Consulte la información completa de prescripción para obtener información sobre la administración conjunta de fármacos antieméticos.
No es necesario ajustar la dosificación en los pacientes según la edad, sexo, raza o índice de masa corporal (IMC).
No es necesario ajustar la dosificación en los pacientes con insuficiencia renal grave (depuración de creatinina menor a 30 ml/min) ni en los pacientes con nefropatía terminal sometidos a hemodiálisis.
No es necesario ajustar la dosificación en los pacientes con insuficiencia hepática leve a moderada (puntuación de Child-Pugh de 5 a 9). No hay datos clínicos relativos a los pacientes con insuficiencia hepática grave (puntuación de Child-Pugh mayor de 9).
USO PEDIÁTRICO: No se han determinado la seguridad ni la eficacia de EMEND® IV en pacientes pediátricos.
SOBREDOSIS: No hay información específica sobre el tratamiento de las sobredosis. Las dosis únicas de hasta 200 mg de fosaprepitant IV y 600 mg de aprepitant fueron generalmente bien toleradas en los sujetos sanos. Tres de 33 sujetos que recibieron 200 mg de fosaprepitant presentaron trombosis leve en el sitio de la inyección. El aprepitant fue generalmente bien tolerado cuando se administró en dosis de 375 mg una vez al día a pacientes en estudios no relacionados con náusea y vómito inducidos por quimioterapia. En 33 pacientes con cáncer, la administración de una dosis única de 375 mg de aprepitant el día 1 y de 250 mg una vez al día los días 2 al 5 fue generalmente bien tolerada.
En un paciente que ingirió 1,440 mg de aprepitant se reportó somnolencia y cefalea.
En caso de sobredosis, se debe suspender el uso de EMEND® IV, dar tratamiento general de sostén y mantener al paciente bajo observación. Debido al efecto antiemético de aprepitant, el vómito inducido por medicamentos puede no ser efectivo.
El aprepitant no puede eliminarse mediante hemodiálisis.
CLASE TERAPÉUTICA: EMEND® IV (fosaprepitant dimeglumina al que en lo sucesivo se denominará fosaprepitant), es un profármaco de aprepitant.
Química: Fosaprepitant dimeglumina es un profármaco de aprepitant y se describe químicamente como 1Deoxi-1-(metilamino)-D-glucitol [3-[[(2R,3S)-2-[(1R)-1-[3,5-bis(trifluorometil)fenil]etoxi]-3-(4fluorofenil)-4-morfolinil]metil]-2,5-dihidro-5-oxo-1H-1,2,4-triazol-1-yl]fosfonato (2:1) (sal).
Su fórmula empírica es C23H22F7N4O6P • 2(C7H17NO5) y su fórmula estructural es:
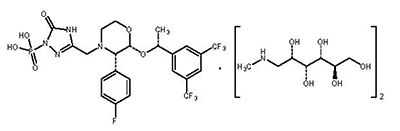
Aprepitant es una sustancia estructuralmente novedosa, antagonista del receptor P de la neurocinasa 1 (NK-1), se describe químicamente como 5-[[(2R,3S)-2-[(1R)-1-[3,5bis(trifluorometil) fenil]etoxi]-3-(4-fluorofenil)-4-morfolinil]metil]-1,2-dihidro-3H-1,2,4-triazol-3-uno.
Su fórmula empírica es C23H21F7N4O3, y su fórmula estructural es:
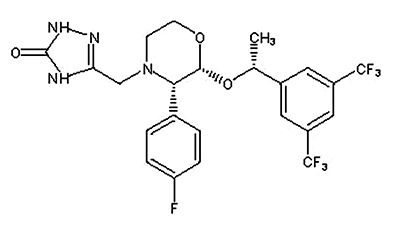
PRESENTACIÓN: EMEND® IV está disponible en una caja con un frasco equivalente a 150 mg de fosaprepitant dimeglumina.
Si requiere mayor información solicítela a la Dirección Médica al Teléfono: (507) 282-7200


ALMACENAMIENTO: Almacénese a 2-8 °C. Luego de la reconstitución, la solución final es estable durante 24 horas a 25 °C o menos.