
ADORLAN
DICLOFENACO SÓDICO, TRAMADOL
Comprimidos
1 Caja, 10 Comprimidos,
1 Caja, 20 Comprimidos,
1 Caja, 30 Comprimidos,
1 Caja, 50 Comprimidos,
COMPOSICIÓN:
Cada COMPRIMIDO contiene:
Diclofenaco sódico 25 mg equivalente a 23,279 mg de diclofenaco base.
Tramadol clorhidrato 25 mg equivalente a 21. 957mg de tramadol base.
Excipientes c. s.
LISTA DE EXCIPIENTES: Celulosa microcristalina, croscarmelosa sódica, dióxido de silicio coloidal anhidro, estearato de magnesio.
INDICACIONES: ADORLAN® está indicado para el alivio del dolor inflamatorio agudo de intensidad moderada a severa.
FARMACODINAMIA:
Grupo farmacoterapéutico: otros opioides; combinaciones de tramadol. Código ATC: N02A X 52.
Tramadol: Tramadol es un analgésico racémico que actúa en el sistema nervioso central. Sus actividades múltiples complementarias residen en los enantiómeros (+) y (-). A concentraciones submicromolares, tramadol (-) inhibe la recaptación sináptica de la norepinefrina (NE) y tramadol (+) inhibe la recaptación sináptica de la serotonina (5-HT). Además, tramadol tiene actividad agonista en los receptores opioides µ a través de los enantiómeros (+) que aumenta en gran medida hacia las afinidades nanomolares en el enantiómero (+) del metabolito O-desmetil-tramadol (M1). A pesar de que las afinidades por los transportadores de monoamina son más bajas que aquellas por el receptor opioide µ, la inhibición de la recaptación de NE y 5-HT contribuye a la actividad antinociceptiva de tramadol.
Diclofenaco: El diclofenaco sódico es un fármaco antiinflamatorio no esteroide (AINE) que exhibe actividades antiinflamatorias, analgésicas y antipiréticas en modelos animales. El mecanismo de acción del diclofenaco sódico, al igual que el de otros AINEs, no se comprende del todo pero puede estar relacionado con la inhibición de la ciclooxigenasa con reducción de la síntesis de prostaglandinas.
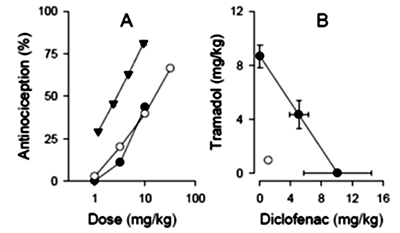
Figura 1. Las curvas dosis-respuesta en la hiperalgesia térmica en ratas después de la administración de diclofenaco (círculos negros), tramadol (círculos abiertos) o la combinación de ambos fármacos (triángulos negros) (A) y el análisis isobolográfico de tal combinación. La combinación de tramadol y diclofenaco a proporciones de dosis equivalentes (círculo abierto) desciende hacia la izquierda y por debajo de la línea de aditividad indicando una interacción supra-aditiva (sinérgica) (B). Los datos se expresan como media ± s.e.m. (n=6).
Fuente: PH242 Rodriguez-Silverio 2011
Efecto antiinflamatorio: En la prueba de edema inducido por carragenina en ratas, la combinación de tramadol y diclofenaco suprimió la formación del edema con un rango de dosis efectiva similar a aquella obtenida con diclofenaco solo. En la misma prueba, el efecto ulcerogénico gástrico de la combinación fue menor que el de diclofenaco. Esto fue indicado por una dosis de umbral dos veces mayor para el efecto ulcerogénico gástrico y un puntaje ulcerogénico menor que fue 3.45 para la combinación a 21.5 mg/kg p.o. y 6.0 para diclofenaco a la misma dosis.
Experiencia clínica: De conformidad con los resultados preclínicos, la combinación de tramadol y diclofenaco ofreció un mejor alivio del dolor en seres humanos con dolor postoperatorio en comparación con la monoterapia con tramadol o diclofenaco.
ADORLAN® está posicionado como un analgésico del escalón II en la escalera analgésica de dolor de la OMS y debe utilizarse de acuerdo con las instrucciones del médico.
FARMACOCINÉTICA:
Absorción y biodisponibilidad: Más del 90% de tramadol es absorbido después de la administración oral. La biodisponibilidad media absoluta después de una dosis oral única es de alrededor del 70% independientemente de la ingestión concomitante de alimentos. La diferencia entre la absorción y la biodisponibilidad absoluta de tramadol se debe probablemente al efecto de primer paso. Después de la administración oral, el efecto de primer paso es un máximo de 30%. Las concentraciones máximas séricas se alcanzan aproximadamente 1.5 a 2 horas después de la administración. Después de la administración oral repetida, el estado estacionario se alcanza en 36 horas. Las concentraciones de estado estacionario son 30 % a 40 %mayores que aquellas extrapoladas de una administración de dosis única. Estas concentraciones mayores son probablemente causadas por la saturación del metabolismo de primer paso.
La absorción de diclofenaco es completa pero su inicio es retardado hasta el paso a través del estómago que puede ser afectado por alimentos, lo cual retrasa el vaciado del estómago. La media de la concentración plasmática pico de diclofenaco se alcanza después de aproximadamente 2 horas. Alrededor de la mitad de diclofenaco administrado es metabolizada durante su primer paso a través del hígado (efecto de “primer paso”), el área por debajo de la curva de concentración (AUC) después de la administración oral es aproximadamente la mitad de aquella después de una dosis parenteral equivalente.
El comportamiento farmacocinético no se altera con la administración repetida. No ocurre acumulación, siempre que se observen los intervalos de dosificación recomendados.
Distribución: Tramadol se distribuye de forma amplia y rápida. El volumen total de distribución según fue determinado en 12 estudios i.v. variaba entre 203 ± 40 L y 290 ± 37 L. Solamente alrededor del 20% del tramadol administrado se liga a proteínas. Tramadol atraviesa la barrera placentaria y una cantidad muy pequeña de tramadol inalterado y M1 (aprox. 0.1% de la dosis materna administrada) entra en la lecha materna de madres lactantes.
El 99.7% del diclofenaco se une a las proteínas, principalmente a la albúmina (99.4%). El diclofenaco entra en el líquido sinovial, donde se determinan concentraciones máximas 2 a 4 horas después de que se hayan alcanzado las concentraciones plasmáticas máximas. La vida media de eliminación aparente del líquido sinovial es de 3-6 horas. Dos horas después de alcanzar los valores plasmáticos pico, las concentraciones de la sustancia activa ya son mayores en el líquido sinovial que en el plasma, y se mantienen más elevadas durante un periodo de hasta 12 horas.
Metabolismo: Se han encontrado más de 11 metabolitos de tramadol en la orina humana. Las rutas metabólicas principales son la N- y O-desmetilación y la conjugación de los derivados de O-desmetilo con el ácido glucurónico y sulfúrico.
Solamente un metabolito, (+)-O-desmetiltramadol, es farmacológicamente activo. Este metabolito tiene propiedades antinociceptivas originadas por la unión al receptor opioide µ.
Varias isoenzimas hepáticas están involucradas en el metabolismo de tramadol; CYP2D6 está principalmente involucrada en la O-desmetilación mientras que CYP3A4 y CYP2B6 son responsables de la N-desmetilación. La inhibición de una de estas isoenzimas involucradas en la biotransformación de tramadol puede afectar la concentración plasmática de tramadol o de su metabolito activo. Hasta ahora, no se han reportado interacciones clínicamente relevantes.
Un estudio de inhibición in vitro mostró que tramadol no tiene un efecto inhibidor clínicamente relevante en las isoformas del citocromo P450 principales a concentraciones terapéuticas.
La biotransformación de diclofenaco se lleva a cabo en parte por la glucuronidación de la molécula intacta, pero principalmente por la hidroxilación y metoxilación única y múltiple que resulta en varios metabolitos fenólicos, la mayoría de los cuales son convertidos a conjugados de glucurónido. Dos de los metabolitos fenólicos son biológicamente activos, pero en un grado mucho menor que el diclofenaco.
Eliminación: Tramadol y sus metabolitos se eliminan casi exclusivamente por los riñones. Ocurre también cierta excreción biliar pero es de menor importancia.
El aclaramiento total según fue determinado en 12 estudios i.v. variaba entre 432 ± 53 mL/min y 607 ± 130 mL/min.
La vida media plasmática promedio terminal del tramadol es de 5 a 7 horas independientemente de la vía de administración. La vida media terminal de M1 es comparable a la de tramadol.
El aclaramiento sistémico total de diclofenaco del plasma es de 263 ± 56 mL/min (media ± SD). La vida media plasmática terminal es de 1-2 horas. Cuatro de los metabolitos, incluyendo los dos activos, también tienen vidas medias cortas en el plasma de 1-3 horas.
Aproximadamente 60% de la dosis administrada es excretada en la orina en la forma del conjugado glucorónido de la molécula intacta y en forma de metabolitos, la mayoría de los cuales también son convertidos en conjugados glucorónidos. Menos del 1% es excretado como sustancia inalterada. El resto de la dosis es eliminado como metabolitos a través de la bilis en las heces.
Tramadol/diclofenaco: Un análisis farmacocinético de población en pacientes post-cesárea no mostró indicios de ningún efecto de diclofenaco en la farmacocinética de disposición de tramadol o su metabolito activo O-desmetil tramadol.
No hay indicios de un potencial de interacción entre tramadol y diclofenaco después de la administración intravenosa y oral en perros.
Datos preclínicos de seguridad:
Tramadol: Tras la administración repetida oral y parenteral de tramadol durante 6 - 26 semanas a ratas y perros, así como durante 12 meses por vía oral a perros, las pruebas hematológicas, clínico-químicos e histológicas no mostraron evidencia de cambios relacionados con la sustancia.
Hubo manifestaciones en el sistema nervioso central sólo tras la administración de dosis elevadas superiores a la dosis terapéutica: excitación, salivación, espasmos y reducción en el aumento de peso. Ratas y perros toleraron, sin reacción alguna, dosis orales de 20 mg/kg y 10 mg/kg de peso corporal respectivamente; los perros toleraron dosis administradas por vía rectal de 20 mg/kg de peso corporal, sin ningún efecto.
Los resultados de las pruebas de mutagenicidad no revelaron un riesgo genotóxico potencial asociado al uso de clorhidrato de tramadol en el hombre. Los resultados de las pruebas de carcinogenicidad no indican que el clorhidrato de tramadol suponga un riesgo potencial para el hombre. Los estudios de toxicidad reproductiva con clorhidrato de tramadol revelaron, a dosis tóxicas maternas, desarrollo y osificación retardados y mortalidad neonatal. No se afectaron el rendimiento reproductivo, fertilidad y desarrollo de las crías. Tramadol atraviesa la placenta. No se ha observado ningún efecto sobre la fertilidad después de la administración oral de tramadol.
Diclofenaco: Con la administración repetida a animales, la toxicidad crónica de diclofenaco fue particularmente evidente en forma de lesiones y ulceraciones en el tracto gastrointestinal. Durante un estudio de toxicidad de 2 años en ratas, se observó un aumento dependiente de la dosis de oclusiones trombóticas de los vasos cardiacos en ratas tratadas con diclofenaco.
En estudios sobre toxicidad reproductiva, diclofenaco causó una inhibición de la ovulación en conejos así como el deterioro de la implantación y el desarrollo embrionario temprano en ratas. El período de gestación y parto se prolongaron con diclofenaco. Efectos embriotóxicos como aborto y retraso de crecimiento en ratas, ratones y conejos se observaron a dosis maternotóxicas. Basándose en los datos disponibles, diclofenaco se clasifica como no teratogénico. Dosis menores al umbral maternotóxico no tienen influencia en el desarrollo postnatal de la progenie.
Tramadol/diclofenaco: La administración intravenosa en bolo de HCl de tramadol y diclofenaco (3 mg/kg + 1.5 mg/kg) causó ligeros efectos cardiovasculares y respiratorios (p.ej. disminuciones de la presión arterial, el ritmo cardiaco y frecuencia respiratoria) en conejos anestesiados.
En un estudio de toxicidad de dosis orales repetidas en ratas, la administración de HCl de tramadol de 8 mg/kg y diclofenaco Na de 4 mg/kg por 13 semanas indujo intranquilidad y peritonitis que se asoció con la muerte en 1 de 20 ratas hembra.
En estudios de toxicidad embrio-fetal en ratas y conejos la administración oral de HCl de tramadol de 8 mg/kg y diclofenaco Na de 4 mg/kg no fue teratogénica y no causó retardos de crecimiento fetal ni siquiera con toxicidad materna. Solamente en los conejos aumentó el número de resorciones y se encontró una congestión del hígado en los fetos.
CONTRAINDICACIONES:
En pacientes con hipersensibilidad al tramadol, diclofenaco o cualquiera de los excipientes (ver Excipientes).
En casos de intoxicación aguda con alcohol, medicamentos hipnóticos, analgésicos opioides u otros medicamentos psicotrópicos.
En pacientes que reciben inhibidores de la MAO o que los han tomado en los últimos 14 días (ver Interacciones).
En pacientes con epilepsia no controlada adecuadamente con tratamiento.
En pacientes con historial de broncoespasmo, asma, rinitis o urticaria después de la administración de ácido acetilsalicílico u otros AINEs (antiinflamatorios no esteroideos).
En pacientes con recurrencias actuales o anteriores de úlcera péptica o hemorragia (por lo menos dos episodios distintivos de ulceración o hemorragia demostrados).
En pacientes con antecedentes de hemorragia gastrointestinal o perforación asociados a tratamientos anteriores con AINEs.
En pacientes con hemorragias cerebro vasculares activas u otro tipo de sangramientos activos.
En pacientes con fallo hepático o renal severo.
En pacientes con fallo cardíaco grave (ver Advertencias y precauciones de uso).
Durante el último trimestre del embarazo (ver Embarazo y lactancia).
ADVERTENCIAS Y PRECAUCIONES ESPECIALES DE EMPLEO:
Advertencias:
Se han reportado convulsiones en pacientes a quienes se administra tramadol en los niveles recomendados de dosis. El riesgo puede incrementarse cuando las dosis de clorhidrato de tramadol exceden el límite superior de la dosis diaria recomendada. Además, tramadol puede incrementar el riesgo de presentar convulsiones en pacientes que toman otros medicamentos que disminuyen el umbral convulsivo (ver Interacciones). Los pacientes con epilepsia o aquellos susceptibles a sufrir convulsiones, sólo deben ser tratados con ADORLAN® si existen razones de peso.
Tramadol tiene un bajo potencial de dependencia. En la tolerancia del uso a largo plazo, puede desarrollarse dependencia psíquica y física. En pacientes con tendencia al abuso o dependencia de fármacos, el tratamiento con ADORLAN® sólo debe administrarse por períodos cortos bajo estricta supervisión médica.
ADORLAN® no es recomendado como sustituto en pacientes dependientes de opioides. Aunque es un agonista opioide, tramadol no puede suprimir los síntomas de abstinencia a la morfina.
Debe evitarse el uso de ADORLAN® combinado con AINEs incluyendo inhibidores selectivos de la ciclooxigenasa-2.
Se ha reportado hemorragia, úlceras o perforación gastrointestinal con todos los AINE (incluyendo diclofenaco), en algunos casos con desenlace fatal. Sucede en cualquier momento durante la terapia, con o sin signos de advertencia o antecedentes de eventos gastrointestinales graves.
El riesgo de hemorragia, úlcera o perforación gastrointestinal es mayor con dosis altas de ADORLAN®, en pacientes con historial de úlceras, en particular, con complicaciones de hemorragia o perforación (ver Contraindicaciones), y en pacientes de edad avanzada. Estos pacientes deberán comenzar con la dosis más baja disponible. En estos pacientes y en aquellos que requieran tratamiento concomitante con ácido acetilsalicílico (ASA) en dosis bajas u otros medicamentos que puedan incrementar el riesgo gastrointestinal (ver Interacciones), deberá considerarse la terapia de combinación con agentes protectores (p. ej. misoprostol o inhibidores de la bomba de protones),(ver Interacciones).
Los pacientes con un historial de toxicidad gastrointestinal, en particular en edades avanzadas, deberán reportar cualquier síntoma abdominal inusual (en particular, hemorragia gastrointestinal), especialmente al inicio del tratamiento. Se deberán tomar precauciones en pacientes que estén tomando de manera concomitante medicamentos que puedan incrementar el riesgo de úlceras o hemorragia, p. ej. corticosteroides orales, anticoagulantes como warfarina, inhibidores selectivos de la recaptación de serotonina o inhibidores de la agregación trombocitaria como ASA (ver Interacciones).
En caso de ocurrir hemorragia gastrointestinal o úlceras durante el tratamiento con ADORLAN® el tratamiento debe suspenderse.
En pacientes con antecedentes de hipertensión y / o fallo cardíaco congestivo de leve a moderado, es necesario el seguimiento y asesoramiento adecuados ya que se han reportado casos de retención de líquidos y edemas asociados al tratamiento con AINEs, incluyendo diclofenaco.
Estudios clínicos y datos epidemiológicos sugieren que el uso de diclofenaco, especialmente en altas dosis (150 mg al día) y en el tratamiento a largo plazo puede estar asociado con un riesgo ligeramente mayor de eventos trombóticos arteriales (p. ej. infarto del miocardio o accidente cerebro vascular).
Durante el tratamiento con AINEs existen reportes muy raros de reacciones cutáneas graves, en algunos casos con resultados fatales, incluyendo dermatitis exfoliativa, síndrome de Stevens-Johnson y necrólisis epidérmica tóxica (síndrome de Lyell), (ver Efectos adversos). El riesgo de estas reacciones parece ser más alto al inicio del tratamiento, ya que en la mayoría de los casos, estas reacciones se produjeron en el primer mes de tratamiento. En los primeros signos de sarpullido, lesiones mucosas u otros signos de una reacción de hipersensibilidad, el uso de ADORLAN® debe descontinuarse.
Al igual que con otros medicamentos anti-inflamatorios no esteroideos, pueden ocurrir reacciones alérgicas, incluyendo reacciones anafilacticas/anafilactoides, sin exposición previa al fármaco. En los primeros signos de una reacción de hipersensibilidad tras la administración de ADORLAN® el tratamiento debe suspenderse. El tratamiento médico adecuado debe de ser instaurado por expertos.
El diclofenaco puede inhibir la agregación plaquetaria transitoriamente. Por lo tanto pacientes con trastornos de la coagulación deben ser monitoreados cuidadosamente.
Al igual que otros AINEs, el diclofenaco puede enmascarar los síntomas de una infección debido a sus propiedades farmacodinámicas. Si durante la administración de ADORLAN® se repiten los síntomas de una infección o se deteriora el estado del paciente, debe indicársele al paciente que consulte inmediatamente a su médico quien deberá comprobar si el tratamiento anti-infeccioso/ antibiótico está indicado.
La administración de analgésicos durante periodos prolongados puede dar lugar a dolores de cabeza que no deben ser tratados mediante el aumento de la dosis del medicamento.
En general, el consumo regular de analgésicos, en particular en combinación con otras sustancias analgésicas, puede provocar daño renal permanente con el riesgo de insuficiencia renal (nefropatía por analgésicos).
El uso concomitante de ADORLAN® y el alcohol puede intensificar los efectos adversos relacionados con el producto, en particular los que afectan al sistema gastrointestinal y el sistema nervioso central.
Precauciones:
Para prevenir la sobredosis, no se deben co-administrar otros productos medicinales que contengan diclofenaco o tramadol. En adultos y mayores de 16 años de edad, la dosis total del diclofenaco no debe exceder de 200 mg/día. lo que resulta para la combinación de dosis fija en una dosis diaria máxima de tramadol de 200 mg/ día.
ADORLAN® se puede usar solamente con particular precaución en pacientes dependientes de opioides, pacientes con lesión en la cabeza, shock, nivel reducido de conciencia de origen desconocido, trastornos del centro o de la función respiratoria, aumento de la presión intracraneal.
En pacientes sensibles a los opioides, ADORLAN® debería sólo ser utilizado con precaución.
Los efectos adversos pueden reducirse administrando la dosis efectiva más baja durante el período más corto necesario para controlar los síntomas (ver Posología y forma de administración y riesgos gastrointestinales y cardiovasculares abajo).
En pacientes de edad avanzada, la incidencia de eventos adversos durante el tratamiento con AINEs (como diclofenaco sódico presente en ADORLAN®) es mayor, en particular, hemorragia y perforación gastrointestinal, en algunos casos con resultados fatales (ver Posología y forma de administración).
En pacientes con un historial de enfermedad gastrointestinal (colitis ulcerativa, enfermedad de Crohn) los AINEs sólo deberán ser utilizados con precaución, ya que la condición del paciente puede deteriorarse (ver Efectos adversos).
Los pacientes con hipertensión no controlada, insuficiencia cardíaca congestiva, cardiopatía isquémica establecida, enfermedad arterial periférica y/o cerebro vascular sólo deben ser tratados con diclofenaco tras una cuidadosa consideración. Se deberán hacer consideraciones similares antes de iniciar el tratamiento a largo plazo en pacientes con factores de riesgo por eventos cardiovasculares (p. ej. hipertensión, hiperlipidemia, diabetes mellitus, tabaquismo).
Una estrecha vigilancia médica es imprescindible en pacientes con deterioro severo de la función hepática (ver Contraindicaciones). Si las pruebas de función hepática anormales persisten o empeoran, si se desarrollan signos o síntomas clínicos consistentes con el desarrollo de la enfermedad hepática o si ocurren otras manifestaciones (eosinofilia, sarpullido), ADORLAN® deberá ser descontinuado. Se puede presentar Hepatitis sin síntomas prodrómicos.
ADORLAN® sólo debe usarse después de una cuidadosa consideración de la relación riesgo /beneficio en pacientes con:
• Trastornos congénitos del metabolismo de las porfirinas, por ejemplo porfiria aguda intermitente.
• Lupus eritematoso sistémico (LES) y enfermedad mixta del tejido conectivo (ver Efectos adversos).
Particularmente es necesaria una cuidadosa supervisión médica en los casos de:
• Disfunción renal.
• Trastornos de la función hepática.
• Inmediatamente después de una cirugía mayor.
• Pacientes que sufren de fiebre del heno, pólipos nasales o enfermedad pulmonar obstructiva crónica, ya que tienen un mayor riesgo de reacciones alérgicas. Estas se pueden presentar en forma de ataques de asma (“asma por analgésicos”), edema angioneurótico o urticaria.
• También es necesario el cuidado especial en pacientes que son alérgicos a otras sustancias, porque también hay un riesgo elevado de reacciones alérgicas con la administración de ADORLAN®.
Con la administración a largo plazo de ADORLAN® la función renal y el recuento de células sanguíneas deben ser controlados a intervalos regulares.
EMBARAZO Y LACTANCIA:
Embarazo: Debido a que ADORLAN® es una combinación fija de ingredientes activos que incluye el diclofenaco, está contraindicado en los últimos tres meses de embarazo. Como ADORLAN® contiene, además, clorhidrato de tramadol, no debe utilizarse durante el embarazo.
Datos respecto al clorhidrato de tramadol: El clorhidrato de tramadol no debe utilizarse durante el embarazo, debido a que no hay disponibles evidencia apropiada para evaluar la seguridad de clorhidrato de tramadol en mujeres embarazadas. El clorhidrato de tramadol administrado antes o durante el nacimiento no afecta la contractilidad uterina. En los recién nacidos puede inducir cambios en la frecuencia respiratoria que normalmente no son clínicamente relevantes. El tratamiento a largo plazo durante el embarazo puede conducir a síntomas de abstinencia en el recién nacido después del parto, como consecuencia de la habituación.
Datos respecto al diclofenaco: Se han reportado anormalidades congénitas en asociación con la administración de AINEs en humanos, sin embargo, estos ocurren en una baja frecuencia y no parecen seguir ningún patrón discernible. En vista de los efectos conocidos de los AINEs en el sistema cardiovascular fetal (el riesgo de cierre del conducto arterioso), está contraindicado su uso en el último trimestre del embarazo. El inicio de la labor de parto puede retrasarse y la duración incrementarse con un aumento en la tendencia de sangrado en la madre y el niño. En los primeros seis meses de embarazo, el diclofenaco deberá administrarse sólo si es absolutamente necesario. Si el diclofenaco es administrado a una mujer que está tratando de quedar embarazada o durante los primeros seis meses de embarazo, la dosis debe ser lo más baja posible y la duración del tratamiento lo más corto posible.
Durante los últimos tres meses del embarazo todos los inhibidores de la síntesis de prostaglandinas. Pueden exponer al feto a los siguientes riesgos:
Toxicidad cardiopulmonar (con oclusión prematura del conducto arterioso e hipertensión pulmonar).
Trastornos de la función renal que conduce a la fallo renal y oligohidramnios.
Exponer a la madre y al niño a los siguientes riesgos al final del embarazo:
Posible prolongación del tiempo de sangrado, inhibición de la agregación trombocitaria, lo que puede ocurrir incluso con dosis muy bajas.
Inhibición de las contracciones uterinas resultando en un retraso o prolongación del parto.
Por lo tanto el diclofenaco está contraindicado en los últimos tres meses del embarazo.
Lactancia: Debido a que ADORLAN® es una combinación fija de sustancias activas incluyendo el clorhidrato de tramadol, no se debe usar durante la lactancia.
Datos respecto al clorhidrato de tramadol: El clorhidrato de tramadol y sus metabolitos se encuentra en pequeñas cantidades en la leche materna humana. Un infante podría ingerir aproximadamente 0,1% de la dosis administrada a la madre. El clorhidrato de tramadol no debe ser ingerido durante la lactancia.
Datos respecto al diclofenaco: Pequeñas cantidades de la sustancia activa diclofenaco y sus metabolitos pasan a la leche materna. Hasta el momento no se han reportado efectos negativos en el infante, y por tanto en la administración a corto plazo, generalmente no es necesario interrumpir la lactancia. Si se receta la administración a largo plazo o de dosis elevadas para enfermedades reumáticas, se deberá considerar la descontinuación temprana de la lactancia.
EFECTOS SOBRE LA CAPACIDAD PARA CONDUCIR Y UTILIZAR MAQUINARIA: Aun cuando se tome de acuerdo con las instrucciones, ADORLAN®, puede ocasionar efectos secundarios en el sistema nervioso central como fatiga, somnolencia y mareos, por lo tanto puede afectar a las reacciones de los conductores de vehículos y de operarios de maquinarias. Esto aplica particularmente con dosificaciones elevadas o en conjunto con otras sustancias sicotrópicas, particularmente el alcohol.
EFECTOS ADVERSOS: Los efectos adversos más comúnmente reportadas para la combinación de clorhidrato de tramadol y diclofenaco; fueron: náuseas, mareos y somnolencia, observados en más del 10% de los pacientes.
Las frecuencias se definen como se indica a continuación:
Muy Común: > 1 / 10
Común: > 1 / 100, <1 / 10
Poco común: > 1 / 1000, <1 / 100
Raros: > 1 / 10 000, <1 / 1000
Muy raros: <1 / 10 000
Frecuencia no conocida: no puede estimarse a partir de los datos disponibles. Dentro de cada grupo de frecuencia, las reacciones adversas se presentan en orden decreciente de gravedad.
Trastornos sanguíneos y del sistema linfático:
Muy raros: dishematopoyesis (anemia aplásica, leucopenia, trombocitopenia, pancitopenia, agranulocitosis), anemia hemolítica. Los primeros signos pueden ser fiebre, dolor de garganta, heridas superficiales en la boca, síntomas parecidos a la gripe, agotamiento severo, sangrados por la nariz y sangrado de la piel.
Trastornos cardiacos:
Poco común: palpitaciones, taquicardia. Estas reacciones adversas pueden ocurrir especialmente en pacientes que se encuentran físicamente estresados.
Raros: Bradicardia
Muy raros: Fallo cardíaco congestivo, infarto del miocardio.
Los estudios clínicos y datos epidemiológicos sugieren que el uso de diclofenaco, en particular en dosis elevadas (150 mg al día) y en el tratamiento a largo plazo puede estar asociado con un riesgo ligeramente elevado de eventos trombóticos arteriales (por ejemplo infarto al miocardio o accidente cerebro vascular).
Trastornos oculares:
Raros: Visión borrosa, miosis, midriasis.
Muy raros: Disfunción visual (visión doble).
Trastornos del oído y del laberinto:
Muy raros: Tinitus, trastornos auditivos transitorios.
Trastornos gastrointestinales:
Muy Común: Molestias gastrointestinales como náuseas, vómitos, diarrea y hemorragia gastrointestinal, que en casos excepcionales puede causar anemia.
Común: Estreñimiento, boca seca, dolor abdominal, dispepsia, flatulencia, calambres abdominales, úlceras gastrointestinales (posiblemente con hemorragia y perforación)
Poco común: Arcadas, malestar gastrointestinal (sensación de presión en el estómago, distensión abdominal), hematemesis, melena o diarrea con sangrado.
Muy raros: Estomatitis, glositis, lesiones esofágicas, molestias en el abdomen inferior (por ejemplo, colitis hemorrágica o colitis ulcerativa exacerbada/ enfermedad de Crohn), pancreatitis, estenosis intestinal diafragmática.
Se le pide al paciente que suspenda el medicamento en caso de que se presente dolor abdominal superior grave, melena o hematemesis y consultar inmediatamente a un médico.
Trastornos generales y condiciones del sitio de administración:
Común: Fatiga.
Poco Común: Edema, particularmente en pacientes con hipertensión arterial o insuficiencia renal.
Trastornos hepato-biliares:
Común: Transaminasas elevadas.
Poco común: Lesión hepática, en particular, en el tratamiento a largo plazo, hepatitis aguda con o sin ictericia.
Muy raros: Hepatitis fulminante.
Infecciones e infestaciones:
Muy raros: Ha habido reportes de un deterioro en la inflamación relacionada con la infección (e.j. desarrollo de fascitis necrotizante) en relación temporal con la administración sistémica de AINEs (como diclofenaco sódico presente en ADORLAN®). Esto posiblemente está relacionado con el mecanismo de acción de los AINEs.
Reportes de meningitis aséptica (especialmente en pacientes con trastornos autoinmunes existentes, como lupus eritematoso sistémico, enfermedad mixta del tejido conectivo) con síntomas como rigidez de cuello, dolor de cabeza, náusea, vómito, fiebre o desorientación.
Investigaciones:
Muy raros: Disminución de hemoglobina.
Trastornos del sistema inmunológico:
Raros: Hipersensibilidad. Puede presentarse en forma de edema facial, inflamación de la lengua y la laringe interna con constricción del tracto respiratorio (edema angioneurótico) disnea, broncoespasmo, taquicardia, sibilancias, hipotensión que culmina en shock inminente, anafilaxia.
En el caso de que uno de estos síntomas se presente, que puede presentarse incluso cuando la preparación se usa por primera vez, se deberá descontinuar y será necesario el tratamiento médico inmediato.
Metabolismo y trastornos nutricionales:
Común: Apetito disminuido.
Raros: Cambios en el apetito.
Trastornos músculo esqueléticos y del tejido conectivo:
Raros: Debilidad motora.
Trastornos del sistema nervioso:
Muy Común: Mareos.
Común: Dolor de cabeza, somnolencia, agitación, irritabilidad
Raros: Trastornos del habla, parestesia, temblores, convulsiones, contracciones musculares involuntarias, coordinación anormal, síncope.
Las convulsiones ocurrieron principalmente después de la administración de dosis elevadas de tramadol o después del tratamiento concomitante con medicamentos que pueden disminuir el umbral convulsivo. (ver Advertencias y precauciones e Interacciones).
Muy raros: Desorientación, espasmos musculares, temblores.
Trastornos psiquiátricos:
Raros: Alucinaciones, estado de confusión, alteración del sueño, delirio, ansiedad y pesadillas. Las reacciones psíquicas adversas pueden ocurrir después de la administración de tramadol, las cuales varían individualmente en intensidad y naturaleza (dependiendo de la personalidad y la duración del tratamiento). Estas incluyen cambios en el estado de ánimo (usualmente ánimo eufórico, ocasionalmente disforia), cambios en las actividades (usualmente supresión, ocasionalmente incremento) y cambios en la capacidad cognitiva y sensorial (por ejemplo, comportamiento respecto a la toma de decisiones, trastornos de la percepción). Puede presentarse dependencia a los fármacos. Pueden ocurrir síntomas de síndrome de abstinencia, similares a los que se presentan en la abstinencia de opiáceos, (p. ej. agitación, ansiedad, nerviosismo, insomnio, hiperquinesia, temblores y síntomas gastrointestinales). Otros síntomas que han sido muy raramente observados con la descontinuación de tramadol incluyen: ataques de pánico, ansiedad severa, alucinaciones, parestesias, tinitus y síntomas inusuales del SNC (p. ej. confusión, delirios, despersonalización, desrealización, paranoia).
Muy raros: Depresión.
Trastornos respiratorios, torácicos y mediastinales:
Raros: Depresión respiratoria, disnea.
Si las dosis recomendadas son excedidas considerablemente y se administran de forma concomitante otras substancias depresoras del sistema nervioso central (ver Interacciones) puede ocurrir depresión respiratoria.
Se ha reportado empeoramiento del asma para tramadol (ver Contraindicaciones).
Muy raros: Neumonitis.
Trastornos del sistema renal y urinario:
Poco Común: Retención de fluidos.
Raros: Trastornos de la micción (disuria y retención urinaria).
Muy raros: Daño del tejido renal (nefritis tubulointersticial, necrosis papilar renal) que puede estar acompañado por fallo renal agudo, proteinuria y/o hematuria; síndrome nefrótico.
Trastornos de la piel y del tejido subcutáneo:
Común: Hiperhidrosis, prurito, sarpullido.
Poco común: Alopecia, urticaria.
Muy raros: Eccema, eritema, reacción de fotosensibilidad, púrpura (también púrpura alérgica) y reacciones cutáneas bullosas como el síndrome de Stevens-Johnson y necrólisis epidérmica tóxica (Síndrome de Lyell).
Trastornos vasculares:
Poco común: Regulación cardiovascular (hipotensión postural o colapso cardiovascular).
Muy raros: Hipertensión.
INTERACCIÓN CON OTROS MEDICAMENTOS Y OTRAS FORMAS DE INTERACCIÓN:
ADORLAN® no debe combinarse con inhibidores de la MAO (ver Contraindicaciones). En pacientes tratados con inhibidores de la MAO en los 14 días previos a la utilización del opioide petidina, se han observado interacciones potencialmente mortales en el sistema nervioso central, respiratorio y en la función cardiovascular. No se pueden descartar las mismas interacciones con los inhibidores de la MAO durante el tratamiento con ADORLAN®.
La administración concomitante de ADORLAN® con otros medicamentos depresores del sistema nervioso central (SNC), incluido el alcohol puede potenciar los efectos sobre el SNC (ver Efectos adversos).
Tramadol puede inducir convulsiones y aumentar el potencial de los inhibidores selectivos de la recaptación de serotonina (ISRS), inhibidores de la recaptura de serotonina-norepinefrina (IRSN), antidepresivos tricíclicos, anti psicóticos y otros medicamentos que reducen el umbral para causar convulsiones.
El uso terapéutico concomitante de tramadol y medicamentos serotoninérgicos como los inhibidores selectivos de la recaptación de serotonina (ISRS), los inhibidores de la recaptación de serotonina-norepinefrina (IRSN), los inhibidores de la MAO (ver Contraindicaciones), antidepresivos tricíclicos y mirtazapina pueden ocasionar toxicidad por serotonina.
El síndrome serotoninérgico es probable cuando se observa cualquiera de los signos siguientes:
• Clonus espontáneos.
• Clonus inducible u ocular con agitación o diaforesis.
• Temblor e hiperreflexia.
• Hipertonía y temperatura corporal >38 ºC y clonus ocular o clonus inducible.
El retiro de los medicamentos serotoninérgicos generalmente provoca una rápida mejoría. El tratamiento depende del tipo y gravedad de los síntomas.
Los resultados de los estudios farmacocinéticos han demostrado hasta ahora que con la administración concomitante o previa de cimetidina (inhibidor enzimático) es poco probable que se produzcan interacciones clínicamente relevantes con tramadol. La administración simultánea o previa de carbamazepina (inductor enzimático) puede reducir el efecto analgésico y acortar la duración de la acción.
Otras sustancias activas que inhiben la CYP3A4, como ketoconazol y eritromicina, podrían inhibir el metabolismo de tramadol (N-desmetilación) probablemente también el metabolismo del metabolito activo O-desmetilado. La importancia clínica de esta interacción no se ha estudiado (ver Efectos adversos).
En un número limitado de estudios la aplicación pre o postoperatoria del antiemético antagonista 5HT3 ondansetrón aumentó el requerimiento de tramadol en pacientes con dolor postoperatorio.
Se debe tener precaución durante el tratamiento concomitante con ADORLAN® y derivados de cumarina (p. ej. warfarina) debido a reportes de aumento del INR , con sangrado importante y equimosis en algunos pacientes tratados con tramadol. También los AINEs, incluyendo diclofenaco, pueden intensificar los efectos de los anticoagulantes, como warfarina (ver Advertencias y precauciones).
La administración concomitante de diferentes AINEs puede aumentar el riesgo de úlceras y hemorragias gastrointestinales debido a un efecto sinérgico. Por lo tanto la administración concomitante de ADORLAN® y otros AINEs no está recomendada. (ver Advertencias y Precauciones).
La administración concomitante de ADORLAN® y digoxina o litio puede incrementar la concentración de estos medicamentos en la sangre. Los niveles séricos de litio deben ser monitoreados. Se recomienda el control de los niveles séricos de digoxina.
Medicamentos antiinflamatorios no esteroideos como el diclofenaco pueden atenuar el efecto de los diuréticos y anti hipertensivos. En pacientes con deterioro de la función renal (p. ej. pacientes deshidratados o pacientes ancianos con deterioro de la función renal), la administración concomitante de un inhibidor de la enzima convertidora de angiotensina (IECA) o un antagonista de la angiotensina II, con un medicamento que inhibe la ciclooxigenasa puede deteriorar la función renal con la posibilidad de fallo renal agudo, que suele ser reversible. Por lo tanto esta combinación debe utilizarse únicamente con cuidado, sobre todo en pacientes de edad avanzada. Se debe solicitar a los pacientes tomar cantidades adecuadas de fluidos y se debe considerar hacer verificaciones regulares de los valores renales después del inicio de la terapia de combinación. La administración concomitante de ADORLAN® y de diuréticos ahorradores de potasio puede inducir hipercalemia. Por lo tanto, en tratamiento concomitante, los niveles de potasio se deben monitorizar.
Glucocorticoides: Incremento en el riesgo de hemorragia gastrointestinale. (ver Advertencias y Precauciones).
Inhibidores de la agregación trombocitaria, tales como el ácido acetilsalicílico e Inhibidores selectivos de la recaptura de serotonina (ISRS): Incremento en el riesgo de hemorragia gastrointestinal (ver Advertencias y Precauciones).
La administración de ADORLAN® dentro del lapso de las 24 horas antes o después del metotrexato puede incrementar la concentración de metotrexato en la sangre y aumentar sus efectos tóxicos.
Los AINEs (como diclofenaco sódico contenido en ADORLAN® pueden incrementar la nefrotoxicidad de la ciclosporina).
Los medicamentos que contienen probenecid o sulfinpirazona pueden retrasar la excreción del diclofenaco.
Cuando los AINEs se administran con zidovudina hay un incremento en el riesgo de toxicidad hematológica. Existe evidencia de un aumento en el riesgo de hemartrosis y hematoma en hemofílicos VIH (+) que reciben tratamiento concurrente con zidovudina e ibuprofeno.
MÉTODO DE ADMINISTRACIÓN: Oral.
Los comprimidos no deben ser divididos o masticados. Deben ser ingeridos enteros, con suficiente líquido y no en un ayunas. En caso de un estómago sensible, se recomienda la ingesta con las comidas.
Adultos y adolescentes mayores de 16 años: Una tableta (25 mg de clorhidrato de tramadol, 25 mg de diclofenaco sódico) cada ocho horas (que corresponde a 75 mg de clorhidrato de tramadol, 75 mg de diclofenaco sódico diarios).
Esta dosis puede aumentarse a una tableta (25 mg de clorhidrato de tramadol, 25 mg, de diclofenaco sódico) cada seis horas (100 mg de clorhidrato de tramadol, 100 mg de diclofenaco sódico diarios). El intervalo entre dos dosis únicas debe ser de al menos 6 horas.
La combinación de dosis fija de clorhidrato de tramadol y diclofenaco sódico no debe, bajo ninguna circunstancia, administrarse por más tiempo de lo estrictamente necesario. Si es necesario el tratamiento del dolor a largo plazo con tramadol / diclofenaco en vista de la naturaleza y la gravedad de la enfermedad, debe llevarse a cabo una vigilancia cuidadosa y regular, (si es necesario con interrupciones en el tratamiento) para establecer si es necesario ampliar y en qué grado un tratamiento adicional.
Niños: El uso de la combinación de dosis fija de clorhidrato de tramadol y diclofenaco sódico no se ha establecido en niños menores de 16 años de edad. Por lo tanto el tratamiento no se recomienda en esta población.
Pacientes de geriatría: Generalmente no es necesario un ajuste de dosis en pacientes de hasta 75 años de edad sin insuficiencia renal y/o hepática manifiesta clínicamente. La eliminación del tramadol se puede prolongar en pacientes mayores de 75 años de edad. Por lo tanto, si resulta necesario, el intervalo de dosificación se ampliará de acuerdo con las necesidades del paciente. ADORLAN® debe utilizarse con especial precaución en estos pacientes que en general son más propensos a reacciones adversas de medicamentos antiinflamatorios no-esteroides. La eliminación de clorhidrato de tramadol puede prolongarse en pacientes de edad avanzada (mayores de 75 años).
En particular, se recomienda que la dosis efectiva más baja sea utilizada en pacientes ancianos frágiles o con un bajo peso corporal, y el paciente debe ser monitorizado por posible sangrado Gastrointestinal durante el tratamiento.
Insuficiencia renal/diálisis y disfunción hepática: En los pacientes con insuficiencia renal y/o hepática, la eliminación de tramadol está retardada. En estos pacientes, la prolongación de los intervalos de dosificación debe ser considerada cuidadosamente de acuerdo a las necesidades del paciente.
Para pacientes con disfunción renal y/o hepática severa, el uso de la combinación de dosis fija de clorhidrato de tramadol y diclofenaco sódico no está recomendada (véase Contraindicaciones).
POSOLOGÍA Y FORMA DE ADMINISTRACIÓN: La dosis debe ajustarse de acuerdo a la intensidad del dolor y a la sensibilidad del paciente individual. Generalmente debe seleccionarse la dosis efectiva más baja para analgesia. En adultos y jóvenes mayores de 16 años de edad, la dosis total de diclofenaco no debe exceder los 200 mg/día, resultando para la combinación de dosis fija en una dosis diaria máxima de tramadol de 200 mg/día. A menos que se prescriba de otra manera, ADORLAN® debe ser administrado de la siguiente manera:
SOBREDOSIS:
ADORLAN® es una combinación fija de sustancias activas. En caso de sobredosis, los síntomas pueden incluir los signos y síntomas de toxicidad de clorhidrato de tramadol o diclofenaco o de los dos principios activos.
Síntomas de sobredosis con clorhidrato de tramadol: En principio, en caso de una intoxicación con clorhidrato de tramadol, se esperan síntomas similares a los de otros analgésicos de acción central (opioides). Estos incluyen, en particular, miosis, vómitos, colapso cardiovascular, trastornos de la conciencia hasta el coma, convulsiones y depresión respiratoria hasta paro respiratorio.
Síntomas de una sobredosis con diclofenaco: Trastornos del SNC, tales como dolor de cabeza, mareos, aturidimiento y pérdida del conocimiento (en niños también convulsiones mioclónicas); pueden ocurrir como síntomas de una sobredosis, así como dolor abdominal, náuseas y vómitos. Asimismo es posible que se presenten hemorragia gastrointestinale y trastornos de la función hepática y renal. También pueden ocurrir hipotensión, depresión respiratoria y cianosis.
Tratamiento de la sobredosis: Se deben observar las normas generales para casos de emergencia consistentes en mantener despejadas las vías respiratorias, mantener la respiración y circulación dependiendo de los síntomas. En caso de depresión respiratoria se debe utilizar como antídoto la naloxona. En el caso de convulsiones deben administrarse las benzodiacepinas de acción prolongada (p.ej. diazepam). No existe ningún antídoto específico para diclofenaco.
En caso de intoxicación, la descontaminación gastrointestinal con carbón activado o mediante lavado gástrico sólo se recomienda dentro de las 2 primeras horas después de la ingesta. La descontaminación gastrointestinal en un tiempo posterior puede ser útil en caso de intoxicación con cantidades excepcionalmente grandes.
Mediante hemodiálisis o hemofiltración se eliminan cantidades mínimas de tramadol sérico. Por lo tanto, el tratamiento de la intoxicación aguda causada por ADORLAN® exclusivamente mediante hemodiálisis o hemofiltración no es adecuado para la desintoxicación.
PRESENTACIONES:
ADORLAN® se presenta en cajas con 10, 20, 30 o 50 comprimidos.
CENTRO AMÉRICA Y EL CARIBE
Si desea información adicional consulte al profesional de la salud, o contacte a nuestro Departamento Médico al e-mail: direccionmedica.cam@grunenthal.com; dirección: Torre de las Américas “C” piso 31, Punta Pacífica, ciudad de Panamá (507) 215 5600.
Este material ha sido revisado y aprobado por el Departamento Médico de Grunenthal Centroamérica y El Caribe.
Fecha de revisión local del texto: Mayo-2013.
Elaborado por Tecnandina, S.A. - Ecuador para
GRÜNENTHAL ECUATORIANA C.LTDA - ECUADOR.
CONSERVACIÓN: No almacenar a temperaturas mayores a 30 °C.
Mantener fuera del alcance de los niños. No usar después de la fecha de expiración indicada en el estuche y en el blister de aluminio.
Los medicamentos no se deben eliminar a través del agua o basura de la casa. Consulte a su farmacéutico sobre como eliminar medicamentos que ya no se usan. Estas medidas ayudaran a proteger el medio ambiente.