
VENTANA ROS1 (SP384) RABBIT MONOCLONAL PRIMARY ANTIBODY
Para visualizar el contenido completo de la IPPA (información para prescribir amplia), deberá iniciar sesión.
INTERPRETACIÓN DE LAS TINCIONES Y RESULTADOS PREVISTOS:
El patrón de tinción celular del anticuerpo VENTANA ROS1 (SP384) es principalmente citoplasmático y, excepcionalmente, membranoso y nuclear. Los criterios de evaluación varían en función de la experiencia del anatomopatólogo a la hora de interpretar los resultados de la tinción del ensayo y de determinar si la muestra de la prueba debe someterse a otras pruebas mediante métodos moleculares o citogenéticos. Las directrices de College of American Pathologists, International Association for the Study of Lung Cancer y Association for Molecular Pathology recomiendan someter todos los resultados obtenidos mediante IHC positivos en ROS1 a una confirmación a través de FISH o un método molecular.9 Estas directrices también señalan que las pruebas publicadas en la actualidad no son suficientes para recomendar un sistema específico de puntuación para establecer la positividad en ROS1 y que cada laboratorio debería validar sus propios criterios de interpretación de la tinción a partir de muestras positivas y negativas conocidas.9
ALMACENAMIENTO Y ESTABILIDAD:
Tras la recepción y cuando no se utilice, consérvese de 2-8°C. No lo congele.
Para garantizar una dispensación adecuada del reactivo y la estabilidad del anticuerpo, vuelva a poner el tapón del dispensador después de cada uso y almacene inmediatamente el dispensador en la nevera, en posición vertical.
Todos los dispensadores de anticuerpos tienen una fecha de caducidad. Si se almacena correctamente, el reactivo se mantendrá estable hasta la fecha indicada en la etiqueta. No usar el reactivo después de la fecha de caducidad.
ADVERTENCIAS Y PRECAUCIONES:
1. Para uso diagnóstico in vitro (IVD).
2. Solo para uso profesional.
3. No utilizar por encima del número especificado de ensayos.
4. La solución ProClin 300 se utiliza como conservante en este reactivo. Está clasificada como irritante y puede ocasionar sensibilización por contacto con la piel. Adopte precauciones razonables cuando la manipule. Evite el contacto de los reactivos con los ojos, la piel y las membranas mucosas. Utilice ropa protectora y guantes.
5. Los portaobjetos con carga positiva pueden verse afectados por presiones ambientales, dando lugar a una tinción incorrecta. Póngase en contacto con su representante de servicio de Roche para obtener más información sobre el uso de este tipo de portaobjetos.
6. Los materiales de origen animal o humano deben manipularse como materiales biopeligrosos y eliminarse con las precauciones adecuadas. En caso de exposición, deberán seguirse las directivas sanitarias de las autoridades responsables.11,12
7. Evite el contacto de los reactivos con los ojos y las membranas mucosas. Si los reactivos entran en contacto con zonas sensibles, lávelas con agua abundante.
8. Evite la contaminación microbiana de los reactivos, dado que podría dar lugar a resultados incorrectos.
9. Para obtener más información sobre el uso de este producto, consulte el Manual del usuario del instrumento BenchMark IHC/ISH y las instrucciones de uso de todos los componentes necesarios que puede encontrar en navifyportal.roche.com.
10. Consultar a las autoridades locales y/o estatales sobre el método de eliminación recomendado.
11. El etiquetado de seguridad de los productos sigue principalmente las directrices del SGA de la UE. Está disponible bajo petición la hoja de datos de seguridad para los usuarios profesionales.
12. Para comunicar la sospecha de incidentes graves relacionados con este dispositivo, póngase en contacto con su representante local de servicio Roche y con las autoridades competentes del Estado o País Miembro de residencia del usuario.
Este producto contiene componentes clasificados como sigue de conformidad con el Reglamento (CE) n.º 1272/2008:
Tabla 1. Información de riesgos
|
Riesgo |
Código |
Declaración |
|
Advertencia
|
H317 |
Puede provocar una reacción alérgica en la piel. |
|
H412 |
Perjudicial para los organismos acuáticos con efectos nocivos duraderos. |
|
|
P261 |
Evite inhalar la niebla o los vapores. |
|
|
P273 |
Evitar su emisión al medio ambiente. |
|
|
P280 |
Llevar guantes de protección. |
|
|
P333 + P313 |
En caso de irritación o erupción cutánea: Consultar a un médico. |
|
|
P362 + P364 |
Quitarse las prendas contaminadas y lavarlas antes de volver a usarlas. |
|
|
P501 |
Eliminar el contenido/el recipiente en una planta de eliminación de residuos aprobada. |
Este producto contiene CAS n.º 55965-84-9, masa reactiva de: 5-cloro-2-metil-2H-isotiazol-3-ona y 2-metil-2H-isotiazol-3-ona (3:1).
MATERIAL SUMINISTRADO:
El anticuerpo VENTANA ROS1 (SP384) contiene reactivo suficiente para 50 pruebas.
Un dispensador de 5 mL de anticuerpo VENTANA ROS1 (SP384) contiene aproximadamente 1 μg de un anticuerpo monoclonal de conejo.
El anticuerpo se diluye en un diluyente Tris-HCl con proteína transportadora, el conservante ProClin 300 al 0.10% y Brij-35 al 0.17%.
La concentración del anticuerpo específico es aproximadamente de 0.2 μg/mL. No se ha observado ninguna reactividad del anticuerpo no específica conocida en este producto.
El anticuerpo VENTANA ROS1 (SP384) es un anticuerpo recombinante monoclonal de conejo producido como sobrenadante de un cultivo celular purificado.
Consulte la hoja de datos del kit de detección VENTANA correspondiente para obtener descripciones detalladas de los siguientes aspectos: Principio del procedimiento, Material y métodos, Recogida y preparación de muestras para análisis, Procedimientos de control de calidad, Resolución de problemas, Interpretación de los resultados y Limitaciones.
MATERIALES NECESARIOS PERO NO SUMINISTRADOS:
No se suministran reactivos de tinción, como kits de detección VENTANA, ni componentes auxiliares, incluyendo portaobjetos de control de tejido negativos y positivos.
Puede que no todos los productos que aparecen en la hoja de datos estén disponibles en todos los lugares. Consulte al representante local de asistencia técnica de Roche.
No se suministran los reactivos y materiales siguientes, pero pueden ser necesarios para la tinción:
1. Tejido de control recomendado
2. Portaobjetos para microscopio con carga positiva
3. Rabbit Monoclonal Negative Control Ig (n.º de cat. 790-4795/06683380001)
4. OptiView DAB IHC Detection Kit (n.º de cat. 760-700/06396500001)
5. EZ Prep Concentrate (10X) (n.º cat. 950-102/05279771001)
6. Reaction Buffer Concentrate (10X) (n.º cat. 950-300/05353955001)
7. LCS (Predilute) (n.º cat. 650-010/05264839001)
8. ULTRA LCS (Predilute) (n.º cat. 650-210/05424534001)
9. Cell Conditioning Solution (CC1) (n.º cat. 950-124/05279801001)
10 ULTRA Cell Conditioning Solution (ULTRA CC1) (n.º cat. 950-224/05424569001)
11. Hematoxylin II (n.º cat. 790-2208/05277965001)
12. Bluing Reagent (n.º de cat. 760-2037/05266769001)
13. Equipo de laboratorio de uso general
14. Instrumento BenchMark IHC/ISH
CONTROL DE REACTIVOS NEGATIVO:
Además de la tinción con el anticuerpo VENTANA ROS1 (SP384), se debe teñir un segundo portaobjetos con Rabbit Monoclonal Negative Control Ig.
CONTROL DE TEJIDO POSITIVO:
La práctica de laboratorio óptima consiste en incluir una sección de control positivo en el mismo portaobjetos que el tejido de la prueba. Esto contribuye a identificar fallos al aplicar los reactivos al portaobjetos. Un tejido con una tinción débil positiva es más adecuado para el control de calidad. El tejido de control puede contener elementos de tinción tanto positiva como negativa y ambos sirven como control positivo y negativo. El tejido de control debe ser una muestra de autopsia reciente, biopsia o cirugía preparada o fijada con la mayor brevedad con un proceso idéntico al de las secciones de prueba.
Los controles de tejido positivos conocidos solo se deben usar para monitorizar el comportamiento correcto de los reactivos y los instrumentos, y no como ayuda para establecer un diagnóstico específico de las muestras de prueba. Si los controles de tejido positivos no muestran una tinción positiva, los resultados de las muestras de la prueba se deben considerar no válidos.
Como ejemplos de tejidos de control positivos de este anticuerpo figuran los tejidos de NSCLC positivos en ROS1 conocidos, los neumocitos alveolares reactivos de tipo II y las estirpes celulares con expresión de fusiones de ROS1 conocidas, como HCC78.
CARACTERÍSTICAS DE RENDIMIENTO:
Rendimiento de análisis:
Se realizaron pruebas de tinción para evaluar la sensibilidad, especificidad y precisión y los resultados se indican a continuación.
Sensibilidad y especificidad:
Tabla 3. La sensibilidad/especificidad del anticuerpo VENTANA ROS1 (SP384) se determinó analizando tejidos normales FFPE
|
Tejido |
N.º de casos positivos/ total |
Tejido |
N.º de casos positivos/ total |
|
Cerebro a |
1/8 |
Glándula suprarrenal |
0/5 |
|
Cerebelo a |
1/4 |
Ovario |
0/5 |
|
Páncreasb |
1/6 |
Estómago e |
1/5 |
|
Ganglio linfático |
0/5 |
Intestino delgado f |
2/5 |
|
Glándula pituitaria |
0/6 |
Colon |
0/6 |
|
Testículos c |
2/6 |
Hígado |
0/6 |
|
Glándula tiroidea d |
3/6 |
Glándula salival |
0/6 |
|
Mama |
0/3 |
Riñón g |
5/5 |
|
Bazo |
0/5 |
Próstata h |
2/5 |
|
Amígdala |
0/5 |
Endometrio |
0/3 |
|
Glándula timo |
0/5 |
Cuello del útero |
0/3 |
|
Glándula paratiroidea |
0/3 |
Músculo esquelético |
0/4 |
|
Vejiga |
0/4 |
Piel i |
1/12 |
|
Mieloide (médula ósea) |
0/5 |
Nervio |
0/4 |
|
Pulmón |
0/16 |
Mesotelio j |
3/4 |
|
Corazón |
1/3 |
Ojo |
0/1 |
|
Esófago |
0/6 |
Laringe |
0/1 |
a Tinción citoplasmática neurológica; b Tinción citoplasmática de células acinosas/de islotes; c Tinción estromal;
d Tinción coloidal; e Tinción focal de secretoras luminales; f Tinción de linfocitos en el estroma; g Tinción de membrana apical; hTinción citoplasmática epitelial y de membrana apical;
i Tinción citoplasmática epidérmica y de linfocitos; j Tinción de neumocitos de tipo II en un caso
Tabla 4. La sensibilidad/especificidad del anticuerpo VENTANA ROS1 (SP384) se determinó analizando una variedad de tejidos neoplásicos FFPE
|
Patología |
N.º de casos positivos/ total |
|---|---|
|
Glioblastoma (cerebro) |
0/2 |
|
Meningioma (cerebro) |
0/1 |
|
Oligodendroglioma (cerebro) |
0/1 |
|
Carcinoma seroso (ovario) a |
1/2 |
|
Neoplasia neuroendocrina (páncreas) |
0/1 |
|
Adenocarcinoma ductal (páncreas) |
0/1 |
|
Seminoma (testículos) |
0/1 |
|
Carcinoma embrionario (testículos) |
0/1 |
|
Carcinoma medular (tiroides) |
0/1 |
|
Carcinoma papilar (tiroides) |
0/1 |
|
Carcinoma intraductal (mama) b |
1/1 |
|
Carcinoma ductal invasivo (mama) |
0/2 |
|
Linfoma difuso de linfocitos B (bazo) |
0/1 |
|
Carcinoma de células pequeñas (pulmón) a |
1/1 |
|
Carcinoma de células escamosas (pulmón) |
3/27 |
|
Adenocarcinoma (pulmón) |
4/15 |
|
Adenocarcinoma papilar (pulmón) |
1/2 |
|
Adenocarcinoma mucinoso (pulmón) |
0/2 |
|
Carcinoma adenoescamoso (pulmón) |
0/1 |
|
Carcinoma de células escamosas (esófago) |
0/1 |
|
Adenocarcinoma (esófago) |
0/1 |
|
Adenocarcinoma mucinoso (estómago) |
0/1 |
|
Adenocarcinoma (gastrointestinal) |
0/1 |
|
Tumor estromal gastrointestinal (GIST) (intestino delgado) |
0/1 |
|
Adenocarcinoma (colon) |
0/1 |
|
Tumor estromal gastrointestinal (GIST) (colon) |
0/1 |
|
Adenocarcinoma (recto) |
0/1 |
|
Tumor estromal gastrointestinal (GIST) (recto) |
0/1 |
|
Carcinoma hepatocelular (hígado) |
0/1 |
|
Hepatoblastoma (hígado) |
0/1 |
|
Colangiocarcinoma intrahepático (hígado) |
12/89 |
|
Carcinoma de células claras (riñón) |
0/1 |
|
Adenocarcinoma (próstata) |
0/2 |
|
Leiomiosarcoma (útero) |
0/1 |
|
Adenocarcinoma (útero) |
0/1 |
|
Carcinoma de células claras (útero) |
0/1 |
|
Carcinoma de células escamosas (cuello uterino) |
0/1 |
|
Carcinoma invasivo de células escamosas (cuello uterino) |
0/1 |
|
Rabdomiosarcoma embrionario (músculo estriado) |
0/1 |
|
Melanoma (recto) |
0/1 |
|
Carcinoma de células basales (piel) |
0/1 |
|
Carcinoma de células escamosas (piel) |
0/1 |
|
Melanoma (piel) |
2/40 |
|
Neuroblastoma (retroperitoneo) |
0/1 |
|
Mesotelioma (peritoneo) a |
1/1 |
|
Linfoma de linfocitos B; sin especificar (ganglio linfático) |
0/2 |
|
Linfoma de Hodgkin (ganglio linfático) c |
1/1 |
|
Carcinoma urotelial de alto grado (vejiga) |
0/1 |
|
Leiomiosarcoma (vejiga) |
0/1 |
|
Rabdomiosarcoma de células fusiformes (peritoneo) |
0/1 |
a Tinción de linfocitos; b Tinción citoplasmática; c Tinción de células de Hodgkin
Precisión:
Se llevaron a cabo estudios de precisión con el anticuerpo VENTANA ROS1 (SP384) para demostrar:
• La precisión entre lotes del anticuerpo.
• La precisión dentro de la sesión y entre días en un instrumento BenchMark ULTRA.
• La precisión entre instrumentos en los instrumentos BenchMark GX, BenchMark XT y BenchMark ULTRA.
• La precisión entre plataformas entre los instrumentos BenchMark GX, BenchMark XT y BenchMark ULTRA.
Todos los estudios cumplieron los criterios de aceptación.
Se demostró la precisión del instrumento BenchMark ULTRA PLUS mediante ensayos representativos. Entre los estudios que se llevaron a cabo figuraban la repetibilidad entre sesiones y la precisión intermedia entre días y entre análisis. Todos los estudios cumplieron los criterios de aceptación.
Datos comparativos de IHC y FISH:
En la Tabla 5, se muestran los resultados de un estudio de comparación analítica de casos que se habían teñido con el anticuerpo VENTANA ROS1 (SP384) para IHC y que también se sometieron a análisis mediante hibridación in situ con fluorescencia (FISH). Los datos de la comparación analítica del anticuerpo VENTANA ROS1 (SP384) frente a FISH se proporcionan únicamente con fines informativos. Todos los ensayos y los criterios de evaluación deben validarse por parte del laboratorio clínico teniendo en cuenta su propio entorno, factores previos al análisis y de otro tipo que son exclusivos de las condiciones del laboratorio.
RENDIMIENTO CLÍNICO:
Los datos de rendimiento clínico pertinentes para el uso previsto del anticuerpo VENTANA ROS1 (SP384) se evaluaron mediante revisión sistemática de la documentación oportuna. Los datos obtenidos respaldan la utilización del dispositivo de acuerdo con su uso previsto.
Tabla 5. Datos de la comparación analítica del anticuerpo VENTANA ROS1 (SP384): IHC frente a FISH
|
IHC |
Resultado FISH |
Porcentaje de concordancia % a (n/N) |
||
|
Positiva |
Negativa |
Total |
||
|
Tinción ≥ 2+ en citoplasma en cualquiera de las células tumorales |
45 |
18 |
63 |
PPA: 97.8 (45/46) (88.7, 99.6) |
|
Tinción ≥ 2+ en citoplasma y no en cualquiera de las células tumorales |
1 |
58 |
59 |
NPA: 76.3 (58/76) (65.6, 84.5) |
|
Total |
46 |
76 |
122 |
OPA: 84.4 (103/122) (77.0, 89.8) |
|
Tinción ≥ 2+ en citoplasma en > 25% del total de las células tumorales |
45 |
11 |
56 |
PPA: 97.8 (45/46) (88.7, 99.6) |
|
Tinción ≥ 2+ en citoplasma en ≤ 25% del total de las células tumorales |
1 |
65 |
66 |
NPA: 85.5 (65/76) (75.9, 91.7) |
|
Total |
46 |
76 |
122 |
OPA: 90.2 (110/122) (83.6, 94.3) |
|
Tinción ≥ 2+ en citoplasma en > 30% del total de las células tumorales |
45 |
8 |
53 |
PPA: 97.8 (45/46) (88.7, 99.6) |
|
Tinción ≥ 2+ en citoplasma en ≤ 30% del total de las células tumorales |
1 |
68 |
69 |
NPA: 89.5 (68/76) (80.6, 94.6) |
|
Total |
46 |
76 |
122 |
OPA: 92.6 (113/122) (86.6, 96.1) |
|
Tinción ≥ 2+ en citoplasma en > 50% del total de las células tumorales |
42 |
5 |
47 |
PPA: 91.3 (42/46) (79.7, 96.6) |
|
Tinción ≥ 2+ en citoplasma en ≤ 50% del total de las células tumorales |
4 |
71 |
75 |
NPA: 93.4 (71/76) (85.5, 97.2) |
|
Total |
46 |
76 |
122 |
OPA: 92.6 (113/122) (86.6, 96.1) |
a PPA = porcentaje de concordancia positiva; NPA = porcentaje de concordancia negativa; OPA = porcentaje de concordancia global;
b Intervalo de confianza bilateral del 95% mediante el método de puntuación de Wilson; CI = Intervalo de confianza
USO PREVISTO:
VENTANA ROS1 (SP384) RABBIT MONOCLONAL PRIMARY ANTIBODY está destinado a su uso en laboratorio para la detección cualitativa inmunohistoquímica de la proteína ROS1 mediante microscopía óptica en secciones de tejido fijado con formol y embebido en parafina teñido con un instrumento BenchMark IHC/ISH.
La interpretación de este producto debe correr a cargo de un anatomopatólogo cualificado junto con un examen histológico, la información clínica pertinente y los controles adecuados.
Este anticuerpo está destinado para uso diagnóstico in vitro (IVD).
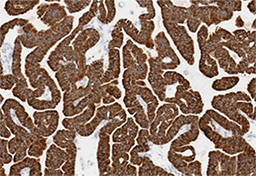
Figura 1. Tinción con VENTANA ROS1 (SP384) RABBIT MONOCLONAL PRIMARY ANTIBODY de tejido de cáncer de pulmón de células no pequeñas (NSCLC).
LIMITACIONES ESPECÍFICAS:
Este anticuerpo se ha optimizado para un tiempo de incubación de 16 minutos en el instrumento BenchMark IHC/ISH junto con el OptiView DAB IHC Detection Kit y con los parámetros indicados en la Tabla 2, pero el usuario debe validar los resultados obtenidos con este reactivo.
Es posible que no todos los ensayos estén registrados en todos los instrumentos. Póngase en contacto con el representante local de servicio Roche para obtener más información.
PREPARACIÓN DE MUESTRAS:
Los tejidos FFPE que se procesan de forma habitual resultan adecuados para su uso con este anticuerpo primario cuando se utilizan con los kits de detección de VENTANA y los instrumentos BenchMark IHC/ISH. El fijador de tejido recomendado es formol tamponado neutro al 10%.10 Las secciones de tejido se deben cortar con un grosor aproximado de 4 μm y colocarse en portaobjetos cargados positivamente. Los portaobjetos deben teñirse inmediatamente, dado que la antigenicidad de las secciones de los cortes de tejido puede disminuir con el tiempo. Solicite a su representante de servicio de Roche una copia de «Recommended Slide Storage and Handling» para obtener más información al respecto.
Se recomienda analizar controles positivos y negativos a la vez que las muestras desconocidas.
PRINCIPIO DEL PROCEDIMIENTO:
El anticuerpo VENTANA ROS1 (SP384) se une a la proteína ROS1 en muestras de tejido fijado con formol y embebido en parafina (FFPE). El anticuerpo específico se puede localizar mediante un anticuerpo secundario haptenado, seguido por un conjugado multímero de peroxidasa de rábano (HRP) anti-hapteno (OptiView DAB IHC Detection Kit, n.º de cat. 760-700/06396500001). El complejo específico de anticuerpo-enzima se puede visualizar a través del precipitado del producto de reacción enzimático. Consulte la hoja de datos correspondiente para obtener más información.
PROCEDIMIENTO DE TINCIÓN:
Los anticuerpos primarios VENTANA se han desarrollado para su uso en los instrumentos BenchMark IHC/ISH junto con los kits de detección de VENTANA y sus accesorios.
Consulte la Tabla 2 para ver los protocolos de tinción recomendados.
Este anticuerpo se ha optimizado para tiempos de incubación específicos, pero el usuario debe validar los resultados obtenidos con este reactivo.
Los parámetros de los procedimientos automatizados se pueden visualizar, imprimir y editar según el procedimiento descrito en el Manual del usuario del instrumento. Consulte la hoja de datos del kit de detección VENTANA correspondiente para obtener más detalles sobre los procedimientos de tinción de inmunohistoquímica.
Tabla 2. Protocolo de tinción recomendado para el anticuerpo VENTANA ROS1 (SP384) con OptiView DAB IHC Detection Kit en instrumentos BenchMark IHC/ISH. Utilizar el procedimiento de tinción de IHC para OptiView DAB
|
Tipo de procedimiento |
Método |
||
|
GX |
XT |
ULTRA o ULTRA PLUSa |
|
|
Desparafinado |
Seleccionado |
Seleccionado |
Seleccionado |
|
Cell Conditioning (desenmascaramiento del antígeno) |
CC1, 64 minutos, |
CC1, 64 minutos, |
ULTRA CC1, 64 minutos, 100 °C |
|
Inhibidor preprimario de peroxidasa |
Seleccionado |
Seleccionado |
Seleccionado |
|
Anticuerpo (Primario) |
16 minutos, 37 °C |
16 minutos, 37 °C |
16 minutos, 36 °C |
|
OptiView HQ Linker |
8 minutos (predeterminado) |
||
|
OptiView HRP Multimer |
8 minutos (predeterminado) |
||
|
Contratinción |
Hematoxylin II, 4 minutos |
||
|
Post-contratinción |
Bluing, 4 minutos |
||
a Se demostró la concordancia entre los instrumentos BenchMark ULTRA y BenchMark ULTRA PLUS mediante ensayos representativos.
Debido a variaciones en la fijación y el procesamiento del tejido, así como a las condiciones generales de los instrumentos y del entorno del laboratorio, puede que sea necesario aumentar o disminuir el tiempo de incubación del anticuerpo primario, el acondicionamiento celular o tratamiento previo de la proteasa en función de las muestras particulares, de la detección que se haya utilizado y de las preferencias del profesional encargado de la lectura. Para obtener más información sobre las variables de fijación, consulte «Immunohistochemistry Principles and Advances».13
RESUMEN Y EXPLICACIÓN:
VENTANA ROS1 (SP384) RABBIT MONOCLONAL PRIMARY ANTIBODY (anticuerpo VENTANA ROS1 (SP384)) es un anticuerpo monoclonal de conejo dirigido contra la proteína ROS1, un receptor de tirosina quinasa de la familia de receptores de la insulina.1-5 El gen ROS1 es susceptible a las reorganizaciones cromosómicas.1-5 Estas reorganizaciones cromosómicas dan lugar a la unión de una porción de ROS1, que contiene el dominio quinasa, con uno o varios genes pares conocidos actualmente.1-6 Se ha demostrado que la consecuente sobreexpresión de estas nuevas proteínas ROS1 reorganizadas favorece la oncogénesis en varios tipos de cáncer, entre otros, el cáncer de pulmón de células no pequeñas (NSCLC).1-6 La inmunohistoquímica (IHC) de ROS1 puede detectar las proteínas ROS1 de tipo silvestre y reorganizadas, por lo que la determinación del estado de reorganización genética del gen ROS1 es imposible únicamente con la IHC de ROS1.1-5 Así pues, los tejidos en los que se detecta la expresión de ROS1 mediante IHC deberían caracterizarse más detalladamente a través de un método molecular o citogenético.7,8,9
La detección de la proteína ROS1 mediante IHC con el anticuerpo VENTANA ROS1 (SP384) puede servir de ayuda en la identificación de cáncer de pulmón de células no pequeñas (NSCLC) con expresión de ROS1 para la caracterización más detallada a través de un método molecular o citogenético. El patrón de tinción es principalmente citoplasmático y, excepcionalmente, membranoso y nuclear.
REFERENCIAS:
1. Rossi G, Jocolle G, Conti A, et al. Detection of ROS1 Rearrangement in Non-Small Cell Lung Cancer: Current and Future Perspectives. Lung Cancer (Auckl). 2017;8:45-55.
2. Bubendorf L, Buttner R, Al-Dayel F, et al. Testing for ROS1 in Non-Small Cell Lung Cancer: A Review with Recommendations. Virchows Arch. 2016;469(5):489-503.
3. Gainor JF, Shaw AT. Novel Targets in Non-Small Cell Lung Cancer: ROS1 and RET Fusions. Oncologist. 2013;18(7):865-875.
4. Lin JJ, Shaw AT. Recent Advances in Targeting ROS1 in Lung Cancer. J Thorac Oncol. 2017;12(11):1611-1625.
5. Davies KD, Doebele RC. Molecular Pathways: ROS1 Fusion Proteins in Cancer. Clin Cancer Res. 2013;19(15):4040-4045.
6. Varella-Garcia M, Yoshida A. ROS1 Testing with FISH. IASLC Atlas of ALK and ROS1 Testing in Lung Cancer. Ed. Tsao M, Ed. Hirsch F, Ed. Yatabe Y. 2nd Edition. Aurora, CO, USA. Editorial Rx Press; 2016. 55-61. Print.
7. D. Planchard, S. Popat, K. Kerr, et al. ESMO Clinical Practice Metastatic NSCLC Guidelines for Diagnosis, Treatment and Follow Up. Ann Oncol. 2019.
8. Wu YL, Planchard D, Lu S, et al. Pan-Asian Adapted Clinical Practice Guidelines for the Management of Patients with Metastatic Non-Small-Cell Lung Cancer: A CSCO- ESMO Initiative Endorsed by JSMO, KSMO, MOS, SSO and TOS. Ann Oncol. 2019;30(2):171-210.
9. Lindeman NI, Cagle PT, Aisner DL, et al. Updated Molecular Testing Guideline for the Selection of Lung Cancer Patients for Treatment with Targeted Tyrosine Kinase Inhibitors: Guideline from the College of American Pathologists, the International Association for the Study of Lung Cancer, and the Association for Molecular Pathology. Arch Pathol Lab Med. 2018;142(3):321-346.
10. Carson FL, Cappellano C. Histotechnology; A Self-Instructional Text, 5th edition. American Society for Clinical Pathology Press; 2020, 2022.
11. Occupational Safety and Health Standards: Occupational exposure to hazardous chemicals in laboratories. (29 CFR Part 1910.1450). Fed. Register.
12. Directive 2000/54/EC of the European Parliament and Council of 24 June 2020 on the protection of workers from risks related to exposure to biological agents at work.
13. Roche PC, Hsi ED. Immunohistochemistry-Principles and Advances. Manual of Clinical Laboratory Immunology, 6th edition. In: NR Rose, ed. ASM Press; 2002.
Nota: En este documento se ha usado el punto como separador decimal para marcar el borde entre la parte entera y la parte fraccionaria de los numerales con decimales. No se han usado separadores para las unidades de millar.
El resumen de los aspectos de seguridad y rendimiento se puede ver a continuación: https://ec.europa.eu/tools/eudamed
Símbolos:
Ventana usa los siguientes símbolos y signos además de los indicados en la norma ISO 15223-1 (para USA: consulte elabdoc.roche.com/symbols para obtener más información).
|
GTIN |
Número mundial de artículo comercial |
|
Rx only |
Para USA: Precaución: Las normas nacionales restringen la venta de este dispositivo a médicos autorizados o por orden de estos. |
Propiedad intelectual:
VENTANA, BENCHMARK y OPTIVIEW son marcas comerciales de Roche. Todos los demás nombres de productos y marcas comerciales pertenecen a sus respectivos propietarios.
© 2024 Ventana Medical Systems, Inc.
For USA: Rx only
Información de contacto:
ROCHE DIAGNOSTICS GMBH
Sandhofer Strasse 116
68305 Mannheim Germany
+800 5505 6606