OFEV - Cápsulas
Sustancia(s):
- Lecitina De Soya, Nintedanib
Presentaciones:
- 1 Caja, 30 Cápsulas, 100 mg
- 1 Caja, 30 Cápsulas, 150 Miligramos
- 1 Caja, 60 Cápsulas, 100 Miligramos
- 1 Caja, 60 Cápsulas, 150 Miligramos
FORMA FARMACÉUTICA Y FORMULACIÓN:
Cada CÁPSULA de 100 mg de OFEV® contiene:
Nintedanib 100 mg (como esilato)
Excipiente cbp 1 cápsula
Excipiente con efecto conocido:
Cada CÁPSULA de 100 mg contiene:
Lecitina de soya 1.2 mg
Cada CÁPSULA de 150 mg de OFEV® contiene:
Nintedanib (como esilato) 150 mg Excipiente cbp 1 cápsula
Excipiente con efecto conocido:
Cada CÁPSULA de 150 mg contiene:
Lecitina de soya 1.8 mg
INDICACIONES TERAPÉUTICAS: OFEV® está indicado en adultos para tratar la fibrosis pulmonar idiopática (FPI).
OFEV® también está indicado en adultos para el tratamiento de otras enfermedades pulmonares intersticiales (ILD) crónicas fibrosantes con fenotipo progresivo.
OFEV® está indicado en adultos para tratar la enfermedad pulmonar intersticial asociada a esclerosis sistémica (SSc-ILD).
FARMACOCINÉTICA Y FARMACODINAMIA:
Grupo farmacoterapéutico: Agentes antineoplásicos, inhibidores de la proteína cinasa.
Código ATC: L01EX09.
Mecanismo de acción: Nintedanib es un inhibidor de molécula pequeña de la tirosina cinasa, incluidos los receptores del factor de crecimiento derivados de plaquetas (PDGFR) α y β, los receptores del factor de crecimiento de fibroblastos (FGFR) 1-3 y los receptores del factor de crecimiento del endotelio vascular (VEGFR) 1-3. Además, nintedanib inhibe las cinasas Lck (proteína tirosina cinasa específica de los linfocitos), Lyn (proteína tirosina cinasa Lyn), Src (proteína tirosina cinasa proto-oncogénica Src) y CSF1R (receptor del factor estimulante de colonias de tipo 1). Nintedanib se une de forma competitiva al sitio de unión de adenosina trifosfato (ATP) de estas cinasas y bloquea las cascadas de señalización intracelular que se ha demostrado que participan en la patogenia de la remodelación del tejido fibrótico en las enfermedades pulmonares intersticiales.
Efectos farmacodinámicos: En los estudios in vitro con células humanas, se ha demostrado que nintedanib inhibe los procesos que se supone que participan en el inicio de la patogenia fibrótica, la liberación de mediadores profibróticos de las células monocíticas de sangre periférica y la polarización de los macrófagos a macrófagos activados de forma alternativa. Se ha demostrado que nintedanib inhibe los procesos fundamentales en la fibrosis de los órganos, la proliferación y la migración de los fibroblastos y la transformación al fenotipo de miofibroblasto activo y la secreción de matriz extracelular. En los estudios realizados en animales con múltiples modelos de FPI, SSc/SSc-ILD, ILDI asociada a artritis reumatoide (AR) y otras fibrosis de órganos, nintedanib ha demostrado efectos antiinflamatorios y antifibróticos en el pulmón, la piel, el corazón, el riñón y el hígado. Nintedanib también ejerció actividad vascular. Redujo la apoptosis de las células endoteliales microvasculares dérmicas y atenuó la remodelación vascular pulmonar reduciendo la proliferación de las células de músculo liso vascular, el grosor de las paredes de los vasos pulmonares y el porcentaje de vasos pulmonares ocluidos.
Eficacia clínica y seguridad:
Fibrosis pulmonar idiopática (FPI): La eficacia clínica de nintedanib se ha estudiado en pacientes con FPI en dos ensayos con diseño idéntico fase III, aleatorizados, doble ciego y controlados con placebo (INPULSIS-1 [1199.32] e INPULSIS-2 [1199.34]). Los pacientes con una CVF basal prevista inferior al 50% o un factor de transferencia de monóxido de carbono (DLCO, corregido para la hemoglobina) prevista inferior al 30% en el nivel basal se excluyeron de los ensayos. Los pacientes se aleatorizaron en una proporción de 3:2 entre el tratamiento con OFEV® 150 mg y el tratamiento con placebo dos veces al día durante 52 semanas.
La variable principal fue la pérdida anual de la capacidad vital forzada (CVF). Los criterios de valoración secundarios principales fueron el cambio respecto al valor basal en la puntuación obtenida a las 52 semanas en el Saint George’s Respiratory Questionnaire (CRSG) y el tiempo hasta que se produjo la primera exacerbación aguda de la FPI.
Pérdida anual de la CVF: La pérdida anual de la CVF (en ml) se redujo significativamente en los pacientes que recibieron nintedanib en comparación con los pacientes que recibieron placebo. El efecto del tratamiento fue coincidente en ambos ensayos. Ver los resultados del estudio individual y conjunto en la Tabla 1.
Tabla 1. Pérdida anual de la CVF (ml) en los ensayos INPULSIS-1, INPULSIS-2 y sus datos conjuntos: grupo tratado
|
INPULSIS-1 |
INPULSIS-2 |
INPULSIS-1 e INPULSIS-2 combinados |
||||
|
Placebo |
OFEV® 150 mg dos veces al día |
Placebo |
OFEV® 150 mg dos veces al día |
Placebo |
OFEV® 150 mg dos veces al día |
|
|
Número de pacientes analizados |
204 |
309 |
219 |
329 |
423 |
638 |
|
Tasa1 (SE) de disminución a lo largo de 52 semanas |
-239.9 (18.71) |
-114.7 (15.33) |
-207.3 (19.31) |
-113.6 (15.73) |
-223.5 (13.45) |
-113.6 (10.98) |
|
Comparación frente al placebo |
||||||
|
Diferencias1 |
125.3 |
93.7 |
109.9 |
|||
|
95% de IC |
(77.7, 172.8) |
(44.8, 142.7) |
(75.9, 144.0) |
|||
|
Valor p |
< 0.0001 |
0.0002 |
< 0.0001 |
|||
1 Calculado basándose en un modelo de regresión de coeficientes aleatorios.
IC: intervalo de confianza.
En un análisis de sensibilidad que supuso que, en el caso de los pacientes en los que faltan datos en la semana 52, la pérdida de la CVF después del último valor observado sería la misma que en todos los pacientes tratados con placebo, la diferencia ajustada en la pérdida anual entre nintedanib y placebo fue de 113.9 ml/año (95% de IC: 69.2, 158.5) en el ensayo INPULSIS-1 y de 83.3 ml/año (95% de IC: 37.6, 129.0) en el ensayo INPULSIS-2.
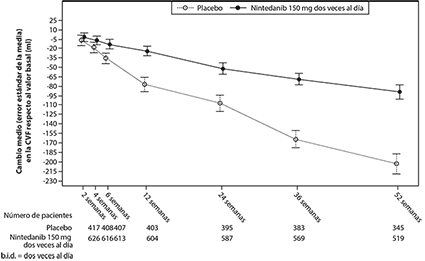
Ver en la figura 1 la evolución del cambio respecto al valor basal a lo largo del tiempo en los dos grupos de tratamiento basándose en el análisis conjunto de los estudios INPULSIS-1 e INPULSIS-2.
Figura 1. Cambio medio (error estándar de la media [SEM]) respecto al valor basal (ml) observado en la CVF a lo largo del tiempo; estudios INPULSIS-1 e INPULSIS-2 conjuntos
Análisis de los pacientes que responden en términos de CVF: En ambos ensayos INPULSIS, la proporción de pacientes que respondieron en términos de CVF, definidos como los pacientes con una pérdida absoluta en la CVF prevista inferior al 5% (un umbral indicador del aumento del riesgo de mortalidad en la FPI), fue significativamente más alta en el grupo tratado con nintedanib que en el grupo tratado con placebo. En los análisis que utilizaron un umbral conservador del 10% se observaron resultados similares. Ver los resultados del estudio individual y conjunto en la Tabla 2.
Tabla 2. Proporción de pacientes que respondieron en términos de CVF a las 52 semanas en los estudios INPULSIS-1, INPULSIS-2 y sus datos conjuntos: grupo tratado
|
INPULSIS-1 |
INPULSIS-2 |
INPULSIS-1 e INPULSIS-2 combinados |
||||
|---|---|---|---|---|---|---|
|
Placebo |
OFEV® |
Placebo |
OFEV® |
Placebo |
OFEV® |
|
|
Número de pacientes analizados |
204 |
309 |
219 |
329 |
423 |
638 |
|
Umbral del 5% |
||||||
|
Número (%) de respondedores por CVF1 |
78 (38.2) |
163 (52.8) |
86 (39.3) |
175 (53.2) |
164 (38.8) |
338 (53.0) |
|
Comparación frente al placebo |
||||||
|
Cociente de probabilidades (OR) |
1.85 |
1.79 |
1.84 |
|||
|
IC 95% |
(1.28, 2.66) |
(1.26, 2.55) |
(1.43, 2.36) |
|||
|
Valor p2 |
0.0010 |
0.0011 |
< 0.0001 |
|||
|
Umbral del 10% |
||||||
|
Número (%) de respondedores por CVF1 |
116 (56.9) |
218 (70.6) |
140 (63.9) |
229 (69.6) |
256 (60.5) |
447 (70.1) |
|
Comparación frente al placebo |
||||||
|
Cociente de probabilidades (OR) |
1.91 |
1.29 |
1.58 |
|||
|
IC 95% |
(1.32, 2.79) |
(0.89, 1.86) |
(1.21, 2.05) |
|||
|
Valor p2 |
0.0007 |
0.1833 |
0.0007 |
|||
1 Los pacientes que responden son aquellos que no presentan una pérdida absoluta superior al 5% o superior al 10% en el % de CVF previsto, dependiendo del umbral y con una evaluación de la CVF a las 52 semanas.
2 Basándose en una regresión logística.
Tiempo hasta la progresión (≥ 10% de pérdida absoluta de la CVF prevista o muerte): Desde el punto de vista estadístico, en ambos ensayos INPULSIS, el riesgo de progresión fue significativamente menor en los pacientes tratados con nintedanib que en los tratados con placebo. En el análisis conjunto, el cociente de riesgos (hazard ratio) fue de 0.60, lo que indica una reducción de un 40% del riesgo de progresión en los pacientes tratados con nintedanib en comparación con los tratados con placebo. Ver Tabla 3.
Tabla 3. Frecuencia de pacientes con ≥ 10% de pérdida absoluta de la CVF prevista o muerte en el transcurso de 52 semanas y tiempo hasta la progresión en los ensayos INPULSIS-1, INPULSIS-2 y sus datos conjuntos: grupo tratado
|
INPULSIS-1 |
INPULSIS-2 |
INPULSIS-1 e INPULSIS-2 combinados |
||||
|
Placebo |
OFEV® |
Placebo |
OFEV® |
Placebo |
OFEV® |
|
|
Número de pacientes en riesgo |
204 |
309 |
219 |
329 |
423 |
638 |
|
Pacientes con eventos, N (%) |
83 (40.7) |
75 (24.3) |
92 (42.0) |
98 (29.8) |
175 (41.4) |
173 (27.1) |
|
Comparación frente al placebo1 |
||||||
|
Valor p2 |
0.0001 |
0.0054 |
< 0.0001 |
|||
|
Razón de riesgos instantáneos3 |
0.53 |
0.67 |
0.60 |
|||
|
IC 95% |
(0.39, 0.72) |
(0.51, 0.89) |
(0.49, 0.74) |
|||
1 Basándose en los datos recopilados durante un máximo de 372 días (52 semanas + 7 días de margen).
2 Basándose en una prueba de orden logarítmico.
3 Basándose en un modelo de regresión de Cox.
Cambio respecto al valor basal en la puntuación total del CRSG en la semana 52: En el análisis conjunto de los ensayos INPULSIS, el valor basal de la puntuación del CRSG fue de 39.51 en el grupo tratado con nintedanib y de 39.58 en el grupo tratado con placebo. El cambio medio calculado desde el valor basal hasta la semana 52 en la puntuación total del CRSG fue menor en el grupo tratado con nintedanib (3.53) que en el grupo tratado con placebo (4.96), con una diferencia entre los grupos de tratamiento de -1.43 (95% de IC: -3.09, 0.23; p = 0.0923). En conjunto, el efecto de nintedanib sobre la calidad de vida relacionada con la salud medida por la puntuación total del CRSG es moderado, lo que indica que empeora menos la situación que el placebo.
Tiempo hasta la primera exacerbación aguda de la FPI: En el análisis conjunto de los ensayos INPULSIS, los pacientes que recibieron nintedanib presentaron un riesgo de una primera exacerbación aguda numéricamente menor que los que fueron tratados con placebo. Ver los resultados del estudio individual y conjunto en la Tabla 4.
Tabla 4. Frecuencia de pacientes con exacerbaciones agudas en el transcurso de 52 semanas y análisis del tiempo hasta la primera exacerbación basándose en los episodios descritos por el investigador en los ensayos INPULSIS-1, INPULSIS-2 y sus datos conjuntos: grupo tratado
|
INPULSIS-1 |
INPULSIS-2 |
INPULSIS-1 e INPULSIS-2 conjuntos |
|||||
|---|---|---|---|---|---|---|---|
|
Placebo |
OFEV® |
Placebo |
OFEV® |
Placebo |
OFEV® |
||
|
Número de pacientes en riesgo |
204 |
309 |
219 |
329 |
423 |
638 |
|
|
Pacientes con eventos, N (%) |
11 (5.4) |
19 (6.1) |
21 (9.6) |
12 (3.6) |
32 (7.6) |
31 (4.9) |
|
|
Comparación frente al placebo1 |
|||||||
|
Valor p2 |
0.6728 |
0.0050 |
0.0823 |
||||
|
Cociente de riesgos instantáneos3 |
1.15 |
0.38 |
0.64 |
||||
|
IC 95% |
(0.54, 2.42) |
(0.19, 0.77) |
(0.39, 1.05) |
||||
1 Basándose en los datos recopilados durante un máximo de 372 días (52 semanas + 7 días de margen).
2 Basándose en una prueba de orden logarítmico.
3 Basándose en un modelo de regresión de Cox.
En un análisis preespecificado de sensibilidad, la frecuencia de pacientes con al menos una exacerbación adjudicada en el transcurso de 52 semanas fue inferior en el grupo tratado con nintedanib (1.9% de los pacientes) que en el grupo tratado con placebo (5.7% de los pacientes). El análisis del tiempo transcurrido hasta los episodios de exacerbación adjudicados que utilizó los datos conjuntos obtuvo un cociente de riesgos (hazard ratio) de 0.32 (95% de IC: 0.16, 0.65; p = 0.0010).
Análisis de la supervivencia: En el análisis conjunto preespecificado de los datos de supervivencia de los ensayos INPULSIS, la mortalidad global en el transcurso de 52 semanas fue inferior en el grupo tratado con nintedanib (5.5%) que en el grupo tratado con placebo (7.8%). El análisis del tiempo transcurrido hasta la muerte dio lugar a un cociente de riesgos (hazard ratio) de 0.70 (95% de IC: 0.43, 1.12; p = 0.1399).
Los resultados de todos los criterios de valoración de supervivencia (tales como la mortalidad durante el tratamiento o la mortalidad respiratoria) mostraron una diferencia numérica homogénea en favor de nintedanib.(ver Tabla 5).
Tabla 5. Mortalidad por cualquier causa en el transcurso de 52 semanas en los ensayos INPULSIS-1, INPULSIS-2 y sus datos conjuntos: grupo tratado
|
INPULSIS-1 |
INPULSIS-2 |
INPULSIS-1 e INPULSIS-2 Combinados |
||||
|
Placebo |
OFEV® |
Placebo |
OFEV® |
Placebo |
OFEV® |
|
|
Número de pacientes en riesgo |
204 |
309 |
219 |
329 |
423 |
638 |
|
Pacientes con eventos, N (%) |
13 (6.4) |
13 (4.2) |
20 (9.1) |
22 (6.7) |
33 (7.8) |
35 (5.5) |
|
Comparación frente al placebo1 |
||||||
|
Valor p2 |
0.2880 |
0.2995 |
0.1399 |
|||
|
Cociente de riesgos (HR)3 |
0.63 |
0.74 |
0.70 |
|||
|
IC 95% |
(0.29, 1.36) |
(0.40, 1.35) |
(0.43, 1.12) |
|||
1 Basándose en los datos recopilados durante un máximo de 372 días (52 semanas + 7 días de margen).
2 Basándose en una prueba de orden logarítmico.
3 Basándose en un modelo de regresión de Cox.
Evidencia complementaria de los resultados del estudio de fase II (1199.30) con OFEV® 150 mg dos veces al día:
El estudio aleatorizado, doble ciego, comparativo con placebo, de fase II, para establecer la dosis, en el que se incluyó un grupo de dosis de OFEV® de 150 mg dos veces al día aportó evidencia adicional de la eficacia [84].
El criterio de valoración primario, la tasa de disminución de la CVF a lo largo de 52 semanas en el grupo de OFEV® (-0.060 litro/año, N = 84) fue más bajo que en el grupo del placebo (-0.190 litro/año, N = 83). La diferencia estimada entre los grupos de tratamiento fue 0.131 litro/año (IC del 95%: 0.027; 0.235). Esta diferencia entre los grupos de tratamiento alcanzó la significancia estadística nominal (p = 0.0136).
La media estimada del cambio respecto del nivel inicial en la puntuación total del SGRQ a las 52 semanas fue 5.46 para el placebo, lo que indica un empeoramiento de la calidad de vida relacionada con la salud y de -0.66 para OFEV®, lo cual indica una calidad de vida relacionada con la salud estable. La diferencia media estimada para OFEV® en comparación con el placebo fue -6.12 (IC del 95%: -10.57, -1.67; p = 0.0071).
La cantidad de pacientes con exacerbaciones agudas de la FPI a lo largo de 52 semanas fue más baja en el grupo de OFEV® (2.3%, N = 86) en comparación con el placebo (13.8%, N = 87). El cociente de riesgos (HR) estimado de OFEV® frente al placebo fue 0.16 (IC del 95%: 0.04, 0.71; p = 0.0054).
Tratamiento a largo plazo con OFEV® en pacientes con FPI (INPULSIS-ON): En un estudio de extensión abierto de OFEV® se incluyó a 734 pacientes con FPI. Los pacientes que completaron el periodo de tratamiento de 52 semanas en un ensayo INPULSIS recibieron tratamiento abierto con OFEV® en el ensayo de extensión INPULSIS-ON. La mediana del tiempo de exposición en los pacientes tratados con OFEV® en los ensayos INPULSIS e INPULSIS-ON fue de 44.7 meses (intervalo 11.9-68.3). Entre los criterios de valoración exploratorios de la eficacia se encuentra la tasa anual de pérdida de la CVF durante 192 semanas, que fue de -135.1 (5.8) ml/año en todos los pacientes tratados y que fue consistente con la tasa anual de pérdida de la CVF en los pacientes tratados con OFEV® en los ensayos de fase III INPULSIS (-113.6 ml al año). El perfil de acontecimientos adversos de OFEV® en el ensayo INPULSIS-ON fue consistente con el observado en los ensayos de fase III INPULSIS.
Pacientes con FPI con deterioro de la función pulmonar avanzado (INSTAGE): INSTAGE fue un ensayo clínico prospectivo, doble ciego, aleatorizado, multicéntrico, multinacional y de grupos paralelos en pacientes con FPI y afectación avanzada de la función pulmonar (DLCO prevista ≤ 35%) durante 24 semanas. Fueron tratados con OFEV® en monoterapia 136 pacientes. El resultado de la variable principal mostró una reducción en la puntuación total del cuestionario respiratorio de St George (SGRQ) de -0.77 unidades en la semana 12, basada en el cambio medio ajustado respecto al valor basal. Una comparación post hoc demostró que la disminución de la CVF en estos pacientes fue consistente con la disminución de la CVF en los pacientes con enfermedad menos avanzada y tratados con OFEV® en los ensayos INPULSIS de fase III.
El perfil de seguridad y tolerabilidad de OFEV® en los pacientes con FPI y afectación avanzada de la función pulmonar fue consistente con el observado en los ensayos INPULSIS de fase III.
Datos adicionales del estudio clínico de fase IV INJOURNEY con OFEV® 150 mg dos veces al día y pirfenidona como tratamiento complementario: Se ha investigado el tratamiento conjunto con nintedanib y pirfenidona en un ensayo exploratorio, abierto, aleatorizado de nintedanib 150 mg dos veces al día con pirfenidona como tratamiento complementario (ajustada a 801 mg tres veces al día) en comparación con nintedanib 150 mg dos veces al día en monoterapia en 105 pacientes aleatorizados durante 12 semanas. La variable principal fue el porcentaje de pacientes con reacciones adversas gastrointestinales desde el inicio del estudio y hasta la semana 12. Las reacciones adversas gastrointestinales fueron frecuentes y en línea con el perfil de seguridad establecido de cada componente. Las reacciones adversas más frecuentes fueron diarrea, náuseas y vómitos, notificadas en pacientes tratados con pirfenidona añadida a nintedanib frente a nintedanib en monoterapia, respectivamente.
La media (EE) de los cambios absolutos de la CVF con respecto al valor basal en la semana 12 fue de -13.3 (17.4) ml en los pacientes tratados con nintedanib con pirfenidona como tratamiento complementario (n = 48) en comparación con -40.9 (31.4) ml en los pacientes tratados con nintedanib en monoterapia (n = 44).
Otras enfermedades pulmonares intersticiales (ILD) crónicas fibrosantes con fenotipo progresivo: La eficacia clínica de OFEV® se ha estudiado en pacientes con otras ILD fibrosantes crónicas con un fenotipo progresivo en un ensayo de fase III, aleatorizado, doble ciego y controlado con placebo (INBUILD). Se excluyó a pacientes con FPI. Se seleccionó a pacientes con un diagnóstico clínico de ILD fibrosante crónica si presentaban fibrosis relevante (> 10% de características fibróticas) en la TCAR y signos clínicos de progresión (definida como pérdida de la CVF ≥ 10%, pérdida de la CVF ≥ 5% y < 10% junto con un empeoramiento de los síntomas o de los estudios de imagen torácica, o empeoramiento de los síntomas de los estudios de imagen torácica, en los 24 meses previos a la selección). Los pacientes tenían que tener una CVF igual o superior al 45% del valor previsto y una DLCO de entre el 30% y menos del 80% del valor previsto. Los pacientes tenían que haber experimentado progresión a pesar del tratamiento considerado apropiado en la práctica clínica para la ILD relevante del paciente.
Se aleatorizó a un total de 663 pacientes en una relación de 1:1 para recibir OFEV® 150 mg dos veces al día o un placebo equivalente durante al menos 52 semanas. La mediana de la exposición a OFEV® durante todo el ensayo fue de 17.4 meses y la media de la exposición a OFEV® durante todo el ensayo fue de 15.6 meses. La aleatorización se estratificó en función del patrón fibrótico observado en la TCAR valorado por evaluadores centrales. Se aleatorizó a 412 pacientes con un patrón fibrótico de tipo neumonía intersticial usual (NIU) en la TCAR y a 251 pacientes con otros patrones fibróticos en la TCAR. Se definieron dos poblaciones coprincipales para los análisis de este ensayo: todos los pacientes (la población global) y los pacientes con un patrón fibrótico de tipo NIU en la TCAR. Los pacientes con otros patrones fibróticos en la TCAR representaban la población “complementaria”. El criterio de valoración principal fue la tasa anual de pérdida de la capacidad vital forzada (CVF) (en ml) en el transcurso de 52 semanas. Los criterios de valoración secundarios principales fueron el cambio absoluto respecto al valor basal en la puntuación total obtenida a las 52 semanas en el cuestionario King’s Brief Interstitial Lung Disease (K-BILD), el tiempo hasta la primera exacerbación aguda de la ILD o la muerte en el transcurso de 52 semanas, y el tiempo hasta la muerte en el transcurso de 52 semanas.
Los pacientes tenían una media (desviación estándar [DE, mín-máx]) de edad de 65.8 años y un porcentaje medio de CVF previsto del 69.0% (15.6, 42-137). Los diagnósticos clínicos de ILD subyacente en los grupos representados en el ensayo fueron neumonitis por hipersensibilidad (26.1%), ILD autoinmunes (25.6%), neumonía intersticial idiopática inespecífica (18.9%), neumonía intersticial idiopática inclasificable (17.2%) y otras ILD (12.2%).
El ensayo INBUILD no estaba diseñado ni tenía la potencia estadística adecuada para proporcionar evidencias de un beneficio de nintedanib en subgrupos específicos de diagnóstico. Se demostraron efectos homogéneos en los subgrupos basados en los diagnósticos de ILD. La experiencia con nintedanib en ILD fibrosantes progresivas muy raras es limitada.
Pérdida anual de la CVF: La pérdida anual de la CVF (en ml) en el transcurso de 52 semanas disminuyó de forma significativa en 107.0 ml en los pacientes que recibieron OFEV® en comparación con los pacientes que recibieron placebo (Tabla 6), lo que corresponde a un efecto relativo del tratamiento del 57.0%.
Tabla 6. Pérdida anual de la CVF (ml) en el transcurso de 52 semanas
|
Placebo |
OFEV® |
|
|
Número de pacientes analizados |
331 |
332 |
|
Pérdida¹ (EE) en el transcurso de 52 semanas |
–187.8 (14.8) |
–80.8 (15.1) |
|
Comparación con el placebo |
||
|
Diferencia¹ |
107.0 |
|
|
95% de IC |
(65.4, 148.5) |
|
|
Valor p |
< 0.0001 |
|
¹ Basándose en un modelo de regresión de coeficientes aleatorios con efectos categóricos fijos del tratamiento, patrón en la TCAR, efectos continuos fijos del tiempo, CVF basal [ml] e incluyendo las interacciones de tratamiento por tiempo y de momento basal por tiempo.
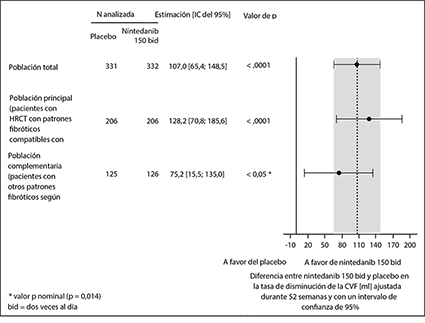
Se observaron resultados similares en la población coprincipal de pacientes con un patrón fibrótico de tipo NIU en la TCAR. El efecto del tratamiento fue homogéneo en la población complementaria de pacientes con otros patrones fibróticos en la TCAR (valor de p de la interacción 0.2268) (Figura 2).
Figura 2. Gráfico de bosque de la pérdida anual de la CVF (ml) en el transcurso de 52 semanas en las poblaciones de pacientes
Los resultados del efecto de OFEV® en la reducción de la pérdida anual de la CVF se confirmaron en todos los análisis preespecificados de sensibilidad y se observaron resultados homogéneos en los subgrupos preespecificados de eficacia: sexo, grupo de edad, raza, porcentaje de CVF basal previsto y diagnóstico clínico de ILD subyacente original en los grupos.
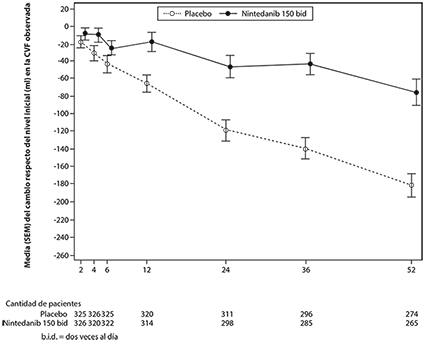
En la Figura 3 se muestra la evolución del cambio de la CVF respecto al valor basal a lo largo del tiempo en los grupos de tratamiento.
Figura 3. Cambio medio (EEM) observado en la CVF respecto al valor basal (ml) en el transcurso de 52 semanas
Además, se observaron efectos favorables de OFEV® sobre el cambio medio absoluto ajustado respecto al valor basal en el porcentaje de CVF previsto en la semana 52. El cambio medio absoluto ajustado respecto al valor basal en el porcentaje de CVF previsto en la semana 52 fue menor en el grupo tratado con nintedanib (-2.62%) que en el grupo tratado con placebo (-5.86%). La diferencia media ajustada entre los grupos de tratamiento fue de 3.24 (IC del 95%: 2.09, 4.40, valor nominal de p < 0.0001).
Análisis de los pacientes que responden en términos de CVF: La proporción de pacientes que responden en términos de CVF, definidos como los pacientes con una pérdida relativa del porcentaje de CVF previsto no superior al 5%, fue mayor en el grupo tratado con OFEV® que en el grupo tratado con placebo. Se observaron resultados similares en los análisis utilizando un umbral del 10% (Tabla 7).
Tabla 7. Proporción de pacientes que respondieron en términos de CVF a las 52 semanas del estudio INBUILD
|
Placebo |
OFEV® |
|
|---|---|---|
|
Número de pacientes analizados |
331 |
332 |
|
Umbral del 5% |
||
|
Cantidad (%) de respondedores por CVF1 |
104 (31.4) |
158 (47.6) |
|
Comparación con placebo |
||
|
Cociente de probabilidades2 |
2.01 |
|
|
IC del 95% |
(1.46, 2.76) |
|
|
Valor p nominal |
< 0.0001 |
|
|
Umbral del 10% |
||
|
Cantidad (%) de respondedores por CVF1 |
169 (51.1) |
197 (59.3) |
|
Comparación con placebo |
||
|
Cociente de probabilidades2 |
1.42 |
|
|
IC del 95% |
(1.04, 1.94) |
|
|
Valor p nominal |
0.0268 |
|
¹ Los pacientes que responden son aquellos que no presentan una pérdida relativa superior al 5% o superior al 10% en el % de CVF previsto, dependiendo del umbral y con una evaluación de la CVF a las 52 semanas (los pacientes de los que no se disponía de datos a las 52 semanas se consideraron pacientes que no respondieron).
² Basándose en un modelo de regresión logística con el % de CVF basal previsto como covariable continua y el patrón en la TCAR como covariable binaria.
Tiempo transcurrido hasta la primera exacerbación aguda de la ILD o la muerte: Durante todo el ensayo, la proporción de pacientes con al menos un acontecimiento de primera exacerbación aguda de la ILD o la muerte fue del 13.9% en el grupo tratado con OFEV® y del 19.6% en el grupo tratado con placebo. El cociente de riesgos (hazard ratio) fue de 0.67 (IC del 95%: 0.46, 0.98; valor nominal de p = 0.0387), que indica una reducción del 33% del riesgo de una primera exacerbación aguda de la ILD o de muerte en los pacientes tratados con OFEV® en comparación con los tratados con placebo (Figura 4).
Figura 4. Gráfico de Kaplan–Meier del tiempo hasta la primera exacerbación aguda de la ILD o la muerte durante todo el ensayo
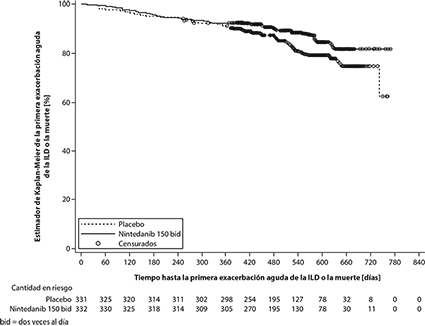
Análisis de supervivencia: El riesgo de muerte fue menor en el grupo tratado con OFEV® que en el grupo tratado con placebo. El cociente de riesgos (hazard ratio) fue 0.78 (IC del 95%: 0.50, 1.21; valor nominal de p = 0.2594), que indica una reducción del 22% del riesgo de muerte en los pacientes tratados con OFEV® en comparación con los tratados con placebo.
Tiempo hasta la progresión (≥ 10% de pérdida absoluta del porcentaje de CVF previsto) o muerte: En el ensayo INBUILD, el riesgo de progresión (≥ 10% de pérdida absoluta del porcentaje de CVF previsto) o muerte disminuyó en los pacientes tratados con OFEV®. La proporción de pacientes con un acontecimiento fue del 40.4% en el grupo tratado con OFEV® y del 54.7% en el grupo tratado con placebo. El cociente de riesgos (hazard ratio) fue de 0.66 (IC del 95%: 0.53, 0.83; p = 0.0003), que indica una reducción del 34% del riesgo de progresión (≥ 10% de pérdida absoluta del porcentaje de CVF previsto) o muerte en los pacientes tratados con OFEV® en comparación con los tratados con placebo.
Calidad de vida: El cambio medio ajustado respecto al valor basal en la puntuación total del K-BILD a las 52 semanas fue de -0.79 unidades en el grupo tratado con placebo y de 0.55 en el grupo tratado con OFEV®. La diferencia entre los grupos de tratamiento fue de 1.34 (IC del 95%: -0.31, 2.98; valor nominal de p = 0.1115).
El cambio absoluto medio ajustado respecto al valor basal en la puntuación del dominio de disnea del cuestionario de síntomas Living with Pulmonary Fibrosis (L-PF) a las 52 semanas fue de 4.28 en el grupo tratado con OFEV® en comparación con 7.81 en el grupo tratado con placebo. La diferencia media ajustada entre los grupos a favor de OFEV® fue de -3.53 (IC del 95%: -6.14, -0.92; valor nominal de p = 0.0081). El cambio absoluto medio ajustado respecto al valor basal en la puntuación del dominio de tos del cuestionario de síntomas L-PF a las 52 semanas fue de -1.84 en el grupo tratado con OFEV® en comparación con 4.25 en el grupo tratado con placebo. La diferencia media ajustada entre los grupos a favor de OFEV® fue de -6.09 (IC del 95%: -9.65, -2.53; valor nominal de p = 0.0008).
Enfermedad pulmonar intersticial asociada a esclerosis sistémica (SSc-ILD): Se ha estudiado la eficacia clínica de OFEV® en pacientes con SSc-ILD en un ensayo fase III doble ciego, aleatorizado y controlado con placebo (SENSCIS). Los pacientes habían sido diagnosticados de SSc-ILD de acuerdo con los criterios de clasificación de ES del American College of Rheumatology/European League Against Rheumatism de 2013 y una tomografía computarizada de alta resolución (TCAR) torácica realizada dentro de los 12 meses previos. Un total de 580 pacientes fueron aleatorizados en una proporción 1:1 a recibir OFEV® 150 mg dos veces al día o bien un placebo equivalente durante al menos 52 semanas, de los cuales 576 fueron tratados. La aleatorización se estratificó por el estado de anticuerpos antitopoisomerasa (ATA). Los pacientes individuales permanecieron con el tratamiento del ensayo ciego hasta 100 semanas (mediana de exposición a OFEV® de 15.4 meses; media de exposición a OFEV® de 14.5 meses).
El criterio de valoración principal fue la tasa anual de pérdida de la CVF a lo largo de 52 semanas. Los criterios de valoración secundarios clave fueron el cambio absoluto respecto al valor basal en la puntuación de la escala cutánea de Rodnan modificada (mRSS) en la semana 52 y el cambio absoluto respecto al valor basal en la puntuación total del cuestionario respiratorio de Saint George (SGRQ) en la semana 52.
En la población global, el 75.2% de los pacientes eran mujeres. La media (desviación estándar [DE, mín-máx]) de edad era de 54.0 años. En conjunto, el 51.9% de los pacientes tenían esclerosis sistémica (SSc) cutánea difusa y el 48.1% tenían ES cutánea limitada. La media (DE) de tiempo desde la primera aparición de un síntoma no-Raynaud fue de 3.49 (1.7) años. El 49.0% de los pacientes estaban en tratamiento estable con micofenolato en el momento basal. El perfil de seguridad en pacientes con o sin micofenolato en el momento basal fue comparable.
Pérdida anual de la CVF: La pérdida anual de la CVF (ml) en el transcurso de 52 semanas se redujo significativamente en 41.0 ml en los pacientes que recibieron OFEV® en comparación con los pacientes que recibieron placebo (Tabla 8), lo que corresponde a un efecto relativo del tratamiento del 43.8%.
Tabla 8. Pérdida anual de la CVF (ml) en el transcurso de 52 semanas
|
Placebo |
OFEV® 150 mg dos veces al día |
|
|
Número de pacientes analizados |
288 |
287 |
|
Pérdida¹ (EE) en el transcurso de 52 semanas |
-93.3 (13.5) |
-52.4 (13.8) |
|
Comparación con el placebo |
||
|
Diferencia¹ |
41.0 |
|
|
95% de IC |
(2.9, 79.0) |
|
|
Valor p |
< 0.05 |
|
¹ Basándose en un modelo de regresión de coeficientes aleatorios con efectos categóricos fijos del tratamiento, estado de ATA, sexo, efectos continuos fijos del tiempo, CVF basal [ml], edad, estatura e incluyendo las interacciones de tratamiento por tiempo y de momento basal por tiempo. Se incluyó el efecto aleatorio para la intersección específica del paciente y el tiempo. Los errores en un mismo paciente se modelizaron mediante una matriz de varianzas-covarianzas no estructurada. La variabilidad interindividual se modelizó mediante una matriz de varianzas-covarianzas de componentes de varianza.
El efecto de OFEV® para reducir la pérdida anual de la CVF fue similar en los distintos análisis de sensibilidad preespecificados y no se detectó heterogeneidad en los subgrupos preespecificados (p. ej., por edad, sexo y uso de micofenolato).
Además, se observaron efectos similares en otros criterios de valoración de la función pulmonar, p. ej., el cambio absoluto respecto al valor basal en la CVF en ml en la semana 52 (Figura 3 y Tabla 12) y la pérdida de la CVF en % prevista en el transcurso de 52 semanas (Tabla 13), lo que corrobora aún más los efectos de OFEV® a la hora de enlentecer la progresión de la SSc-ILD. Además, hubo menos pacientes en el grupo de OFEV® que tuvieron una pérdida absoluta de la CVF prevista > 5% (20.6% en el grupo de OFEV® frente a 28.5% en el grupo de placebo, CP = 0.65, p = 0.0287). La pérdida relativa de la CVF en ml > 10% fue comparable entre ambos grupos (16.7% en el grupo de OFEV® frente a 18.1% en el grupo de placebo, CP = 0.91, p = 0.6842). En estos análisis, los valores de CVF ausentes en la semana 52 se imputaron con el peor valor del paciente en el tratamiento.
Un análisis exploratorio de datos de hasta 100 semanas (duración máxima del tratamiento en SENSCIS) sugirió que el efecto de OFEV® durante el tratamiento en la ralentización de la progresión de SSc-ILD persistió después de 52 semanas.
Figura 5. Cambio medio (EEM) observado en la CVF respecto al valor basal (ml) en el transcurso de 52 semanas
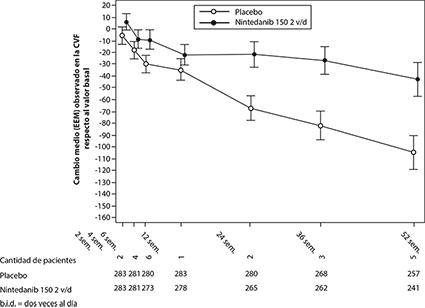
Tabla 9. Cambio absoluto respecto al valor basal en la CVF (ml) en la semana 52
|
Placebo |
OFEV® 150 mg dos veces al día |
|
|
Número de pacientes analizados |
288 |
288 |
|
Media (DE) en el momento basal |
2541.0 (815.5) |
2458.5 (735.9) |
|
Cambio medio¹ (EE) respecto al valor basal en la semana 52 |
-101.0 (13.6) |
-54.6 (13.9) |
|
Comparación con el placebo |
||
|
Media¹ |
46.4 |
|
|
95% de IC |
(8.1, 84.7) |
|
|
Valor p |
< 0.05 |
|
¹ Basándose en un modelo mixto de medidas repetidas (MMMR), con efectos categóricos fijos de estado de ATA, visita, interacción de tratamiento por visita, interacción de momento basal por visita, edad, sexo y estatura. La visita fue la medida repetida. Los errores dentro de un mismo paciente se modelizaron mediante estructura de varianzas-covarianzas no estructurada. La media ajustada se basó en todos los pacientes analizados en el modelo (no sólo los pacientes con una medición basal y una medición en la semana 52).
Tabla 10. Pérdida anual de la CVF (% previsto) en el trascurso de 52 semanas
|
Placebo |
OFEV® |
|
|---|---|---|
|
Número de pacientes analizados |
288 |
287 |
|
Pérdida¹ (EE) en el transcurso de 52 semanas |
-2.6 (0.4) |
-1.4 (0.4) |
|
Comparación con el placebo |
||
|
Diferencia¹ |
1.15 |
|
|
95% de IC |
(0.09, 2.21) |
|
|
Valor p |
< 0.05 |
|
¹ Basándose en un modelo de regresión de coeficientes aleatorios con efectos categóricos fijos de tratamiento, estado de ATA, efectos continuos fijos del tiempo, CVF basal [% previsto] e incluyendo las interacciones de tratamiento por tiempo y de momento basal por tiempo. Se incluyó el efecto aleatorio para la coordenada específica del paciente y el tiempo. Los errores dentro de un mismo paciente se modelizaron mediante una matriz de varianzas-covarianzas no estructurada. La variabilidad interindividual se modelizó mediante una matriz de varianzas-covarianzas con componentes de varianza.
Cambio respecto al valor basal en la puntuación de la escala cutánea de Rodnan modificada (mRSS)en la semana 52: El cambio absoluto medio ajustado respecto al valor basal en la escala mRSS en la semana 52 fue comparable entre el grupo de OFEV® (-2.17 [IC del 95% -2.69, -1.65]) y el grupo de placebo (-1.96 [IC del 95% -2.48, -1.45]). La diferencia media ajustada entre los grupos de tratamiento fue de -0.21 (IC del 95% -0.94, 0.53; p = 0.5785).
Cambio respecto al valor basal en la puntuación total del cuestionario respiratorio de St. George (SGRQ) en la semana 52: El cambio absoluto medio ajustado respecto al valor basal en la puntuación total del SGRQ en la semana 52 fue comparable entre el grupo de OFEV® (0.81 [IC del 95% -0.92, 2.55]) y el grupo de placebo (-0.88 [IC del 95% -2.58, 0.82]). La diferencia media ajustada entre los grupos de tratamiento fue de 1.69 (IC del 95% -0.73, 4.12; p = 0.1711).
Análisis de la supervivencia: La mortalidad a lo largo de todo el ensayo fue comparable entre el grupo de OFEV® (N = 10; 3.5%) y el grupo de placebo (N = 9; 3.1%). El análisis del tiempo hasta la muerte durante todo el ensayo condujo a un CR de 1.16 (IC del 95% 0.47, 2.84; p = 0.7535).
Intervalo QT: En un estudio específico realizado en pacientes con cáncer de las células renales, se registraron las mediciones de los intervalos QT/QTc y se demostró que una dosis oral única de 200 mg de nintedanib, así como dosis orales múltiples de 200 mg de nintedanib administradas dos veces al día durante 15 días no prolongaron el intervalo QTcF.
Población pediátrica:
No está registrado el tratamiento en pacientes pediátricos con nintedanib para las enfermedades pulmonares intersticiales (ILD) fibrosantes.
Farmacocinética:
Absorción: Nintedanib alcanzó la concentración plasmática máxima aproximadamente de 2 a 4 horas después de la administración oral como cápsula de gelatina blanda junto con alimentos (rango de 0.5 a 8 horas). La biodisponibilidad absoluta de una dosis de 100 mg fue del 4.69% (90% de IC: 3.615 a 6.078) en voluntarios sanos. La absorción y la biodisponibilidad disminuyen por los efectos de los transportadores y por el metabolismo sustancial de primer paso. La proporcionalidad de la dosis se demostró mediante un aumento de la exposición a nintedanib (rango de dosis de 50 a 450 mg una vez al día y de 150 a 300 mg dos veces al día). Las concentraciones plasmáticas en estado estacionario se lograron como muy tarde en el plazo de una semana de dosificación.
Después de la ingesta de alimentos, la exposición a nintedanib aumentó en aproximadamente el 20% en comparación con la administración en ayunas (IC: 95.3 a 152.5%) y la absorción se retrasó (mediana de tmáx en ayunas: 2.00 h; con alimentos: 3.98 h).
Distribución: Nintedanib sigue al menos una cinética de disposición bifásica. Después de una perfusión intravenosa, se observó un alto volumen de distribución (Vss: 1.050 l, 45.0% de gCV).
La unión a proteínas in vitro de nintedanib en el plasma humano fue alta, con una fracción unida del 97.8%. Se considera que la albúmina sérica es la proteína de unión más importante. Nintedanib se distribuye preferentemente en el plasma, con una relación sangre/plasma de 0.869.
Biotransformación: La reacción metabólica prevalente para nintedanib es la ruptura hifrolítica mediante esterasas que dan lugar a la fracción de ácido libre BIBF 1202. A continuación, BIBF 1202 se glucuronida mediante enzimas uridina 5’-difosfo-glucurosiltransferasa (UGT), concretamente UGT 1A1, UGT 1A7, UGT 1A8 y UGT 1A10, a glucurónido de BIBF 1202.
Tan sólo una pequeña proporción de la biotransformación de nintedanib se realiza a través de las vías CYP, siendo la CYP 3A4 la enzima predominante implicada. El principal metabolito dependiente de CYP no pudo detectarse en el plasma en el estudio ADME realizado con humanos. In vitro, el metabolismo dependiente de CYP representó aproximadamente un 5% en comparación con aproximadamente un 25% de ruptura de ésteres. Nintedanib, BIBF 1202 y el glucurónido BIBF 1202 tampoco inhibieron ni indujeron las enzimas CYP en estudios preclínicos con animales. Por lo tanto, no cabe esperar interacciones farmacológicas entre nintedanib y sustratos de CYP, inhibidores de CYP o inductores de CYP.
Eliminación: El aclaramiento plasmático total después de la perfusión intravenosa fue alto (aclaramiento: 1.390 ml/min, 28.8% de gCV). La eliminación por la orina del principio activo inalterado en el plazo de 48 horas fue de aproximadamente el 0.05% de la dosis (31.5% de gCV) después de la administración oral, y de aproximadamente 1.4% de la dosis (24.2% de gCV) después de la administración intravenosa; el aclaramiento renal fue de 20 ml/min (32.6% de gCV). La principal vía de eliminación del fármaco marcado radioactivamente después de la administración oral de [14C] nintedanib fue la excreción biliar/fecal (93.4% de la dosis, 2.61% de gCV). La contribución de la eliminación renal al aclaramiento total fue baja (0.649% de la dosis, 26.3% de gCV). La recuperación total se consideró completa (por encima del 90%) en los cuatro días posteriores a la dosificación. La semivida terminal de nintedanib fue de entre 10 y 15 horas (gCV de aproximadamente el 50%).
Linealidad/no linealidad: La farmacocinética de nintedanib se puede considerar lineal respecto al tiempo (es decir, los datos de una sola dosis pueden extrapolarse a los datos de múltiples dosis). La acumulación en el caso de múltiples administraciones fue de 1.04 veces para la Cmáx y de 1.38 veces para el AUCτ. Las concentraciones mínimas de nintedanib permanecieron estables durante más de un año.
Transporte: Nintedanib es un sustrato de la gp-P. Para obtener más información sobre el potencial de interacción de nintedanib con este transportador, ver sección 4.5. Se demostró que nintedanib no es un sustrato ni un inhibidor de OATP-1B1, OATP-1B3, OATP-2B1, OCT-2 o MRP-2 in vitro. Nintedanib tampoco resultó ser un sustrato de la BCRP. Sólo se observó in vitro un leve potencial inhibidor en el OCT-1, la BCRP y la gp-P, pero se considera que esto tiene una baja relevancia clínica. Lo mismo se aplica a nintedanib como sustrato del OCT-1.
Análisis farmacocinético poblacional en poblaciones especiales: Las propiedades farmacocinéticas de nintedanib fueron similares en los voluntarios sanos, los pacientes con FPI, los pacientes con otras ILD fibrosantes crónicas con un fenotipo progresivo, los pacientes con SSc-ILD y los pacientes con cáncer. Basándose en los resultados de un análisis farmacocinético poblacional en pacientes con FPI y cáncer de pulmón no microcítico (CPNM) (N = 1.191) y en las investigaciones descriptivas, la exposición a nintedanib no se vio afectada por el sexo (corregido por el peso corporal), la insuficiencia renal leve y moderada (calculada según el aclaramiento de creatinina), el consumo de alcohol ni por el genotipo de la gp-P. Los análisis farmacocinéticos poblacionales indicaron efectos moderados en la exposición a nintedanib dependiendo de la edad, el peso corporal y la raza (ver más abajo). Teniendo en cuenta la alta variabilidad de la exposición entre individuos, los efectos moderados observados no se consideran clínicamente relevantes (ver sección 4.4).
Edad: La exposición a nintedanib aumentó linealmente con la edad. El AUCτ,ss disminuyó en un 16% en el caso de un paciente de 45 años y aumentó en un 13% en el caso de un paciente de 76 años en comparación con un paciente con la mediana de edad de 62 años. El rango de edad cubierto por el análisis fue de 29 a 85 años; aproximadamente el 5% de la población era mayor de 75 años. Basándose en un modelo farmacocinético poblacional, se observó un aumento en la exposición a nintedanib de aproximadamente entre el 20 y el 25% en pacientes de 75 años o más, en comparación con pacientes menores de 65 años.
No se han realizado estudios con poblaciones pediátricas.
Peso corporal: Se observó una correlación inversa entre el peso corporal y la exposición a nintedanib. El AUCτ,ss aumentó en un 25% en el caso de un paciente de 50 kg (percentil 5) y disminuyó en un 19% en el caso de un paciente de 100 kg (percentil 95) en comparación con un paciente con la mediana de peso de 71.5 kg.
Raza: La exposición media de la población a nintedanib fue un 33-50% superior en pacientes chinos, taiwaneses e indios y un 16% superior en pacientes japoneses, mientras que fue un 16-22% inferior en el caso de pacientes coreanos comparados con los caucásicos (corregido por peso corporal). Los datos procedentes de individuos de raza negra eran muy limitados, pero se encuentran en el mismo rango que en el caso de los caucásicos.
Insuficiencia hepática: En un estudio específico de fase I de dosis única y comparado con individuos sanos, la exposición a nintedanib basándose en la Cmáx y el AUC fue 2.2 veces más alta en voluntarios con insuficiencia hepática leve (Child Pugh A; IC del 90%: 1.3-3,7 para la Cmáx y 1.2-3.8 para el AUC, respectivamente). En voluntarios con insuficiencia hepática moderada (Child Pugh B), la exposición fue 7.6 veces más alta basándose en la Cmáx (IC del 90%: 4.4-13.2) y 8,7 veces más alta (IC del 90%: 5.7-13.1) basándose en el AUC, respectivamente, comparado con los voluntarios sanos. No se han realizado estudios en individuos con insuficiencia hepática grave (Child Pugh C).
Tratamiento conjunto con pirfenidona: En un estudio farmacocinético específico, se investigó el tratamiento conjunto de nintedanib con pirfenidona en pacientes con FPI. El grupo 1 recibió una dosis única de 150 mg de nintedanib antes y después del ajuste a 801 mg de pirfenidona tres veces al día en estado estacionario (n = 20 pacientes tratados). El grupo 2 recibió tratamiento en estado estacionario con 801 mg de pirfenidona tres veces al día y fue objeto de la elaboración de un perfil farmacocinético antes y después de al menos 7 días de tratamiento conjunto con 150 mg de nintedanib dos veces al día (n = 17 pacientes tratados). En el grupo 1, las relaciones ajustadas de las medias geométricas (intervalo de confianza [IC] del 90%) fueron del 93% (57%-151%) y del 96% (70%-131%) para la Cmáx y el AUC0-tz de nintedanib, respectivamente (n = 12 para la comparación intraindividual). En el grupo 2, las relaciones ajustadas de las medias geométricas (IC del 90%) fueron del 97% (86%-110%) y del 95% (86%-106%) para la Cmáx,ss y el AUCτ,ss de pirfenidona, respectivamente (n = 12 para la comparación intraindividual).
De acuerdo con estos resultados, no existe evidencia de una interacción farmacocinética relevante entre nintedanib y pirfenidona cuando se administran en combinación.
Tratamiento concomitante con bosentán: En un estudio de farmacocinética específico, se investigó el tratamiento concomitante de OFEV® con bosentán en voluntarios sanos. Los sujetos recibieron una dosis única de 150 mg de OFEV® antes y después de administraciones múltiples de 125 mg de bosentán dos veces al día en estado estacionario. Los cocientes ajustados de media geométrica (intervalo de confianza [IC] del 90% fueron del 103% [86-124%] y del 99% [91%-107%] para la Cmáx y el AUC0-tz de nintedanib, respectivamente (n = 13), lo que indica que la administración conjunta de nintedanib con bosentán no alteró la farmacocinética de nintedanib.
Tratamiento concomitante con anticonceptivos hormonales orales: En un estudio farmacocinético específico, las pacientes con SSc-ILD recibieron una dosis única de una combinación de 30 μg de etinilestradiol y 150 μg de levonorgestrel antes y después de una pauta de dos veces al día de 150 mg de nintedanib durante al menos 10 días. Los cocientes ajustados de media geométrica (intervalo de confianza [IC] del 90%) fueron del 117% (108%-127%; Cmáx) y del 101% (93%-111%; AUC0-tz) para etinilestradiol y del 101% (90%-113%; Cmáx) y del 96% (91%-102%; AUC0-tz) para levonorgestrel, respectivamente (n = 15), lo que indica que la administración conjunta de nintedanib no tiene ningún efecto relevante sobre la exposición plasmática de etinilestradiol y levonorgestrel.
Relación exposición-respuesta: Los análisis de la relación exposición-respuesta de pacientes con FPI y otras ILD fibrosantes crónicas con un fenotipo progresivo indicaron una relación débil entre la exposición plasmática a nintedanib y las elevaciones de la ALT y/o de la AST. La dosis administrada real podría ser el mejor factor predictivo del riesgo de aparición de diarrea de cualquier intensidad, aunque no pueda descartarse la exposición plasmática como factor determinante del riesgo.
CONTRAINDICACIONES:
OFEV® está contraindicado en pacientes con hipersensibilidad conocida a nintedanib, el cacahuate o la soya, o a cualquiera de los excipientes (véase la sección Forma farmacéutica y formulación).
OFEV® está contraindicado durante el embarazo y lactancia (véanse las secciones Embarazo, Lactancia y Fertilidad, Toxicología). No se administre en menores de 18 años.
RESTRICCIONES DE USO DURANTE EL EMBARAZO Y LA LACTANCIA:
Mujeres en edad fértil/anticoncepción: Nintedanib puede causar daño fetal en humanos (ver sección Toxicología). Se debe advertir a las mujeres en edad fértil que estén siendo tratadas con OFEV® que eviten quedarse embarazadas mientras reciban dicho tratamiento y que utilicen métodos anticonceptivos altamente efectivos al inicio del tratamiento, durante el mismo y al menos 3 meses después de la última dosis de OFEV®. Nintedanib no afecta de manera relevante a la exposición plasmática de etinilestradiol y levonorgestrel. La eficacia de los anticonceptivos hormonales orales puede verse reducida por los vómitos y/o la diarrea u otras situaciones en las que la absorción pueda verse afectada. Se debe advertir a las mujeres que tomen anticonceptivos hormonales orales y que experimenten estas situaciones que utilicen un método anticonceptivo alternativo altamente efectivo.
Embarazo: No existe información sobre el uso de OFEV® en las mujeres embarazadas; pero los estudios preclínicos de este principio activo en animales han mostrado la toxicidad para la reproducción (véase la sección Toxicología). Como nintedanib puede causar daño fetal también en humanos, no se debe utilizar durante el embarazo (véase la sección Contraindicaciones) y se deben realizar pruebas de embarazo antes y durante el tratamiento con OFEV®, según proceda.
Se debe aconsejar a las pacientes que informen a su médico o farmacéutico si se quedan embarazadas durante el tratamiento con OFEV®.
Si una paciente se queda embarazada mientras está recibiendo tratamiento con OFEV®, se debe suspender el tratamiento y la paciente debe recibir la información correspondiente sobre el riesgo potencial que existe para el feto.
Lactancia: No se dispone de información relativa a la excreción de nintedanib y sus metabolitos en la leche materna.
Los estudios preclínicos mostraron que pequeñas cantidades de nintedanib y sus metabolitos (≤ 0.5% de la dosis administrada) se excretaban en la leche de las ratas lactantes. No se puede excluir el riesgo para los recién nacidos/lactantes. Debe interrumpirse la lactancia durante el tratamiento con OFEV®.
Fertilidad: Sobre la base de las investigaciones preclínicas, no hay evidencia de que afecte la fertilidad masculina (véase la sección Toxicología). Teniendo en cuenta los estudios de toxicidad subcrónica y crónica, no hay evidencia de que la fertilidad femenina en ratas se vea afectada a un nivel de exposición sistémica similar al de la dosis humana máxima recomendada de 150 mg dos veces al día.
REACCIONES SECUNDARIAS Y ADVERSAS:
Resumen del perfil de seguridad:
Estudios clínicos en pacientes adultos:
Se investigó OFEV® en estudios clínicos en los que participaron 1529 pacientes con fibrosis pulmonar idiopática (FPI), 663 pacientes con otras enfermedades pulmonares intersticiales (ILD) fibrosantes crónicas con un fenotipo progresivo y 576 pacientes con enfermedad pulmonar intersticial asociada a la esclerosis sistémica (SSc-ILD).
Los datos de seguridad que se brindan a continuación se basan en lo siguiente:
• Dos estudios aleatorizados, doble ciego, comparativos con placebo, de fase III, en los que se comparó el tratamiento con OFEV® 150 mg dos veces al día frente al placebo durante 52 semanas (INPULSIS-1 e INPULSIS-2) y en los que participaron 1061 pacientes con FPI.
• Un estudio aleatorizado, doble ciego, comparativo con placebo, de fase III en el que se comparó el tratamiento con OFEV® 150 mg dos veces al día frente al placebo durante al menos 52 semanas en 663 pacientes con otras ILD fibrosantes crónicas con un fenotipo progresivo (INBUILD).
• Un estudio aleatorizado, doble ciego, comparativo con placebo, de fase III, en el que se comparó el tratamiento con OFEV® 150 mg dos veces al día frente al placebo durante al menos 52 semanas y en el que participaron 576 pacientes con SSc-ILD (SENSCIS).
• Los datos observados durante la experiencia posterior a la comercialización.
En los estudios clínicos, las reacciones adversas asociadas al uso de OFEV® informadas con mayor frecuencia fueron diarrea, náuseas y vómitos, dolor abdominal, disminución del apetito, descenso de peso y elevación de las enzimas hepáticas.
El perfil de seguridad de OFEV® en un estudio de extensión a largo plazo en pacientes con FPI, tratados durante un periodo de 1 a más de 5 años, fue concordante con el observado en los estudios de fase III (véase la sección Estudios clínicos).
Tabla de reacciones adversas: La tabla 11 incluye un resumen de las reacciones adversas a medicamentos (RAM) según la clasificación de órganos del sistema MedDRA y la categoría de frecuencia, usando la siguiente convención: muy frecuentes (≥ 1/10), frecuentes (≥ 1/100 a < 1/10), poco frecuentes (≥ 1/1.000 a < 1/100), raras (≥ 1/10.000 a < 1/1.000), muy raras (< 1/10.000), frecuencia no conocida (no se puede estimar a partir de los datos disponibles).
Tabla 11. Resumen de las RAM por categoría de frecuencia
|
Frecuencia |
|||
|
Término preferido del sistema de clasificación de órganos |
Fibrosis pulmonar idiopática |
Otras ILD fibrosantes crónicas con un fenotipo progresivo |
Enfermedad pulmonar intersticial asociada a esclerosis sistémica |
|
Trastornos de la sangre y del sistema linfático |
|||
|
Trombocitopenia |
Poco frecuente |
Poco frecuente |
Poco frecuente |
|
Trastornos del metabolismo y de la nutrición |
|||
|
Pérdida de peso |
Frecuente |
Frecuente |
Frecuente |
|
Apetito disminuido |
Frecuente |
Muy frecuente |
Frecuente |
|
Deshidratación |
Poco frecuente |
Poco frecuente |
Frecuencia no conocida |
|
Trastornos cardiacos |
|||
|
Infarto de miocardio |
Poco frecuente |
Poco frecuente |
Frecuencia no conocida |
|
Trastornos vasculares |
|||
|
Sangrado |
Frecuente |
Frecuente |
Frecuente |
|
Hipertensión |
Poco frecuente |
Frecuente |
Frecuente |
|
Aneurismas y disecciones arteriales |
Frecuencia no conocida |
Frecuencia no conocida |
Frecuencia no conocida |
|
Trastornos gastrointestinales |
|||
|
Diarrea |
Muy frecuente |
Muy frecuente |
Muy frecuente |
|
Náuseas |
Muy frecuente |
Muy frecuente |
Muy frecuente |
|
Dolor abdominal |
Muy frecuente |
Muy frecuente |
Muy frecuente |
|
Vómitos |
Frecuente |
Muy frecuente |
Muy frecuente |
|
Pancreatitis |
Poco frecuente |
Poco frecuente |
Frecuencia no conocida |
|
Colitis |
Poco frecuente |
Poco frecuente |
Poco frecuente |
|
Trastornos hepatobiliares |
|||
|
Daño hepático inducido por el fármaco |
Poco frecuente |
Frecuente |
Poco frecuente |
|
Aumento de las enzimas hepáticas |
Muy frecuente |
Muy frecuente |
Muy frecuente |
|
Aumento de la alanina aminotransferase (ALT) |
Frecuente |
Muy frecuente |
Frecuente |
|
Aumento de la aspartato aminotransferasa (AST) |
Frecuente |
Frecuente |
Frecuente |
|
Aumento de la gamma-glutamil-transferasa (GGT) |
Frecuente |
Frecuente |
Frecuente |
|
Hiperbilirrubinemia |
Poco frecuente |
Poco frecuente |
Frecuencia no conocida |
|
Aumento de la fosfatasa alcalina (FA) en sangre |
Poco frecuente |
Frecuente |
Frecuente |
|
Trastornos de la piel y del tejido subcutáneo |
|||
|
Erupción |
Frecuente |
Frecuente |
Poco frecuente |
|
Prurito |
Poco frecuente |
Poco frecuente |
Poco frecuente |
|
Alopecia |
Poco frecuente |
Poco frecuente |
Frecuencia no conocida |
|
Trastornos renales y urinarios |
|||
|
Insuficiencia renal |
Frecuencia no conocida |
Poco frecuente |
Poco frecuente |
|
Proteinuria |
Poco frecuente |
Poco frecuente |
Frecuencia no conocida |
|
Trastornos del sistema nervioso |
|||
|
Cefalea |
Frecuente |
Frecuente |
Frecuente |
|
Síndrome de encefalopatía posterior reversible |
Frecuencia no conocida |
Frecuencia no conocida |
Frecuencia no conocida |
Descripción de reacciones adversas específicas:
Diarrea: En los ensayos clínicos, la diarrea fue el acontecimiento gastrointestinal más frecuente notificado. En la mayoría de los pacientes, el episodio fue de intensidad leve a moderada. Más de dos tercios de los pacientes que sufrieron diarrea describieron que ésta había aparecido por primera vez durante los primeros tres meses de tratamiento. En la mayoría de los pacientes, los episodios se trataron con un tratamiento antidiarreico, una reducción de la dosis o la interrupción del tratamiento.
En la Tabla 12 se muestra una descripción general de los episodios de diarrea notificados en los ensayos clínicos:
Tabla 12. Diarrea en los ensayos clínicos a lo largo de 52 semanas
|
INPULSIS |
INBUILD |
SENSCIS |
||||
|---|---|---|---|---|---|---|
|
Placebo |
OFEV® |
Placebo |
OFEV® |
Placebo |
OFEV® |
|
|
Diarrea |
18.4% |
62.4% |
23.9% |
66.9% |
31.6% |
75.7% |
|
Diarrea grave |
0.5% |
3.3.% |
0.9% |
2.4% |
1.0% |
4.2% |
|
Diarrea que da lugar a la reducción de la dosis de OFEV® |
0% |
10.7% |
0.9% |
16.0% |
1.0% |
22.2% |
|
Diarrea que da lugar a la suspensión de OFEV® |
0.2% |
4.4% |
0.3% |
5.7% |
0.3% |
6.9% |
Aumento de las enzimas hepáticas: En los ensayos INPULSIS, el aumento de las enzimas hepáticas (ver sección 4.4) se describió en el 13.6% frente al 2.6% de los pacientes tratados con OFEV® y placebo, respectivamente. En el ensayo INBUILD, se notificó aumento de las enzimas hepáticas en el 22.6% frente al 5.7% de los pacientes tratados con OFEV® y placebo, respectivamente. En el ensayo SENSCIS, se notificó aumento de las enzimas hepáticas en el 13.2% frente al 3.1% de los pacientes tratados con OFEV® y placebo, respectivamente. Los aumentos de las enzimas hepáticas fueron reversibles y no estuvieron asociados a una enfermedad hepática clínicamente manifiesta.
Para obtener más información sobre las poblaciones especiales y sobre las medidas y ajustes de dosis recomendados en caso de diarrea y aumento de las enzimas hepáticas, ver las secciones Advertencias y precauciones especiales y Dosis y vía de administración, respectivamente.
Sangrado: En los ensayos clínicos, la frecuencia de pacientes que experimentaron sangrado fue ligeramente mayor en los pacientes tratados con OFEV® o similar entre los grupos de tratamiento (10.3% con OFEV® frente al 7.8% con placebo en los ensayos INPULSIS; 11.1% con OFEV® frente al 12.7% con placebo en el ensayo INBUILD; 11.1% con OFEV® frente al 8.3% con placebo en el ensayo SENSCIS). El acontecimiento de sangrado notificado más frecuente fue epistaxis no grave. Se produjeron acontecimientos de sangrado graves con una frecuencia baja en los dos grupos de tratamiento (1.3% con OFEV® frente al 1.4% con placebo en los ensayos INPULSIS; 0.9% con OFEV® frente al 1.5% con placebo en el ensayo INBUILD; 1.4% con OFEV® frente al 0.7% con placebo en el ensayo SENSCIS). Los acontecimientos de sangrado del periodo de poscomercialización afectan, entre otros, al aparato gastrointestinal, al aparato respiratorio y al sistema nervioso central, siendo los más frecuentes los acontecimientos gastrointestinales.
Proteinuria: En los ensayos clínicos, la frecuencia de pacientes que experimentaron proteinuria fue baja y similar entre los grupos de tratamiento (0,8% con OFEV® frente al 0,5% con placebo en los ensayos INPULSIS; 1,5% con OFEV® frente al 1,8% con placebo en el ensayo INBUILD; 1,0% con OFEV® frente al 0,0% con placebo en el ensayo SENSCIS). No se ha notificado síndrome nefrótico en los ensayos clínicos. En el periodo de poscomercialización, se han notificado muy pocos casos de proteinuria en rango nefrótico con o sin disfunción renal. Los hallazgos histológicos en casos individuales eran compatibles con microangiopatía glomerular con o sin trombos renales. Se ha observado la desaparición de los síntomas tras suspender el tratamiento con OFEV®, con proteinuria residual en algunos casos. En pacientes que desarrollan signos o síntomas de síndrome nefrótico se debe valorar la necesidad de interrumpir el tratamiento.
PRECAUCIONES EN RELACIÓN CON EFECTOS DE CARCINOGÉNESIS, MUTAGÉNESIS, TERATOGÉNESIS Y SOBRE LA FERTILIDAD:
Toxicología general: Los estudios de toxicidad de una sola dosis realizados en ratas y ratones indicaron un bajo potencial de toxicidad aguda de nintedanib. En los estudios de toxicología con dosis repetidas realizados en ratas, los efectos adversos (como el engrosamiento de las placas epifisarias o las lesiones de los incisivos) estuvieron relacionados en su mayoría con el mecanismo de acción (es decir, la inhibición del VEGFR-2) de nintedanib. Estos cambios se conocen de otros inhibidores del VEGFR-2 y se pueden considerar efectos de clase.
La diarrea y los vómitos, acompañados de una reducción en la ingesta de alimentos y una pérdida del peso corporal, se observaron en estudios de toxicidad con no roedores.
No se produjeron signos de aumentos en las enzimas hepáticas en ratas, perros y monos cynomolgus. Los aumentos leves en las enzimas hepáticas que no se debían a efectos adversos graves, como la diarrea, se observaron únicamente en monos rhesus.
Toxicidad para la reproducción: En el caso de las ratas, la mortalidad embriofetal y los efectos teratogénicos se observaron a una exposición inferior a la exposición humana a la dosis humana máxima recomendada de 150 mg dos veces al día. También se observaron efectos en el desarrollo del esqueleto axial y en el desarrollo de las grandes arterias a niveles de exposición subterapéuticos.
En el caso de los conejos, la mortalidad embriofetal y los efectos teratogénicos se observaron a una exposición aproximadamente 3 veces superior a la dosis humana máxima recomendada, pero se observaron efectos equívocos en el desarrollo embriofetal del esqueleto axial y del corazón a una exposición inferior a la dosis humana máxima recomendada de 150 mg dos veces al día.
En un estudio de desarrollo prenatal y posnatal realizado en ratas, los efectos sobre el desarrollo prenatal y posnatal se observaron a una exposición inferior a la dosis humana máxima recomendada.
Un estudio de la fertilidad en varones y del desarrollo embrionario temprano hasta la implantación en ratas no reveló efectos en el sistema reproductivo ni en la fertilidad de los varones.
En el caso de las ratas, pequeñas cantidades de nintedanib marcado radiactivamente y/o sus metabolitos se excretaron en la leche (≤ 0.5% de la dosis administrada).
A partir de los estudios de carcinogénesis de dos años en ratones y ratas, no se obtuvieron pruebas de un potencial carcinógeno de nintedanib.
Los estudios de genotoxicidad no indicaron ningún potencial mutagénico para nintedanib.
INTERACCIONES MEDICAMENTOSAS Y DE OTRO GÉNERO:
Glicoproteína-P (gp-P): Nintedanib es un sustrato de gp-P (véase la sección Farmacocinética). La administración conjunta con ketoconazol, un potente inhibidor de la gp-P, aumentó la exposición a nintedanib 1.61 veces basándose en el AUC y 1.83 veces basándose en la Cmáx en un estudio específico de interacción farmacológica. En un estudio de interacción farmacológica con rifampicina, un potente inductor de la gp-P, la exposición a nintedanib disminuyó al 50.3% basándose en el AUC y al 60.3% basándose en la Cmáx en la administración conjunta con rifampicina en comparación con la administración de nintedanib en monoterapia. Si se administran de forma conjunta con OFEV®, los inhibidores potentes de la gp-P (por ejemplo, ketoconazol, eritromicina o ciclosporina) pueden aumentar la exposición a nintedanib. En tales casos, es preciso controlar estrechamente a los pacientes para evaluar la tolerabilidad a nintedanib. El tratamiento de los efectos adversos puede requerir la interrupción, la reducción de la dosis o la suspensión del tratamiento con OFEV® (véase la sección Dosis y vía de administración).
Los inductores potentes de la gp-P (por ejemplo, rifampicina, carbamazepina, fenitoína y la hierba de San Juan) pueden disminuir la exposición a nintedanib. En este caso se debe valorar la selección de un medicamento concomitante alternativo que no tenga potencial de inducción de la gp-P o en el que dicho potencial sea mínimo.
Alimentos:
Se recomienda que OFEV® se ingiera con alimentos (véase la sección Farmacocinética).
Enzimas del citocromo CYP: Tan sólo una pequeña proporción de la biotransformación de nintedanib se produce a través de las vías del CYP. Nintedanib y sus metabolitos, la porción de ácido libre BIBF 1202 y su glucurónido BIBF 1202, no inhibieron ni indujeron las enzimas CYP en estudios preclínicos con animales (véase la sección Farmacocinética). Así pues, se considera que hay pocas probabilidades de que se produzcan interacciones farmacológicas con nintedanib basándose en el metabolismo del CYP.
Administración conjunta con otros medicamentos: La administración conjunta de nintedanib con anticonceptivos hormonales orales no alteró la farmacocinética de los anticonceptivos hormonales orales de forma significativa (véase la sección Farmacocinética).
La administración conjunta de nintedanib y bosentán no alteró la farmacocinética de nintedanib (véase la sección Farmacocinética).
Población pediátrica:
Solamente se han realizado estudios de interacciones en adultos.
ALTERACIONES EN LOS RESULTADOS DE PRUEBAS DE LABORATORIO:
No se han reportado cambios clínicamente significativos en los parámetros de laboratorio y de ECG, excepto por los ya enumerados como efectos secundarios:
• Disminución del recuento de plaquetas (efecto secundario: trombocitopenia).
• Aumento de las enzimas hepáticas (aumento de la alanina aminotransferasa, aumento de la aspartato aminotransferasa, aumento de la gamma-glutamiltransferasa, aumento de la fosfatasa alcalina en sangre).
• Aumento de la bilirrubina.
• Prueba de proteína en orina positiva (efecto secundario: proteinuria).
PRECAUCIONES GENERALES:
Trastornos gastrointestinales:
Diarrea: En los ensayos clínicos (ver sección Estudios clínicos), la diarrea fue la reacción adversa gastrointestinal más frecuente descrita. En la mayoría de los pacientes, la reacción adversa fue de intensidad leve a moderada y se produjo en los primeros 3 meses de tratamiento.
En los estudios INPULSIS realizados en pacientes con FPI, se informó diarrea en el 62.4% versus el 18.4% de los pacientes tratados con OFEV® y placebo, respectivamente. La diarrea causó una reducción de la dosis de OFEV® en el 10.7% de los pacientes y a la interrupción de OFEV® en el 4.4% de los pacientes [10]. En el estudio INBUILD realizado en pacientes con otras ILD fibrosantes crónicas con un fenotipo progresivo, se informó diarrea en el 66.9% versus el 23.9% de los pacientes tratados con OFEV® y placebo, respectivamente. La diarrea causó una reducción de la dosis de OFEV® en el 16.0% de los pacientes y a la interrupción de OFEV® en el 5.7% de los pacientes [3, 25]. En el estudio SENSCIS realizado en pacientes con SSc-ILD, se informó diarrea en el 75.7% versus el 31.6% de los pacientes tratados con OFEV® y placebo, respectivamente. La diarrea causó una reducción de la dosis de OFEV® en el 22.2% de los pacientes y a la interrupción de OFEV® en el 6.9% de los pacientes [5, 26]. (Véase la sección Reacciones adversas).
Se debe tratar a los pacientes en cuanto aparezcan los primeros síntomas con una adecuada hidratación y la administración de medicamentos antidiarreicos, como la loperamida, y puede requerir la reducción de la dosis o la interrupción del tratamiento. El tratamiento con OFEV® puede reanudarse a una dosis reducida o a la dosis completa (ver sección Dosis y vía de administración). Si se produce una diarrea grave y persistente a pesar de seguir un tratamiento sintomático, el tratamiento con OFEV® se debe suspender.
Náusea y vómito: Las náuseas y los vómitos fueron reacciones adversas gastrointestinales descritas con frecuencia (ver sección Reacciones secundarias y adversas). En la mayoría de los pacientes con náuseas y vómitos, el episodio presentó una intensidad de leve a moderada. En los estudios INPULSIS, las náuseas causaron la interrupción del tratamiento con OFEV® en el 2.0% de los pacientes y los vómitos causaron la interrupción en el 0.8% de los pacientes. En el estudio INBUILD, la frecuencia de náuseas y vómitos que causaron la interrupción del tratamiento con OFEV® fue de 0.3% y 0.9%, respectivamente. En el estudio SENSCIS, la frecuencia de náuseas y vómitos que causaron la interrupción del tratamiento con OFEV® fue del 2.1% y 1.4%, respectivamente.
Si los síntomas persisten a pesar de recibir un tratamiento de soporte adecuado (incluido un tratamiento antiemético), puede que sea necesario reducir la dosis o interrumpir el tratamiento. El tratamiento puede reanudarse a una dosis reducida o a la dosis completa (ver sección Dosis y vía de administración). Si persisten los síntomas graves, el tratamiento con OFEV® se debe suspender.
La diarrea y los vómitos pueden provocar deshidratación con o sin alteraciones electrolíticas que pueden progresar a deterioro de la función renal.
Función hepática: La seguridad y la eficacia de OFEV® no se han estudiado en pacientes con insuficiencia hepática moderada (Child Pugh B) o grave (Child Pugh C). Por lo tanto, el tratamiento con OFEV® no se recomienda en dichos pacientes (ver sección 4.2). Teniendo en cuenta el aumento de la exposición, el riesgo de reacciones adversas puede aumentar en pacientes con insuficiencia hepática leve (Child Pugh A). Los pacientes con insuficiencia hepática leve (Child Pugh A) deben tratarse con una dosis reducida de OFEV® (ver las secciones Dosis y vía de administración, Farmacocinética).
Se han observado casos de la lesión hepática producida por medicamentos con el tratamiento con nintedaib. En el periodo posterior a la comercialización, se han informado casos serios y casos no serios de daño hepático causado por el medicamento, incluso daño hepático grave con desenlace mortal. La mayoría de los eventos hepáticos ocurren dentro de los primeros tres meses de tratamiento. Por lo tanto, deben determinarse los niveles de bilirrubina y transaminasas hepáticas antes de iniciarse el tratamiento con OFEV®, a intervalos periódicos durante los primeros tres meses de tratamiento y luego a intervalos periódicos (p. ej., en cada visita del paciente) o según esté clínicamente indicado.
Los aumentos de las enzimas hepáticas (ALT, AST, fosfatasa alcalina (FA) en sangre, gammaglutamiltransferasa [GGT]) y de la bilirrubina fueron reversibles en la mayoría de los casos al reducir la dosis o interrumpir el tratamiento. Si se detectan aumentos de las transaminasas (AST o ALT) > 3 veces el LSN, se recomienda reducir la dosis o interrumpir el tratamiento con OFEV®, así como vigilar al paciente de forma estrecha. Una vez que las transaminasas han recuperado los valores basales, el tratamiento con OFEV® se puede reanudar a la dosis completa o reiniciar a una dosis reducida, que después se podrá aumentar a la dosis completa (ver sección Dosis y vía de administración). Si se detecta algún aumento en las pruebas hepáticas asociado a signos o síntomas clínicos de daño hepático, como es la ictericia, el tratamiento con OFEV® se debe suspender de forma permanente. Asimismo, es preciso investigar otras posibles causas de los aumentos de las enzimas hepáticas.
Los pacientes con bajo peso corporal (< 65 kg), los de raza asiática y las mujeres tienen un mayor riesgo de elevaciones de las enzimas hepáticas. La exposición a nintedanib aumentó de manera lineal con la edad del paciente, lo cual puede también aumentar el riesgo de presentar un aumento de las enzimas hepáticas (véase la sección Farmacocinética). Se recomienda un monitoreo estrecho en los pacientes que presenten estos factores de riesgo.
Función renal: Se han notificado casos de insuficiencia/fallo renal, algunos de ellos con un desenlace mortal, con el uso de nintedanib.
Los pacientes deben ser controlados durante el tratamiento con nintedanib, con especial atención aquellos pacientes que presenten factores de riesgo para insuficiencia/fallo renal. En caso de insuficiencia/fallo renal, se debe considerar el ajuste del tratamiento (ver sección Ajustes de la dosis).
Hemorragia: La inhibición del receptor del factor de crecimiento endotelial vascular (VEGF) puede estar asociada a un aumento del riesgo de hemorragia.
Los pacientes con riesgo conocido de presentar sangrado, incluidos los pacientes con una predisposición hereditaria al sangrado o los pacientes que recibían una dosis completa de anticoagulante, no se incluyeron en los ensayos clínicos. Se han notificado episodios de sangrado no graves y graves, algunos de ellos mortales, en el periodo de poscomercialización (incluidos pacientes con o sin tratamiento anticoagulante u otros medicamentos que podrían causar sangrado). Por lo tanto, estos pacientes sólo deben ser tratados con OFEV® si los beneficios esperados superan el riesgo potencial.
Eventos tromboembólicos arteriales: Los pacientes con antecedentes recientes de infarto de miocardio o ictus se excluyeron de los ensayos clínicos.
En los ensayos clínicos, los episodios tromboembólicos arteriales se describieron con poca frecuencia (2.5% con OFEV® frente al 0.7% con placebo en los ensayos INPULSIS; 0.9% con OFEV® frente al 0.9% con placebo en el ensayo INBUILD; 0.7% con OFEV® frente al 0.7% con placebo en el ensayo SENSCIS). En los ensayos INPULSIS, el porcentaje de pacientes que sufrió un infarto de miocardio fue mayor en el grupo tratado con OFEV® (1.6%) que en el grupo tratado con placebo (0.5%), mientras que los efectos adversos que reflejaban una cardiopatía isquémica estuvieron equilibrados entre los grupos de OFEV® y de placebo. En el ensayo INBUILD, se observó infarto de miocardio con una frecuencia baja: 0.9% con OFEV® y 0.9% con placebo. En el ensayo SENSCIS, se observó infarto de miocardio con una baja frecuencia en el grupo de placebo (0.7%) y no se observó en el grupo de OFEV®. Se deben tomar las debidas precauciones cuando se trate a pacientes con un alto riesgo cardiovascular, incluida una enfermedad de las arterias coronarias conocida. En pacientes que desarrollan signos o síntomas de isquemia miocárdica aguda, se debe valorar la necesidad de interrumpir el tratamiento.
Aneurismas y disecciones arteriales: El uso de inhibidores de la vía VEGF en pacientes con o sin hipertensión puede promover la formación de aneurismas y/o disecciones arteriales. Antes de iniciar el tratamiento con OFEV®, este riesgo se debe evaluar de forma cuidadosa en pacientes con factores de riesgo como hipertensión o antecedentes de aneurisma.
Tromboembolismo venoso: En los ensayos clínicos no se observó ningún aumento del riesgo de sufrir tromboembolismo venoso en los pacientes tratados con nintedanib. Debido al mecanismo de acción de nintedanib, los pacientes pueden presentar un riesgo más alto de sufrir episodios tromboembólicos.
Perforaciones gastrointestinales y colitis isquémica: En los ensayos clínicos, la frecuencia de los casos de perforación fue de hasta el 0.3% en ambos grupos de tratamiento. Debido al mecanismo de acción de nintedanib, los pacientes pueden presentar un riesgo más alto de sufrir perforaciones gastrointestinales. Se han notificado casos de perforaciones gastrointestinales y casos de colitis isquémica, algunos de ellos mortales, durante el periodo de poscomercialización. Se deben tomar las debidas precauciones cuando se trate a pacientes que se hayan sometido anteriormente a una cirugía abdominal, tengan antecedentes de úlceras pépticas o enfermedad diverticular o reciban tratamiento concomitante con corticosteroides o AINE. El tratamiento con OFEV® se debe iniciar como mínimo 4 semanas después de una cirugía abdominal. El tratamiento con OFEV® se debe suspender de forma permanente en el caso de pacientes que desarrollen una perforación gastrointestinal o una colitis isquémica. De forma excepcional, se puede reanudar el tratamiento con OFEV® tras la resolución completa de la colitis isquémica y tras una evaluación meticulosa del estado del paciente y de otros factores de riesgo.
Proteinuria en rango nefrótico y microangiopatía trombótica: En el periodo de poscomercialización se han notificado muy pocos casos de proteinuria en rango nefrótico con o sin disfunción renal. Los hallazgos histológicos en casos individuales eran compatibles con microangiopatía glomerular con o sin trombos renales. Se ha observado la desaparición de los síntomas tras suspender el tratamiento con OFEV®, con proteinuria residual en algunos casos.
En pacientes que desarrollan signos o síntomas de síndrome nefrótico se debe valorar la necesidad de interrumpir el tratamiento. Los inhibidores de la vía del VEGF se han asociado a microangiopatía trombótica (MAT), incluido un número muy bajo de informes de casos relacionados con nintedanib. Si se observan hallazgos analíticos o clínicos asociados a MAT en un paciente tratado con nintedanib, se debe interrumpir el tratamiento con nintedanib y se debe llevar a cabo una evaluación meticulosa relacionada con la MAT.
Síndrome de encefalopatía posterior reversible (PRES):
Se han informado muy pocos casos de síndrome de encefalopatía posterior reversible (PRES, posterior reversible encephalopathy syndrome) en la experiencia posterior a la comercialización.
El PRES es un trastorno neurológico que puede presentar cefalea, trastornos visuales, convulsiones, letargo, confusión y otras condiciones neurológicas. Puede presentar hipertensión arterial de leve a grave. Para confirmar el diagnóstico de PRES ser requiere de una resonancia magnética nuclear.
Ante la sospecha de PRES, se debe interrumpir el tratamiento con nintedanib. Se desconoce la seguridad de reiniciar el tratamiento con nintedanib en pacientes con antecedentes de PRES.
Complicaciones en la cicatrización de las heridas: En los ensayos clínicos, no se observó un aumento de la frecuencia de complicaciones en la cicatrización de las heridas. Teniendo en cuenta su mecanismo de acción, nintedanib puede dificultar la cicatrización de las heridas. No se realizaron estudios específicos para evaluar el efecto de nintedanib sobre la curación de las heridas. Así pues, el tratamiento con OFEV® sólo se debe iniciar o, en el caso de una interrupción perioperatoria, reanudar basándose en la evaluación clínica de una adecuada cicatrización de las heridas.
Administración conjunta con pirfenidona: En un estudio farmacocinético específico, se investigó el tratamiento conjunto de nintedanib con pirfenidona en pacientes con FPI. De acuerdo con estos resultados, no existe evidencia de una interacción farmacocinética relevante entre nintedanib y pirfenidona cuando se administran en combinación. Dada la similitud de los perfiles de seguridad de ambos medicamentos, cabe prever reacciones adversas aditivas, incluidas reacciones adversas gastrointestinales y hepáticas. No se ha establecido el balance beneficio-riesgo del tratamiento conjunto con pirfenidona.
Efecto en el intervalo QT: En el programa de ensayos clínicos realizados, no se observó ninguna evidencia de una prolongación del intervalo QT al administrar nintedanib (ver sección 5.1). Como se sabe que algunos otros inhibidores de la tirosina cinasa ejercen un efecto sobre el intervalo QT, se debe tomar precaución cuando se administre nintedanib a pacientes que puedan desarrollar una prolongación del intervalo QTc.
Reacción alérgica: Se sabe que los productos alimenticios con soya provocan reacciones alérgicas, incluido un choque anafiláctico grave en personas con alergia a la soya. Los pacientes con una alergia conocida a la proteína del cacahuate presentan un mayor riesgo de desarrollar reacciones graves a los preparados de soya.
Efectos en la capacidad para conducir y usar maquinaria: La influencia de OFEV® sobre la capacidad para conducir y utilizar máquinas es pequeña. Se aconsejará a los pacientes que tomen las debidas precauciones cuando conduzcan o utilicen máquinas si están siguiendo un tratamiento con OFEV®.
DOSIS Y VÍA DE ADMINISTRACIÓN: El tratamiento debe ser iniciado por médicos con experiencia en el manejo de las enfermedades para las cuales OFEV® está indicado.
La dosis recomendada de 150 mg de nintedanib dos veces al día, administrado aproximadamente con 12 horas de diferencia.
La dosis diaria de 100 mg dos veces al día sólo se recomienda en pacientes que no toleran la dosis diaria de 150 mg dos veces al día.
Si se olvida una dosis, se debe reanudar a la dosis recomendada a la siguiente hora establecida. No se debe superar la dosis diaria máxima recomendada de 300 mg.
Ajuste de la dosis: Además del tratamiento sintomático, si procede, el manejo de las reacciones adversas de OFEV® (véase la sección Precauciones generales, Reacciones adversas) puede incluir la reducción de la dosis y la interrupción temporal del tratamiento hasta que la reacción adversa específica haya alcanzado de nuevo niveles que permitan la continuación del tratamiento. El tratamiento con OFEV® se puede reanudar a la dosis completa (150 mg dos veces al día en pacientes adultos) o a una dosis reducida (100 mg dos veces al día en pacientes adultos). Si un paciente no tolera 100 mg dos veces al día, el tratamiento con OFEV® se debe suspender.
En caso de interrumpir el tratamiento debido al aumento de la aspartato aminotransferasa (AST) o la alanina aminotransferasa (ALT) por encima de 3 veces el límite superior de la normalidad (LSN), una vez que las transaminasas hayan recuperado los valores basales, el tratamiento con OFEV® se puede reanudar a una dosis reducida (100 mg dos veces al día en pacientes adultos), que posteriormente podrá aumentarse a la dosis completa (150 mg dos veces al día en pacientes adultos). (Véase la secciones Precauciones generales, Reacciones adversas).
Poblaciones especiales:
Pacientes de edad avanzada (≥ 65 años):
No se observaron diferencias en general en lo que respecta a la seguridad y la eficacia en los pacientes de edad avanzada en comparación con los pacientes menores de 65 años. No se requiere ajuste de la dosis inicial en los pacientes de edad avanzada (véase la sección Farmacocinética).
Raza:
En función de los análisis de farmacocinética (PK) poblacional, no se requiere a priori ningún ajuste de la dosis de OFEV® (véanse las secciones Poblaciones especiales, Precauciones generales, Farmacocinética). Son limitados los datos de seguridad disponibles en relación con los pacientes de raza negra.
Peso corporal:
En función de los análisis PK poblacional, no se requiere a priori ningún ajuste de la dosis de OFEV® en los pacientes adultos (véase la sección Farmacocinética).
Insuficiencia renal:
Menos del 1% de una dosis única de nintedanib se elimina a través de los riñones (véase la sección Farmacocinética). No es necesario ajustar la dosis inicial en pacientes con insuficiencia renal de leve a moderada. La seguridad, la eficacia y la farmacocinética de nintedanib no se han estudiado en pacientes con insuficiencia renal grave (< 30 ml/min de aclaramiento de creatinina).
Insuficiencia hepática: En pacientes con insuficiencia hepática leve (Child Pugh A), la dosis recomendada de OFEV® es de 100 mg dos veces al día con aproximadamente 12 horas de intervalo entre la administración de las dos dosis. En pacientes con insuficiencia hepática leve (Child Pugh A), se debe considerar la interrupción o la suspensión del tratamiento para el manejo de las reacciones adversas. La seguridad y la eficacia de nintedanib no se han estudiado en pacientes con insuficiencia hepática clasificada como Child Pugh B y C. No se recomienda tratar con OFEV® a pacientes con insuficiencia hepática moderada (Child Pugh B) y grave (Child Pugh C); véase la sección Farmacocinética).
Población pediátrica:
No está registrado el tratamiento de enfermedades pulmonares intersticiales (ILD) fibrosantes con nintedanib para pacientes pediátricos.
Modo de administración:
OFEV® se administra por vía oral. Las cápsulas se deben tomar con alimentos, y tragarse enteras con agua, sin masticarlas.
En el caso de omitirse una dosis, la administración se debe reanudar en el siguiente momento programado con la dosis recomendada. En el caso de omitirse una dosis, no se le debe administrar al paciente una dosis adicional.
Las cápsulas de OFEV® se pueden tomar con una cantidad pequeña (una cucharadita de té) de algún alimento blando, como puré de manzana o budín de chocolate, frío o a temperatura ambiente y se deben tragar sin masticar inmediatamente para asegurar que la cápsula quede intacta. La cápsula no se debe abrir ni partir.
En caso de entrar en contacto con el contenido de la cápsula, se deben lavar las manos inmediatamente con abundante agua.
MANIFESTACIONES Y MANEJO DE LA SOBREDOSIFICACIÓN O INGESTA ACCIDENTAL: No hay ningún antídoto ni tratamiento específico en el caso de producirse una sobredosis de OFEV®. Dos pacientes del programa de oncología presentaron una sobredosis de un máximo de 600 mg dos veces al día durante un máximo de ocho días. Las reacciones adversas observadas coincidieron con el perfil de seguridad conocido de nintedanib, es decir, aumento de las enzimas hepáticas y síntomas gastrointestinales. Ambos pacientes se recuperaron de estas reacciones adversas. En los ensayos INPULSIS, un paciente se expuso de forma accidental a una dosis de 600 mg al día durante un total de 21 días. Durante el periodo de dosificación incorrecta, se produjo y se resolvió un efecto adverso no grave (rinofaringitis), pero no se informó de la aparición de otros episodios. En el caso de producirse una sobredosis, es preciso interrumpir el tratamiento e iniciar las medidas de apoyo generales que resulten adecuadas.
PRESENTACIONES:
Caja con 30 cápsulas de 100 mg o 150 mg.
Caja con 60 cápsulas de 100 mg o 150 mg.
Todas las presentaciones con instructivo anexo.
RECOMENDACIONES SOBRE ALMACENAMIENTO:
Consérvese a no más de 25 °C.
Conservar en el empaque original para protegerlo de la humedad.
LEYENDAS DE PROTECCIÓN:
Literatura exclusiva para médicos. Su venta requiere receta médica. Este medicamento debe ser prescrito por médicos especialistas. No se deje al alcance de los niños. No se use en el embarazo ni en la lactancia ni en menores de 18 años. Este producto contiene lecitina de soya, que puede producir reacciones de hipersensibilidad.
Reporte las sospechas de reacción adversa a los correos: farmacovigilancia@cofepris.gob.mx y
farmacovigilancia.mex@boehringer-ingelheim.com
BOEHRINGER INGELHEIM PROMECO S.A de C.V.
Calle Del Maíz No. 49, Col. Barrio Xaltocan,
C.P. 16090, Xochimilco, Ciudad de México, México
Reg. Núm. 115M2022 SSA IV
®Marca Registrada