COMBIVENT RESPIMAT - Solución para inhalación
Sustancia(s):
- Ipratropio, Salbutamol
Presentaciones:
- 1 Caja, 1 Cartucho con dispositivo, 4 mL, 120 Dosis
FORMA FARMACÉUTICA Y FORMULACIÓN:
Cada mililitro contiene:
Bromuro de Ipratropio monohidratado equivalente a 1.68 mg de Bromuro de Ipratropio
Sulfato de Salbutamol equivalente a 8.77 mg de Salbutamol
Vehículo cbp 1 mL
COMBIVENT® RESPIMAT® proporciona 120 dosis (equivalente a 120 disparos).
Cada dosis contiene:
Bromuro de Ipratropio monohidratado equivalente a 20 mcg de bromuro de Ipratropio
Sulfato de Salbutamol equivalente a 100 mcg de Salbutamol
INDICACIONES TERAPÉUTICAS: COMBIVENT® RESPIMAT® solución para inhalación está indicado para el tratamiento del broncoespasmo reversible, que acompaña a las enfermedades obstructivas de vías aéreas, en pacientes que requieran de la administración de más de un broncodilatador.
FARMACOCINÉTICA Y FARMACODINAMIA:
Grupo farmacoterapéutico: Adrenérgicos en combinación con anticolinérgicos para las enfermedades de las vías aéreas obstructivas.
Código ATC: R03AL02.
Mecanismo de acción:
El bromuro de ipratropio es un compuesto de amonio cuaternario con propiedades anticolinérgicas (parasimpatolíticas). En estudios preclínicos, parece inhibir los reflejos vagales antagonizando la acción de su agente transmisor, la acetilcolina el agente transmisor liberado por el nervio vago. Los anticolinérgicos previenen el incremento en la concentración intracelular de Ca++ que es causado por la interacción de acetilcolina con el receptor muscarínico del músculo liso bronquial. La liberación de Ca++ está mediada por el sistema de segundo mensajero, que consiste de IP3 (inositol trifosfato) y DAG (diacilglicerol).
Farmacodinamia: La broncodilatación después de la inhalación del bromuro de ipratropio es principalmente local y específica del sitio en relación a los pulmones y no es de naturaleza sistémica.
El sulfato de salbutamol es un agente β2-adrenérgico que actúa sobre el músculo liso de las vías respiratorias produciendo relajación. El salbutamol relaja el músculo liso desde la tráquea hasta los bronquiolos terminales y protege en contra de todos los retos broncoconstrictores. COMBIVENT® proporciona la liberación simultánea del bromuro de ipratropio y del sulfato de salbutamol, permitiendo el efecto aditivo sobre los receptores muscarínicos y β2-adrenérgicos pulmonares produciendo una broncodilatación superior a la ocasionada por cada agente por separado.
Estudios clínicos: Los estudios controlados en pacientes con broncoespasmo reversible han demostrado que COMBIVENT® tiene un mayor efecto broncodilatador que cualquiera de sus componentes y no hubo ninguna potenciación de los eventos adversos.
En un estudio de 12 semanas, aleatorizado, multicéntrico, doble ciego, con doble simulación y de grupos paralelos, se evaluó la eficacia broncodilatadora, en 1,424 pacientes con EPOC, de COMBIVENT® RESPIMAT® solución para inhalación (20/100 μg) (474 pacientes) en comparación con COMBIVENT® suspensión, inhalación presurizada (42/240 μg ex-válvula) (482 pacientes), y bromuro de ipratropio suministrado por el inhalador COMBIVENT® RESPIMAT® (20 μg) (468 pacientes).
Las mediciones seriadas del VEF1 (mostradas en la Fig. 1 como cambio en VEF1 desde la línea basal del día de prueba) en los días de prueba 1, 29, 57 y 85 mostraron que COMBIVENT® RESPIMAT® solución para inhalación (20/100 μg) fue terapéuticamente equivalente a COMBIVENT® suspensión, inhalación presurizada (42/240 μg ex-válvula) y ambas formulaciones produjeron una mejoría significativamente mayor en el funcionamiento pulmonar en comparación con bromuro de ipratropio cuando se administró por separado.
La mediana del tiempo hasta el inicio, la respuesta máxima y la mediana de la duración de la respuesta fueron comparables para COMBIVENT® RESPIMAT® solución para inhalación (20/100 μg) y para COMBIVENT® suspensión, inhalación presurizada (42/240 μg ex-válvula).
Figura 1. Perfil de tiempo de VEF1 en los días 1, 29, 57 y 85
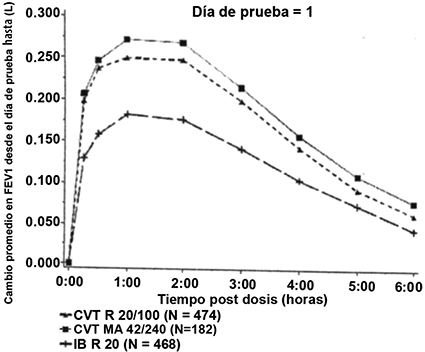
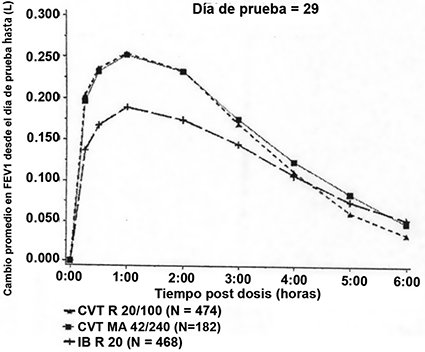
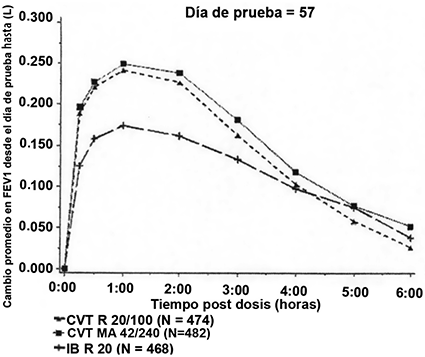
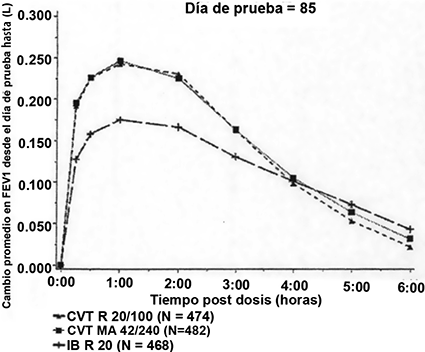
Los promedios son ajustados por el tratamiento basal y el sitio del investigador. Un ANCOVA por separado fue adaptado para cada punto de tiempo.
El método de imputación para datos faltantes debido a que el paciente se retiró del estudio fue hecho con la última vista realizada.
El método de imputación para datos faltantes al final de los días de prueba depende de por qué faltan los datos.
Conjunto de análisis: Conjunto de análisis completo de espirometría clínica 1012.56 (N = 1,424).
Promedio de tratamiento basal = 1.114 L.
Farmacocinética: Desde una perspectiva farmacocinética, la eficacia observada en los ensayos clínicos en el aerosol por Inhalación de COMBIVENT® suspensión, inhalación presurizada, se debe a un efecto local en el pulmón posterior a la inhalación.
Después de la inhalación de un 10 a un 39% de una dosis se deposita generalmente en los pulmones, dependiendo de la formulación, la técnica de la inhalación y el dispositivo, mientras que el resto de la dosis administrada se deposita en la boquilla, la boca y la parte superior del tracto respiratorio (orofaringe).
En particular después de la inhalación de la solución acuosa vía el inhalador RESPIMAT®, se observa de manera experimental un depósito de más del doble en el pulmón en comparación con la del aerosol de dosis medida. El depósito orofaríngeo disminuye de manera correspondiente y es significativamente menor con el inhalador RESPIMAT® en comparación con la suspensión, inhalación presurizada. La porción de la dosis depositada en los pulmones llega a la circulación rápidamente (en cuestión de minutos). La cantidad de la sustancia activa depositada en la orofaringe se traga lentamente y pasa al tracto gastrointestinal. Por lo tanto, la exposición sistémica es una función tanto de la biodisponibilidad oral como de la pulmonar.
La coadministración de bromuro de ipratropio y sulfato de salbutamol no potencia la absorción sistémica de ninguno de los componentes por lo cual la acción aditiva de COMBIVENT® se debe al efecto local combinado sobre el pulmón, tras la inhalación.
Ipratropio:
Absorción: La excreción renal acumulada (0-24 hrs), del ipratropio (compuesto base) es por debajo del 1% de una dosis oral y aproximadamente entre 3-13% de una dosis inhalada. Con base en estos datos, la biodisponibilidad total sistémica de dosis orales e inhaladas del bromuro de ipratropio se estima en un 2% y 7 a 28% respectivamente. Tomando esto en cuenta, las porciones de dosis tragadas del bromuro de ipratropio no contribuyen de una forma relevante a la exposición sistémica.
Distribución: Los parámetros cinéticos que describen la disposición del ipratropio se calcularon a partir de concentraciones en plasma después de la administración I.V. Se observa un rápido descenso bifásico en las concentraciones en plasma. El volumen aparente de distribución en estado estable (Vdss) es de aproximadamente 176 L (≈ 2.4 L/kg). El fármaco se une mínimamente a las proteínas plasmáticas (menos de 20%). Los datos preclínicos indican que la amina cuaternaria del ipratropio no atraviesa la barrera hematoencefálica.
Los principales metabolitos urinarios se unen de manera pobre al receptor muscarínico y deben ser considerados como inefectivos.
Biotransformación: Después de la administración intravenosa aproximadamente un 60% de la dosis se metaboliza en el hígado, la mayor parte probablemente por oxidación.
Eliminación: La vida media de la fase terminal de eliminación es de aproximadamente 1.6 horas. El ipratropio tiene un tiempo total de depuración de 2.3 L/min y una depuración renal de 0.9 L/min. En un estudio de balance de excreción, la excreción acumulada renal (6 días) de radiactividad relacionada con el fármaco (incluyendo al compuesto base y a todos los metabolitos) generó 9.3% después de la administración oral y 3.2% después de la inhalación. La radiactividad total excretada a través de las heces fue de 88.5% posterior a la dosis oral y 69.4% posterior a la inhalación. La vida media de eliminación de la radiactividad relacionada con el fármaco (compuesto base y metabolitos) es de 3.6 horas. Salbutamol:
Absorción y distribución: El salbutamol es rápida y completamente absorbido después de la administración oral ya sea vía inhalada o gástrica y tiene una biodisponibilidad oral de aproximadamente 50%. Las concentraciones plasmáticas máximas de 492 pg/mL ocurren dentro de las primeras tres horas después de la inhalación de COMBIVENT®. Se calcularon los parámetros cinéticos a partir de las concentraciones en plasma después de la administración I.V. El volumen aparente de distribución (Vz) es de aproximadamente 156 L (≈ 2.5 L/kg). Sólo un 8% del fármaco se une a las proteínas plasmáticas. En estudios preclínicos, aproximadamente el 5% de la concentración plasmática de Salbutamol se encuentra en el cerebro. Sin embargo, esta cantidad probablemente representa la distribución de la sustancia en el líquido extracelular del cerebro.
Biotransformación y eliminación:
Después de una única inhalación, se estima que alrededor del 27% de la dosis suministrada por la boquilla se excreta sin modificación en la orina de 24 horas. La vida media terminal es de aproximadamente 4 horas con una depuración total media de 480 mL/min y una depuración renal media de 291 mL/min.
El salbutamol se metaboliza de forma conjugada con el sulfato 4"-O- salbutamol. El R(-)- enantiómero de salbutamol (levosalbutamol) se metaboliza preferentemente y por lo tanto es depurado del cuerpo más rápidamente que el S(+)-enantiómero. Después de la administración oral la excreción urinaria del fármaco inalterado y el conjugado de sulfato representaron 31.8% y 48.2% de la dosis, respectivamente.
Comparación de la exposición sistémica al ipratropio y al salbutamol después de la inhalación de COMBIVENT® RESPIMAT® solución para inhalación y COMBIVENT® suspensión, inhalación presurizada.
La exposición sistémica en estado estable al ipratropio y salbutamol después de la inhalación vía COMBIVENT® suspensión, inhalación presurizada o COMBIVENT® RESPIMAT® solución para inhalación se comparó en un estudio fase III. La exposición sistémica de ambos componentes activos se calculó a partir de muestras de plasma y orina de 108 pacientes con EPOC que recibieron COMBIVENT® RESPIMAT® solución para inhalación (20/100 mcg) o COMBIVENT® suspensión, inhalación presurizada (42/240 mcg) cuatro veces al día. La exposición sistémica en estado estable obtenida por el ipratropio después de COMBIVENT® RESPIMAT® solución para inhalación (20/100 mcg) fue comparable a la de COMBIVENT® suspensión, inhalación presurizada, (42/240 mcg) (las razones de exposición sistémica de salbutamol plasmático y urinario para COMBIVENT® RESPIMAT® solución para inhalación/COMBIVENT® suspensión, inhalación presurizada fueron 1.04 y 1.18); la exposición sistémica al salbutamol fue menor (las razones de exposición sistémica de salbutamol plasmático y urinario para COMBIVENT® RESPIMAT® solución para inhalación/COMBIVENT® suspensión, inhalación presurizada fueron 0.74 y 0.86) porque menos salbutamol del inhalador Respimat® que del inhalador en aerosol de dosis medida está disponible para la absorción oral.
Análisis por subgrupos: Los datos farmacocinéticos en estado estable de 52 pacientes tratados con COMBIVENT® RESPIMAT® solución para inhalación (20/100 mcg) se organizaron en subgrupos por edad y género. Consistente con COMBIVENT® suspensión, inhalación presurizada (42/240 μg ex-válvula), los pacientes que recibieron COMBIVENT® RESPIMAT® solución para inhalación (20/100 μg) con edades de 65 años o mayores tuvieron las exposiciones sistémicas en estado estable de ipratropio más altas (Cmáx. = 38.5 pg./mL) y de salbutamol (Cmáx. = 1.19 ng./mL) que los pacientes menores de 65 años (Cmáx. = 30.1 pg./mL, 0.74 ng./mL respectivamente), después de la administración de COMBIVENT® RESPIMAT® solución para inhalación (20/100 μg). Los pacientes de ambos sexos tuvieron comparables exposiciones sistémicas de ipratropio y salbutamol después de la administración de COMBIVENT® RESPIMAT® solución para inhalación (20/100 μg).
CONTRAINDICACIONES:
COMBIVENT® está contraindicado en:
• Pacientes con cardiomiopatía hipertrófica obstructiva o taquiarritmia.
• Pacientes con hipersensibilidad conocida a la atropina o sus derivados o algún otro componente del producto.
RESTRICCIONES DE USO DURANTE EL EMBARAZO Y LA LACTANCIA:
Embarazo: La seguridad de COMBIVENT® RESPIMAT® durante el embarazo humano no se ha establecido. Debe de tomarse en consideración el efecto inhibitorio de COMBIVENT® sobre las contracciones uterinas. Los beneficios de utilizar COMBIVENT® durante un embarazo confirmado o del cual se sospecha deberán ponderarse en relación con los posibles riesgos al producto aún no nacido. Deben tenerse presentes las precauciones habituales en relación al uso de fármacos en el embarazo, especialmente durante el primer trimestre.
Para el bromuro de ipratropio los estudios preclínicos han demostrado que no hay efectos embriotóxicos o teratogénicos posteriores a la inhalación o la aplicación intranasal a dosis considerablemente mayores que las recomendadas en el hombre. Para el sulfato de salbutamol los estudios preclínicos de no inhalación no indican efectos dañinos directos o indirectos a menos de que se excediera la Dosis Máxima Diaria Recomendada para Humanos (MRHDD) por sus siglas en inglés) (Ver sección X. Precauciones y relación con efectos de carcinogénesis, mutagénesis, teratogénesis y sobre la fertilidad).
Lactancia: No se sabe si el bromuro de ipratropio y el sulfato de salbutamol son excretados en la leche materna. Es improbable que el bromuro de Ipratropio alcance al infante en un grado importante, cuando se administra mediante inhalación. Sin embargo, debe de tenerse precaución cuando el COMBIVENT® se administre a una mujer en periodo lactante.
Fertilidad: No se han llevado a cabo estudios del efecto sobre la fertilidad de COMBIVENT®. No se dispone de datos clínicos sobre la fertilidad para la combinación de bromuro de ipratropio y sulfato de salbutamol ni para ninguno de los componentes individuales de la combinación. Los estudios preclínicos realizados con bromuro de ipratropio y salbutamol no mostraron efectos adversos sobre la fertilidad (Ver sección XII. Precauciones y relación con efectos de carcinogénesis, mutagénesis, teratogénesis y sobre la fertilidad).
Efectos sobre la habilidad para manejar y usar maquinaria: No se han llevado a cabo estudios sobre los efectos en la habilidad para manejar y usar maquinaria.
Sin embargo, deberá advertírseles a los pacientes que pueden experimentar efectos indeseables tales como mareo, trastornos acomodativos, midriasis y visión nublada durante el tratamiento con COMBIVENT®. Por lo tanto, deberá recomendarse precaución cuando manejen un auto u operen maquinaria.
REACCIONES SECUNDARIAS Y ADVERSAS:
Resumen del perfil de seguridad: Muchos de los efectos no deseados que aparecen en la lista pueden atribuirse a las propiedades anticolinérgicas y beta2-simpaticomiméticas de COMBIVENT®. Al igual que todas las terapias de inhalación COMBIVENT® puede mostrar síntomas de irritación local.
Los efectos secundarios más frecuentes reportados en estudios clínicos fueron cefalea, irritación de garganta, tos, boca seca, trastornos de la motilidad gastrointestinal (incluyendo constipación diarrea y vómito), náusea y mareo.
Tabla de resumen de las reacciones adversas:
Se han informado las siguientes reacciones adversas durante el uso de COMBIVENT® en ensayos clínicos y durante la experiencia posterior a la comercialización.
|
Terminología de clasificación de órganos del sistema MedDRA |
Reacciones adversas COMBIVENT® |
|
Trastornos del sistema inmunológico |
Reacción anafiláctica Hipersensibilidad |
|
Trastornos del metabolismo y de la nutrición |
Hipokalemia |
|
Trastornos psiquiátricos |
Nerviosismo Trastorno mental |
|
Trastornos del sistema nervioso |
Cefalea Temblores Vértigo |
|
Trastornos oculares |
Trastorno de acomodación Edema corneal Glaucoma Incremento de la presión intraocular Midriasis Visión borrosa Dolor ocular Hiperemia conjuntival Visión con halo |
|
Trastornos cardiacos |
Palpitaciones Taquicardia Arritmia Fibrilación auricular Taquicardia supraventricular Isquemia del miocardio |
|
Trastornos respiratorios, torácicos y mediastinales |
Tos Disfonia Garganta seca Broncoespasmo Bronco espasmo paradójico Laringoespasmo Edema faríngeo |
|
Trastornos gastrointestinales |
Boca seca Náusea Garganta irritada Diarrea Vómito Constipación Trastorno de motilidad gastrointestinal Edema de la boca Estomatitis |
|
Trastornos de piel y del tejido subcutáneo |
Reacciones en la piel tales como: • Rash • Prurito • Urticaria Angioedema Hiperhidrosis |
|
Trastornos músculoesqueléticos y del tejido conectivo |
Espasmos musculares Debilidad muscular Mialgia |
|
Trastornos renales y urinarios |
Retención urinaria |
|
Trastornos generales y condiciones del sitio de administración |
Astenia |
|
Investigaciones |
Disminución de la presión arterial diastólica. Incremento de la presión arterial sistólica |
PRECAUCIONES EN RELACIÓN CON EFECTOS DE CARCINOGÉNESIS, MUTAGÉNESIS, TERATOGÉNESIS Y SOBRE LA FERTILIDAD:
Toxicidad de dosis única: La toxicidad aguda de COMBIVENT® después de una sola inhalación fue probada en ratas y perros. Hasta la dosis más alta técnicamente posible (ratas: 887/5397 mcg/kg bromuro de ipratropio/salbutamol, perro: 164/861 mcg/kg bromuro de ipratropio/salbutamol, no se encontraron indicios de efectos tóxicos sistémicos, la combinación fue localmente bien tolerada.
La DL50 aproximada después de la administración intravenosa se ha calculado para cada sustancia en particular entre 12 y 20 mg/kg para el bromuro de ipratropio y entre 60 y 73 mg/kg para el sulfato de salbutamol en función de la especie (ratón, rata, perro).
Toxicidad de dosis múltiples: Se han realizado dos estudios de 13 semanas con la combinación de bromuro de ipratropio y sulfato de salbutamol para evaluar la toxicidad por inhalación en ratas y perros. En estos estudios, el corazón resultó ser el órgano blanco. En la rata en dosis de 34/197 a 354.5/2604 mcg/kg/día de bromuro de ipratropio/sulfato de salbutamol, se presentó incremento en el peso del corazón dependiente de la dosis, sin embargo sin ningún tipo de correlación histopatológica. En el perro a dosis de 32/198 a 129/790 mcg/kg/día bromuro de ipratropio/sulfato de salbutamol, aumentó ligeramente el ritmo cardiaco y, con dosis más altas, se observaron cicatrices detectables histopatológicamente y/o fibrosis en el músculo papilar del ventrículo izquierdo, en ocasiones acompañadas de mineralización.
Los hallazgos cardiovasculares obtenidos en los estudios antes mencionados deben ser considerados como los efectos conocidos de los beta-adrenérgicos, como el salbutamol. El perfil toxicológico de (bromuro de ipratropio) también es conocido desde hace muchos años y se caracteriza por los típicos efectos anticolinérgicos como son la sequedad de las membranas mucosas de la cabeza, midriasis, queratoconjuntivitis seca (ojo seco) que se presentan solamente en los perros, reducción de tono e inhibición de la motilidad del tracto gastrointestinal (ratas).
Toxicidad reproductiva: Estudios de la toxicidad reproductiva están disponibles para los dos componentes individuales de COMBIVENT®. En los ratones, el sulfato de salbutamol en altas dosis subcutáneas causa paladar hendido. Empezando en dosis dentro del rango de inhalación MRHDD (basado en mg/m2). Sin embargo, este fenómeno es bien conocido y ocurre también después de la administración de otros compuestos beta-adrenérgicos. Actualmente se asume que este efecto es provocado por un incremento en el nivel de corticoesterona materna y puede considerarse como un resultado del estrés general no relevante para otras especies. Aparte de estos hallazgos, los estudios realizados con sulfato de salbutamol y con bromuro de ipratropio revelaron sólo efectos marginales, si acaso, en el embrión, feto y cachorros y estos sólo en el rango de toxicidad materna. El bromuro de ipratropio no afectó la fertilidad de las ratas macho ni hembra en dosis orales de hasta 50 mg/kg (aproximadamente 3400 veces la DMDRH sobre la base de la relación mg/m2). Los estudios de reproducción en ratas con salbutamol no revelaron indicios de deterioro de la fertilidad.
Genotoxicidad: Ambas sustancias individuales se probaron en numerosos estudios para evaluar la genotoxicidad in-vivo e in-vitro. Ni el sulfato de salbutamol ni el bromuro de ipratropio probaron evidencia de propiedades mutagénicas. Además COMBIVENT® no demostró actividad genotóxica en estudios in-vitro.
Carcinogenicidad: El sulfato de salbutamol y el bromuro de ipratropio se probaron en varios estudios individualmente para evaluar sus propiedades neoplásicas en varios estudios de carcinogenicidad. Después de la administración oral del sulfato de salbutamol en ratas, pero no en ratones, hámsters y perros, se observó un incremento en la incidencia de leiomiomas del meso-ovario a dosis inhaladas alrededor > = 20 veces mayores a la MRHDD. El desarrollo de los leiomiomas se encontró que era prevenible con la administración simultánea de beta-bloqueadores. Estos hallazgos se evaluaron como especie-específicos y, por lo tanto, sin relevancia clínica, consecuentemente no llevaron a alguna restricción en el uso clínico del sulfato de salbutamol.
El bromuro de ipratropio no reveló potencial carcinógenico cuando se probó oralmente en ratones y ratas.
Inmunogenicidad: No se encontró evidencia de algún efecto inmunotoxicológico causado por COMBIVENT® o alguno de sus componentes activos individuales.
INTERACCIONES MEDICAMENTOSAS Y DE OTRO GÉNERO:
La administración concomitante crónica de COMBIVENT® con otros fármacos anticolinérgicos no ha sido estudiada; por lo tanto, no se recomienda la administración concomitante crónica de COMBIVENT® con otros anticolinérgicos.
La administración concurrente de derivados de xantina así como de otros β-adrenérgicos y anticolinérgicos puede aumentar los efectos adversos.
Los β2-adrenérgicos inducen hipokalemia que puede incrementarse con el uso concomitante de derivados de la xantina, glucocorticoides y diuréticos. Debe tenerse esto presente especialmente en los pacientes con grave obstrucción de las vías respiratorias.
La hipokalemia puede incrementar la susceptibilidad a las arritmias en los pacientes tratados con digoxina.
Se recomienda en tales situaciones una vigilancia de los niveles séricos de potasio.
Puede ocurrir una importante reducción del efecto broncodilatador durante la administración concomitante con β-bloqueadores.
Se deben administrar con precaución los medicamentos que contengan beta adrenérgicos en los pacientes que se encuentren sometidos a un tratamiento con inhibidores de la MAO o con antidepresivos tricíclicos, ya que éstos pueden potenciar los efectos de los fármacos primeramente citados.
La administración simultánea de anestésicos halogenados como el halotano, tricloroetileno o el enflurano, puede aumentar el potencial de efectos cardiovasculares de los beta-agonistas.
ALTERACIONES EN LOS RESULTADOS DE PRUEBAS DE LABORATORIO: En algunas ocasiones, con tratamientos β2-agonistas, pueden presentarse datos de hipokalemia, pero, en general, no presenta alteraciones (salbutamol), en pruebas de laboratorio.
El uso de COMBIVENT® puede conducir a resultados positivos con respecto a salbutamol en pruebas para el abuso de sustancias no clínicas, por ejemplo, en el desempeño atlético (dopaje).
PRECAUCIONES GENERALES:
Hipersensibilidad: Podrían ocurrir reacciones de hipersensibilidad inmediata después de la administración de COMBIVENT®, como se demostró en casos raros de urticaria, angioedema, eritema, broncoespasmo y edema orofaríngeo.
Broncoespasmo paradójico:
Al igual que con otros medicamentos inhalables, existe la posibilidad de que COMBIVENT® provoque un espasmo paradójico, cuadro potencialmente fatal. En caso de producirse un espasmo paradójico, debe suspenderse de inmediato el uso de COMBIVENT® y debe utilizarse otra terapia en su reemplazo.
Complicaciones oculares:
Hay reportes aislados de complicaciones oculares (por ejemplo, midriasis, incremento en la presión intraocular, glaucoma de ángulo cerrado, dolor ocular) cuando el bromuro de ipratropio en aerosol solo o combinado con un β2-agonista ha sido aplicado involuntariamente cerca de los ojos.
El dolor ocular o incomodidad, visión borrosa, halos visuales o imágenes coloreadas en asociación con ojos rojos por congestión conjuntival y edema corneal pueden ser signos de glaucoma de ángulo cerrado. Ante el desarrollo de cualquier combinación de estos síntomas, debe iniciarse el tratamiento con gotas mióticas y debe buscarse atención médica especializada inmediatamente.
Los pacientes deben ser instruidos respecto a la correcta administración de COMBIVENT®. Se debe de tener cuidado para evitar que la solución o el aerosol entre a los ojos. Los pacientes con predisposición al glaucoma deben de ser advertidos de manera específica de que protejan sus ojos.
Efectos sistémicos:
En las siguientes situaciones, COMBIVENT® sólo puede ser utilizado después de una cuidadosa valoración de la relación riesgo/beneficio, especialmente cuando se utilicen dosis más altas de las recomendadas: diabetes insuficientemente controlada, infarto al miocardio reciente, trastornos cardiovasculares funcionales graves, hipertirodismo, feocromocitoma, riesgo de glaucoma de ángulo cerrado, hipertrofia prostática u obstrucción del cuello vesical.
Efectos cardiovasculares: Se han observado efectos cardiovasculares con medicamentos simpaticomiméticos, incluyendo COMBIVENT®.
Existe cierta evidencia de datos post-comercialización y literatura publicada de ocurrencias raras de isquemia miocárdica asociada con salbutamol. Los pacientes con enfermedad cardiaca grave subyacente (por ejemplo, cardiopatía isquémica, arritmia o insuficiencia cardiaca grave) que están recibiendo salbutamol para alguna enfermedad respiratoria, deben de ser advertidos para que busquen apoyo médico en caso de que experimenten dolor torácico u otros síntomas de empeoramiento de enfermedad cardiaca. Deberá ponerse especial atención a la evaluación de los síntomas como dolor torácico y disnea, ya que pueden ser de origen cardiaco o respiratorio.
Hipokalemia: El tratamiento con β2-agonistas puede tener como consecuencia una hipokalemia potencialmente grave. Además, la hipoxia, puede agravar los efectos de la hipokalemia sobre el ritmo cardiaco. En tales situaciones, se recomienda monitorear la concentración sérica de potasio.
Alteraciones de la motilidad gastrointestinal:
Los pacientes con fibrosis quística podrían ser más propensos a alteraciones de la motilidad gastrointestinal.
Disnea:
En caso de que se presente disnea aguda o que ésta empeore se debe indicar a los pacientes que consulten inmediatamente a un médico.
Cloruro de Benzalconio:
Este medicamento contiene 0,00114 mg de cloruro de benzalconio en cada actuación.
El cloruro de benzalconio puede causar sibilancias y dificultades para respirar. Los pacientes con asma tienen un mayor riesgo de estos eventos adversos.
Uso incorrecto de COMBIVENT® RESPIMAT®:
Los cartuchos de COMBIVENT® RESPIMAT® se deben utilizar únicamente con el inhalador de COMBIVENT® RESPIMAT®.
DOSIS Y VÍA DE ADMINISTRACIÓN: Se les debe aconsejar a los pacientes que consulten de inmediato a un médico o que acudan al hospital más cercano en caso de rápido deterioro o incremento de la disnea (dificultad respiratoria) si las inhalaciones adicionales de COMBIVENT® no producen la mejoría adecuada.
En caso de requerir dosis de COMBIVENT® más altas que las recomendadas para controlar los síntomas, se deberá revisar el plan terapéutico del paciente.
En asma se debe considerar la terapia anti-inflamatoria concomitante.
Las siguientes dosis de COMBIVENT® RESPIMAT® solución para inhalación son recomendadas (incluyendo pacientes de la tercera edad).
Vía de administración: Oral por inhalación.
Niños a partir de 5 años y hasta 12 años: 1 inhalación cada 8 horas.
Niños mayores de 12 años y adultos: 1 inhalación cada 6 horas (consultar instrucciones de uso).
La dosis se puede incrementarse según lo requerido hasta un límite de 6 inhalaciones en 24 horas.
En pacientes de 5 a 12 años el uso de COMBIVENT® RESPIMAT® solución para inhalación debe ser bajo supervisión médica.
Poblaciones especiales:
Pacientes con insuficiencia renal o hepática:
COMBIVENT® no se ha estudiado en pacientes con insuficiencia renal o hepática: Se debe utilizar con precaución en dichas poblaciones de pacientes.Instrucciones de uso:
Lea previamente las instrucciones.
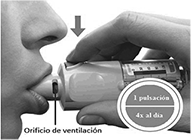
La dosis recomendada es de cuatro veces al día. Cada vez que se use es por una pulsación.

• Si no se ha utilizado por más de 3 días, realice un disparo hacia el suelo.
• Si no se ha utilizado por más de 21 días, repita los pasos 4 a 6 señalados en “Preparación para el primer uso” hasta que la vaporización sea visible. Luego, repita los pasos 4 a 6 tres veces más.
Cuidados del COMBIVENT® RESPIMAT®
Limpia la boquilla incluyendo la parte de metal dentro de la boquilla con un paño húmedo o un pañuelo al menos una vez a la semana.
Cualquier decoloración menor en la boquilla no afecta el funcionamiento del COMBIVENT® RESPIMAT®.
¿Cuándo se debe cambiar el inhalador COMBIVENT® RESPIMAT® por uno nuevo?

• El inhalador de COMBIVENT® RESPIMAT® contiene 120 disparos (igual a 120 dosis de medicamento) si se usa como se indica (un disparo/cuatro veces al día).
• El indicador muestra aproximadamente la cantidad de medicamento que resta.
• Cuando el indicador se encuentra en el área roja es necesario obtener una receta nuevamente, ya que le restan aproximadamente 7 días de medicamento antes de que se termine (28 disparos).
• Una vez que el indicador de COMBIVENT® RESPIMAT® llega al final del área roja, éste se bloquea automáticamente evitando la liberación de más dosis. En este punto, la base transparente no podrá girarse nuevamente.
• Tres meses después del primer uso, el inhalador COMBIVENT® RESPIMAT® debe ser desechado, incluso aun cuando no haya sido utilizado por completo.
Preparación para el primer uso:
|
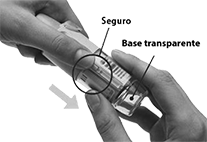
1. Retire la base transparente • Mantenga la tapa cerrada. • Presione el botón de seguridad mientras quita la base transparente con la otra mano. |
|
|
2. Inserte el cartucho • Inserte el extremo más estrecho del cartucho en el inhalador. • Coloque el inhalador en una superficie firme y empuje hacia abajo con firmeza hasta que encaje en su lugar. |
|
|
3. Vuelva a colocar la base transparente • Ponga la base transparente en su lugar hasta que haga “CLICK”. |
|
|
4. Gira • Mantenga la tapa cerrada. • Gira la base transparente en el sentido de las flechas sobre la etiqueta hasta que haga click (medio giro). |
|
|
5. Abrir • Abrir la tapa hasta que encaje completamente. |
|
|
6. Presione • Apunte el inhalador hacia el suelo. • Presione el botón de liberación de dosis. • Cerrar la tapa. • Repita los pasos 4-6 hasta que la nube sea visible, repita los pasos 4-6 tres veces más. |
|
Uso diario:
|
GIRAR • Mantenga la tapa cerrada. • GIRE la base transparente en el sentido de las flechas en la etiqueta hasta que se acomode (medio giro). |
|
|
ABRIR • Quite la tapa hasta que quede totalmente abierta. |
|
|
PRESIONE • Exhale lentamente y por completo. • Cierre los labios alrededor de la boquilla del inhalador cuidando no cubrir las rendijas del inhalador. • Mientras toma una lenta y profunda respiración por la boca PRESIONE el botón de liberación de la dosis y continúe inhalando. • Mantenga la respiración durante 10 segundos o hasta que se sienta cómodo. • Cierre la tapa hasta que utilice de nuevo el inhalador. |
|
MANIFESTACIONES Y MANEJO DE LA SOBREDOSIFICACIÓN O INGESTA ACCIDENTAL:
Síntomas: Los efectos por sobredosificación deben atribuirse principalmente al salbutamol. Los síntomas esperados por la sobredosis son aquellos relacionados con la sobreestimulación beta-adrenérgica, los más importantes son taquicardia, palpitaciones, temblores, hipertensión, hipotensión, hipokalemia, aumento en la amplitud de la presión del pulso, dolor anginoso, arritmias y rubor. Se ha observado también acidosis metabólica con sobredosis de salbutamol.
Los síntomas esperados de la sobredosis con el bromuro de ipratropio (tales como boca seca, alteraciones de la acomodación visual) son leves y de naturaleza transitoria en vista de la administración tópica y del amplio rango terapéutico.
Terapia: Debe interrumpirse el tratamiento con COMBIVENT®. Debe considerarse el monitoreo de los valores electrolíticos y del equilibrio ácido-base.
Administración de sedantes y, en casos severos, hospitalización en terapia intensiva puede ser necesaria.
Los β-bloqueadores, preferentemente los β1 selectivos son adecuados como antídotos específicos. Sin embargo, se debe de tomar en consideración un incremento posible en la obstrucción bronquial y la dosis debe de ajustarse cuidadosamente en pacientes que sufren de asma bronquial.
PRESENTACIÓN: Caja con cartucho de 4.0 mL que contiene 120 dosis y dispositivo dosificador (RESPIMAT®) e instructivo.
RECOMENDACIONES SOBRE ALMACENAMIENTO: Consérvese a no más de 25 °C.
LEYENDAS DE PROTECCIÓN:
Literatura exclusiva para médicos. Su venta requiere receta médica. Almacenar en un lugar seguro. No se deje al alcance de los niños. El empleo de este medicamento durante el embarazo y la lactancia queda bajo la responsabilidad del médico. Una vez insertado el cartucho, el producto se conserva por 3 meses.
Reporte las sospechas de reacción adversa a los correos:
farmacovigilancia@cofepris.gob.mx y
farmacovigilancia.mex@boehringer-ingelheim.com
BOEHRINGER INGELHEIM PROMECO, S.A. de C.V.
Calle del Maíz No. 49, Col. Barrio Xaltocan,
C.P. 16090, Xochimilco, Ciudad de México, México
Reg. Núm. 261M97, SSA IV
®Marca registrada